
目前关于2019-nCoV的感染机理研究才刚刚起步,不过由于其与其他冠状病毒结构上的类似性,其入侵过程应该与其他致病性人类冠状病毒相似。人们可以设计药物对这七个步骤进行干预,不论在哪一步阻断住病毒的进程,疾病便会得到控制。现行的抗病毒方法主要分为三类:血清/抗体疗法,疫苗疗法,化学药物疗法。 |
|
|
理论上来说,很多痊愈患者在自身对抗病毒的过程中产生了专杀新型冠状病毒的抗体,是不是只要从他们血液中提取就行了呢?答案是否定的。
- 血清成分复杂,人体产生的抗体又是与其自身免疫系统相匹配的,如果强行用在他人身上会引起排异反应,从而造成危险;
- 人体不是生物反应器,体内本身这种抗体存货就不多,抗体在应对病毒后会有所减少,再加上提取过程中的损耗,抗体是完全不够用的;
- 单抗制作周期长,费用高昂,大面积用于现有病患不太现实。
疫苗自不用说,天花就被我们用疫苗给干掉了,但一些善变的单链RNA病毒却没那么好对付,疫苗擅长应对相对“稳重”的DNA病毒,天花病毒就是这种太过“稳重”的DNA双链结构,难以快速发生变异而被人类消灭了。因为疫苗的原理就是注射抗原模拟病毒刺激体内免疫反应,一种疫苗只能模拟有同样抗原决定簇的病毒,如果因为突变导致这个结构不断变化,那么通过以前接种的疫苗产生的抗体或者记忆细胞将毫无用处。而且新疫苗开发周期长,无法应对目前的疫情。
目前无论从时间还是现有的研究进度看,最有希望的就是药物疗法了。针对药物开发,最好是药物能特异性识别病毒特有的结构,而对健康宿主细胞中的正常蛋白不要产生影响。但是在不影响大局的情况下,也可以对“自己人”下手,用药物削弱与病毒勾勾搭搭的自身蛋白,达到抑制病毒扩增的目的。目前已知的冠状病毒在入侵的7个步骤中都有相应的细胞作为内应为其服务,下面的表格就总结了武汉新冠状病毒爆发前所有能感染人的冠状病毒入侵宿主时宿主内的“内奸”蛋白,其中红框标注的是和强致病病毒相关的宿主蛋白。
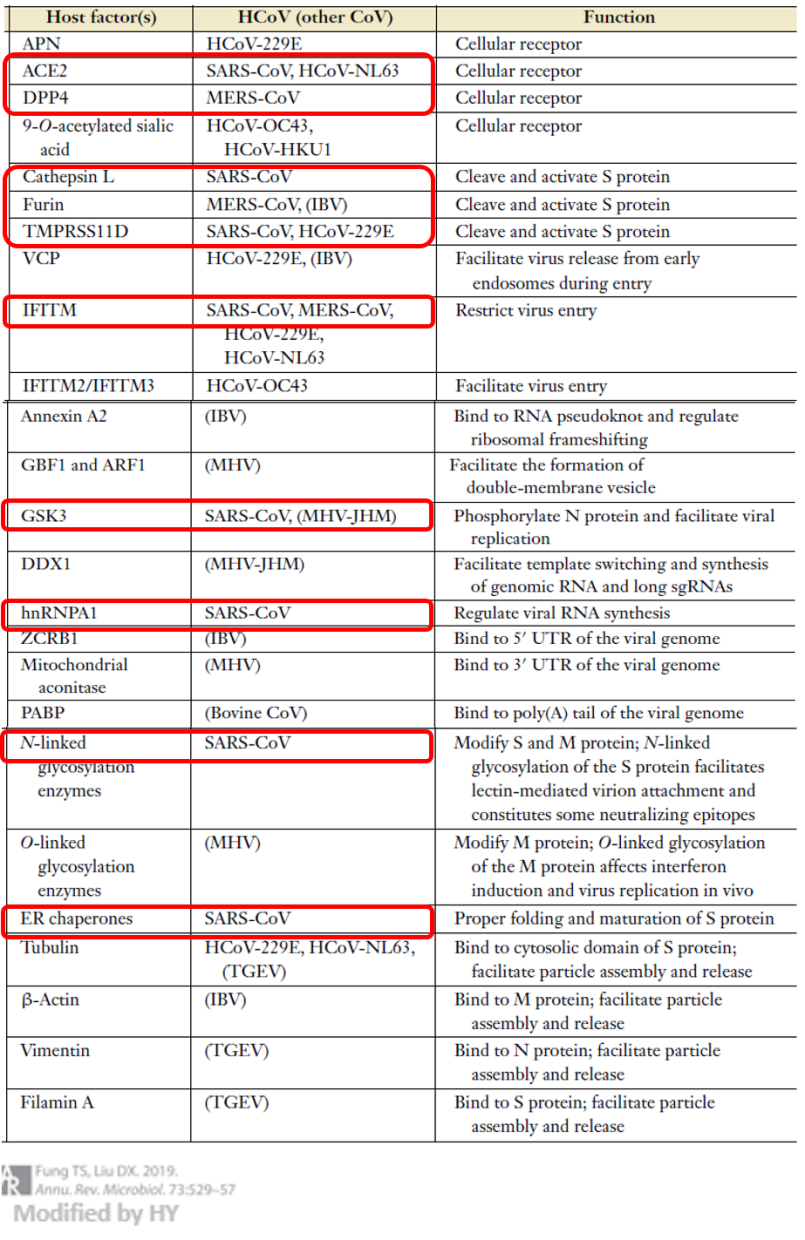
图6. 冠状病毒入侵相关宿主蛋白
(引用自Fung & Liu 2019)
在这些宿主蛋白中,与新冠状病毒相关的受体ACE2同时也是SARS病毒的受体,DPP4则介导MERS的侵入;Cathepsin L、Furin和TMPRSS11D负责切割S蛋白,帮助病毒进入细胞膜;GSK3在复制过程中对核蛋白磷酸化并协助病毒复制,hnRNPA1也在病毒RNA的合成过程中发挥作用;NL-GE对翻译好的病毒刺突蛋白和膜蛋白进行糖基化修饰;ER分子伴侣负责刺突蛋白的正确折叠。上述过程中的宿主蛋白可能是新冠状病毒药物研究的靶点。不过,在新冠状病毒的入侵机理弄清楚之前,其靶点只能参考亲缘关系较近的SARS病毒,不能完全生搬硬套SARS病毒的通路,而且这些蛋白本来也是人类正常生命活动所需,因而对于其感染的基础研究也是迫在眉睫。
在这些潜在的靶点中,宿主细胞表面受体又是尤其重要的。因为如果病毒分子一旦进入细胞,所需的药物也需要能够进入细胞才能发挥作用,这无疑加大了药物设计的难度,而且很多生物大分子药物(如抗体)是无法进入细胞的;细胞内病毒的活动主要就依靠宿主细胞提供的蛋白和能量,因此很多抑制剂类药物的副作用也很大。因此针对膜表面受体的药物研发,直接帮助细胞将病毒“御敌于国门之外”从逻辑上而言无疑是最佳方案。
目前的研究发现ACE2与2019-nCoV和SARS-CoV的感染有关,DPP4与MERS-CoV的感染有关。APN目前只发现与HCoV-229E冠状病毒的感染相关,但这种病毒不会导致严重病症,一般只造成轻微感冒症状。虽然与APN结合的人类冠状病毒目前不引起致死病症,但鉴于APN与MERS病毒受体DPP4一样有着较高的表达量(在肺组织中的蛋白表达量均高于ACE2),一旦被新病毒感染,可能引发和MERS一样的严重致死呼吸系统疾病。更要命的是,单链RNA的冠状病毒的刺突蛋白编码基因,又特别容易变异,很可能随时改变目标。因此,针对目前这三种受体的基础研究和药物研发无论是针对当下的疫情的控制还是对未来的不确定性的预防有重大的现实意义。
| 本次疫情给我们的警示,我们将如何应对当前以及“下一次”疫情? |
自然界大多数病毒都是相当专一的,一般只特异性地感染少数物种,同时很多病毒也不会导致宿主发生生命危险,但是如果不同物种间接有频繁接触,就有可能导致宿主之间的病毒遗传物质发生交换,产生对新宿主的适应性或者更加剧烈的感染性,对新的宿主产生不可预料的影响。
从这次灾难中,我们不但应当吸取教训,在没有安全保障的情况下远离野生动物,减少未知病毒入侵人体的可能。也应该加大医药研究投入,尤其是基础研究的投入,随时为奋战在一线的医疗人员提供有力的武器和充足的后勤技术保障。目前除了被动应对已经爆发的病毒疫情,我们也应该着眼于将来对病毒的预防。
现在随着深度学习和人工智能的快速发展,如果能够利用这些技术手段,加上现有研究积累的大量病毒基因组数据以及突变数据,对病毒序列加以分析,对病毒变异有可能产生的宿主迁移进行概率预测,并对其刺突蛋白等关键结构的三维构象进行精准构建,提前进行药物设计,那么就会使我们面对病毒时更加主动,料敌于先,把病毒对人类造成的伤害降到最低,甚至将病毒疫情的爆发扼杀在摇篮之中。
不论是疫苗研发还是新药研发以及基因治疗,均需要精准的动物模型来验证疾病的发病机制和免疫机制。赛业生物作为一家成熟的动物模型服务商,自疫情爆发以来便紧急召集公司的研发人员竭尽全力开发2019-nCoV研究相关的动物模型,为疫情防范献一份力量。
冠状病毒入侵人体细胞主要是靠与细胞膜受体结合,目前已经发现三种受体与冠状病毒感染人类细胞有关,即ACE2,DPP4和APN。其中ACE2与2019-nCoV和SARS-CoV的感染有关,DPP4与MERS-CoV的感染有关。APN目前只发现与HCoV-229E冠状病毒的感染相关,但这种病毒不会导致严重病症。虽然与APN结合的人类冠状病毒目前不引起致死病症,但鉴于APN与MERS病毒受体DPP4一样有着较高的表达量,一旦被病毒感染,容易引发和MERS一样的严重致死呼吸系统疾病,而冠状病毒用于与细胞表面受体结合的棘突蛋白编码基因又容易发生突变而改变目标受体,进入细胞复制,可能严重危及生命。因此,赛业生物专家团队第一时间开展三种冠状病毒关键受体基因修饰模型的开发工作,期望能为疫情防治贡献一份力量。
参考文献:
1. To Sing Fung and Ding Xiang Liu. Human Coronavirus: Host-Pathogen Interaction. Annual Review of Microbiology. Vol. 73, (2019).
2. Zhou, P. et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature https://doi.org/10.1038/s41586-020-2012-7, (2020).
3. Wu, F. et al. A new coronavirus associated with human respiratory disease in China. Nature https://doi. org/10.1038/s41586-020-2008-3, (2020).
4. Jie Cui et al. Origin and evolution of pathogenic coronaviiruses. Nature reviews. (2019).
5. Shibo Jiang et at. An emerging coronavirus causing pneumonia outbreak in Wuhan, China: calling for developing therapeutic and prophylactic strategies. Emerging microbes&infections. (2020).
6. Chan et at. A familial cluster of pneumoniaassociated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster,The Lancet, (2020).
|
