近期,华南农业大学国家兽医微生物耐药性风险评估实验室在微生物学国际主流学术期刊mBio在线发表了关于肺炎克雷伯菌质粒上发现的一种新型可介导替加环素等药物耐药的多重耐药外排泵基因簇(tmexCD1-toprJ1)的研究论文,该研究系统性地阐述了tmexCD1-toprJ1耐药基因簇的功能、起源以及流行情况。
|

|
近年来,质粒等可移动元件介导的耐药基因水平传播所致革兰阴性菌耐药性的快速发展,引起全球高度关注。黏菌素和替加环素是治疗多重耐药革兰氏阴性杆菌感染的少数有效药物,然而,质粒介导黏菌素耐药基因mcr-1的出现及其在全球的广泛传播,导致黏菌素的临床应用价值面临挑战,使替加环素成为治疗多重耐药肠杆菌所致严重感染的有限药物之一。目前,除了染色体上RND型外排泵过表达以及质粒编码的Tet(A)外排泵变异体和替加环素修饰酶Tet(X3)、Tet(X4)和Tet(X5)介导的替加环素耐药机制外,尚未发现可水平转移的RND型外排泵与替加环素耐药性相关的报道。
2017年,课题组分离到鸡源泛耐药肺炎克雷伯菌,同时对替加环素耐药,通过全基因组测序,发现细菌同时携带碳青霉烯耐药基因(blaNDM-1)、黏菌素耐药基因(mcr-1、mcr-8)等30个耐药基因,未检测到已知的替加环素耐药机制,但发现携带一个质粒编码的RND型外排泵基因簇,该基因簇与铜绿假单胞菌染色体上的mexCD-oprJ基因簇有78%的核苷酸序列同源性,同时位于质粒上具有可转移能力,将其命名为tmexCD1-toprJ1(t表示transferable),并推测该基因簇可能与替加环素耐药有关。通过克隆和接合实验,确证tmexCD1-toprJ1可介导肺炎克雷伯菌、大肠杆菌和沙门氏菌对甘氨酰环素类(替加环素)、四环素类、喹诺酮类、头孢菌素类和氨基糖苷类等多种药物耐药(MIC值增加4~32倍),这意味着tmexCD1-toprJ1也是一种新的质粒介导的喹诺酮耐药基因(PMQR)。
为了证实TMexCD1-TOprJ1的外排泵功能,课题组进一步通过细菌药物蓄积实验,发现携带有外排泵的宿主菌的药物蓄积浓度明显低于对照菌株,并对外排泵抑制剂N-甲基吡咯烷酮(NMP)表现出更为显著的反应。此外,小鼠感染模型的替加环素治疗实验结果显示,接种tmexCD1-toprJ1阳性肺炎克雷伯菌的小鼠死亡率更高,提示其可能会导致临床治疗失败。
|
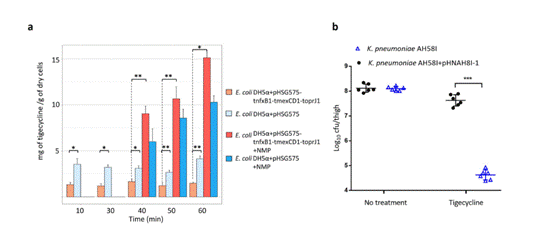
图1TMexCD1-TOprJ1对替加环素体内体外活性研究
本研究进一步分析了tmexCD1-toprJ1的基因环境和质粒结构,发现tmexCD1-toprJ1位于可接合的IncFIA型质粒(pHNAH8I-1)上,同时该质粒上还携带黏菌素耐药基因(mcr-8)。之后通过分析这种新型外排泵基因簇的基因环境,发现在外排泵上游存在位点特异性整合酶基因,与tnfxB1-tmexC1-tmexD1-toprJ1基因簇一同插入在转座子Tn5393的转座酶tnpA基因中。在Genbank数据库中搜索相应高相似度的序列进行比对分析后,推测外排泵基因簇可能通过假定整合酶,从染色体捕获上并转移到质粒上传播。之后,课题组通过构建遗传进化树方法,发现假单胞菌染色体上存在同源性最为接近的外排泵基因簇,因此推定tmexCD1-toprJ1可能来源于某种假单胞菌染色体。
|
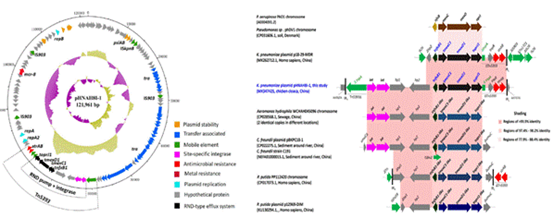
图2 pHNAH8I-1质粒结构和tmexCD1-toprJ1基因环境比较图
|
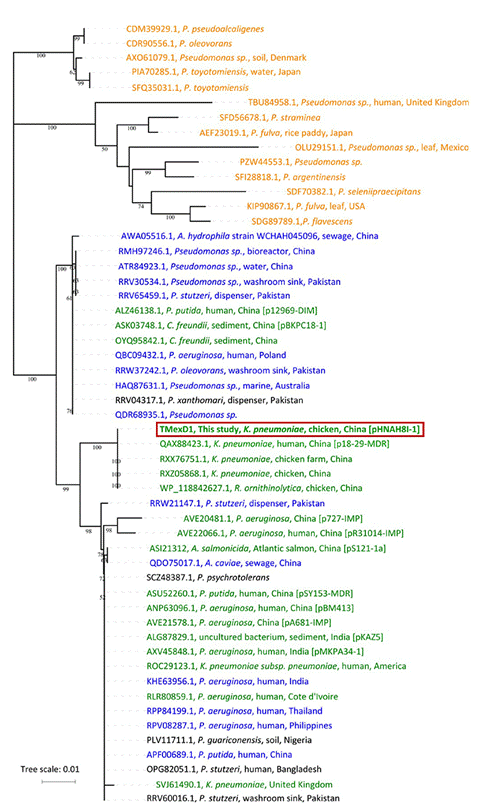
图3 TMexD1及相关高同源性蛋白遗传进化树
|
|
课题组随后进行流行病学调查,发现tmexCD1-toprJ1主要在国内多个地区养鸡场中广泛传播,并已扩散至动物性食品和人,主要在肺炎克雷伯菌及其相近菌属中流行。尽管tmexCD1-toprJ1在人源肠杆菌中检出率较低,但考虑到tmexCD1-toprJ1的可转移性和外排泵底物的广泛性,tmexCD1-toprJ1可能会进一步传播,对食品安全和人类健康构成潜在威胁。
|
|
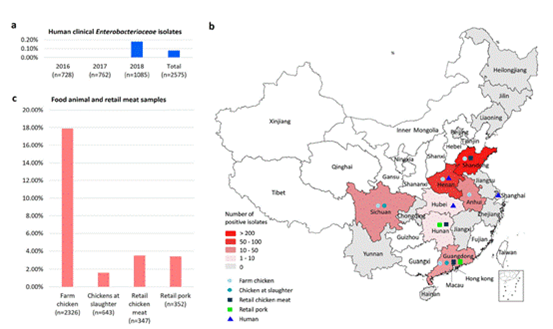
图4携带tmexCD1-toprJ1阳性菌株流行分布情况
|
|
本研究首次报道了一种新型的质粒介导的多重耐药RND家族外排泵,此外排泵可导致包括替加环素在内的多种临床常用药物耐药。因此,应加强相应的流行病学监测,以控制携带TMexCD1-TOprJ1外排泵菌株的进一步传播。
|
相关成果:
|
饿死肿瘤,养活细胞:Nature子刊发现克服耐药性的新方法
Nature出乎意料新发现:没有用抗生素也会出现耐药性
Mayo:噬菌体疗法对付耐药性细菌感染治疗人工关节感染初显潜力
合成生物学家解谜“癌症之王”的耐药性
|
