基因治疗是指将外源正常基因导入靶细胞,以纠正或补偿缺陷和异常基因引起的疾病,从而达到治疗目的。
腺病毒相关病毒(Adenovirus Associated Virus,AAV) 作为一种安全有效的载体,全球有数十个临床试验在进行。
临床研究项目中AAV1和AAV2约占50%
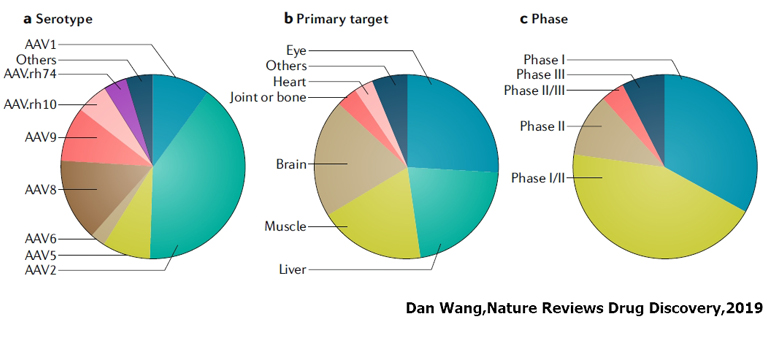
--质量控制--
--Wes全自动定量Western Blot
在AAV生产过程中,使用SDS-PAGE通过Western Blot来鉴定蛋白。然而,传统的Western Blot手动操作繁琐,重复性差,并且仅是半定量,不宜用于工业产品质量控制。Wes全自动定量western以其独特优势逐渐替换传统western blot,可用于新型AAV衣壳的表达到下游制造全程质量控制中。
鉴定衣壳蛋白VP1/2/3
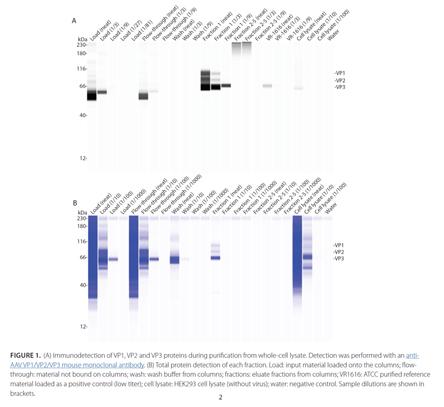
鉴定杂质

筛选抗体
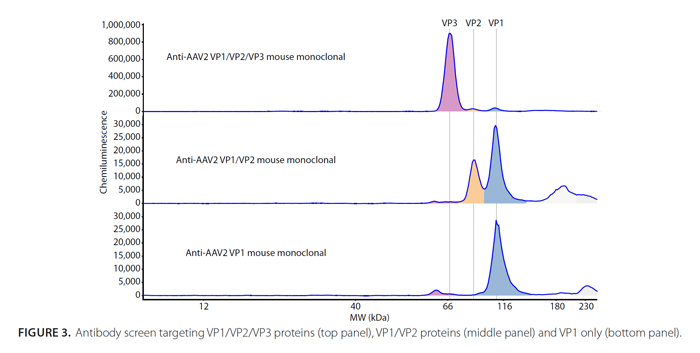
检测动态范围
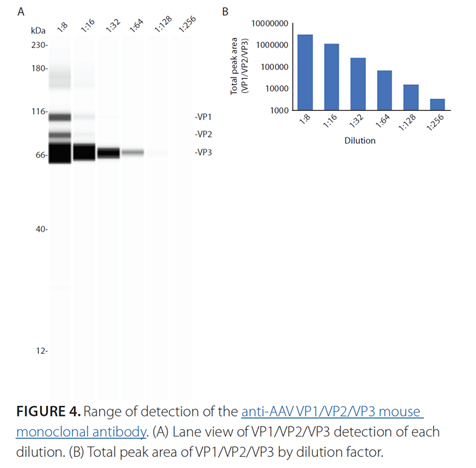
--Maurice表征AAV电荷异质性
与所有治疗药物一样,基因疗法,需要表征包装药物的递送载体电荷等。使用全柱成像毛细管等电聚焦电泳法(icIEF)来表征AAV的电荷异质性,可以确保产品的稳定性和一致性。
Maurice兼具CE-SDS和iCIEF双功能。两种功能均入选国家药典。
AAV病毒电荷表征
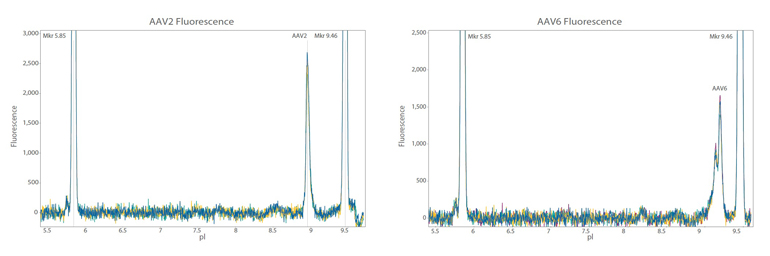
AAV2和AAV6电荷表征,Maurice独有的自发荧光检测器,可以提高电荷变异体检测灵敏度3-5倍。
AAV病毒变性电荷表征
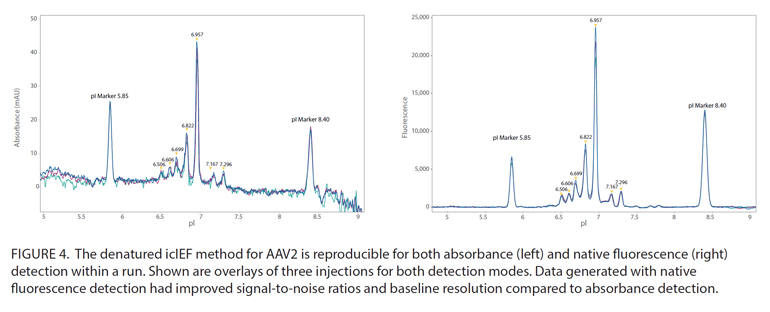
AAV病毒蛋白会进行几种翻译后修饰,包括糖基化和脱酰胺作用。应激引起的病毒蛋白脱酰胺作用可能导致载体活性,衣壳装配和转导效率降低1。icIEF方法通常用于监测由唾液酸化,糖基化和脱酰胺作用诱导的单克隆抗体的电荷异质性,因此对AAV病毒蛋白也进行类似的评估。
AAV病毒稳定性
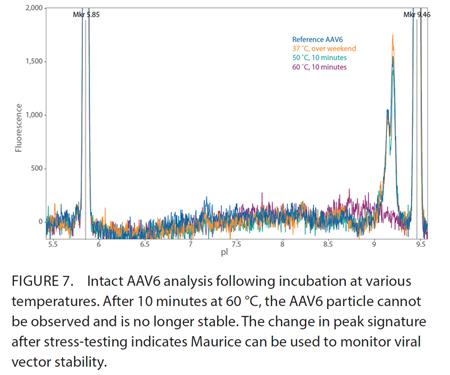 |
对完整的AAV样品进行温度压力测试,以确定是否可以使用Maurice监测病毒载体的稳定性或衣壳蛋白脱酰胺。AAV6颗粒非常稳定,在37°C或50°C下保持10分钟完整无缺。但是,当AAV6颗粒在60°C下10分钟时,不稳定。 |
AAV病毒批间一致性
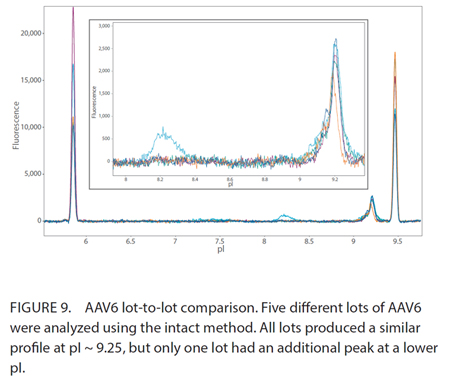 |
利用Maurice icIEF自发荧光监测批次间变异,以鉴别病毒载体批间差别。五批不同的AAV6,使用 Maurice icIEF自发荧光分析。结果显示,所有五个批次在pI〜9.25左右均产生相似的峰形。但是,在一批中观察到了一个较低pI的附加峰,表明该样品与其他四批样品不同。 |
Wes/Jess全自动定量Western Blot系统
- 全程自动化
- 数字定量Western Blot
- 符合FDA 21 CFR Part11
- 覆盖2-440KD
- 只需3μl样本
- 3小时完成检测
- 4-5log线性区间
|
 |
| |
|
Maurice双功能毛细管电泳系统
- iCIEF CE-SDS双功能
- 效率为传统方法5倍
- 灵敏度为传统方法5倍
- 免组装毛细管卡盒
- 方法入选国家药典
|
 |
 |












