
-

生物通官微
陪你抓住生命科技
跳动的脉搏
靶向源头根治tau去磷酸化嵌合体的产生
【字体: 大 中 小 】 时间:2024年04月01日 来源:Science Bulletin
编辑推荐:
Tau过磷酸化蛋白在神经退行性变中起关键作用。Su等人构建了一种名为de磷酸化靶向嵌合体(DEPTAC)的新策略,通过劫持tau蛋白的磷酸酶来实现tau蛋白的特异性去磷酸化。他们展示了每个组成基序的逐步优化,并产生了新的DEPTAC,有效地促进了病理性tau的去磷酸化和随后的清除。
在阿尔茨海默病(AD)和其他许多tau蛋白病变中,tau蛋白的异常过度磷酸化和积累在神经退行性过程中起着关键作用。病理性tau蛋白的积累在阿尔茨海默病(AD)和许多其他tau病的神经变性中起关键作用。因此,改善脑内病理性tau聚集是药物开发的重要方向。然而,由于tau蛋白本身在维持细胞结构和功能方面起着多方面的生理作用,因此针对tau蛋白一般形式的传统策略可能有些武断。
由于tau的病理性过度磷酸化引发了tau病变中神经原纤维缠结和神经变性的形成,因此特异性下调tau磷酸化可能会更精细地用于这些疾病的治疗。然而,直接使用tau激酶抑制剂或磷酸酶激活剂会产生不可接受的毒副作用,因为这些酶中的每一种都同时调节除tau蛋白外的许多信号通路。
因此,选择性地消除过度磷酸化的tau蛋白为这些疾病的治疗提供了希望。
Jian-Zhi Wang教授(华中科技大学同济医学院病理生理教研室)、Jie Zheng教授(北京大学基础医学院神经生物学教研室)、Xiaochuan Wang教授(华中科技大学同济医学院病理生理教研室)牵头提出了一种策略,称为去磷酸化靶向嵌合体(DEPTACs),该策略旨在特异性地劫持磷酸酶与tau蛋白结合,以削弱其过度磷酸化的状态。
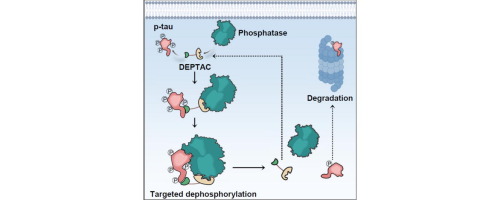
为了实现tau的特异性去磷酸化,Wang和她的团队概念化了一种策略,即去磷酸化靶向嵌合体(DEPTAC),它能够特异性地劫持tau的磷酸酶以削弱其过度磷酸化(图1)。DEPTAC由以下基序组成:(1)专门识别和结合tau的“弹头”(2)招募磷酸酶的“锚”(3)基序间连接体(4)必要时穿透细胞膜的序列。
首先,他们对每个组成基序进行逐步优化以生成新的DEPTAC,该DEPTACs在促进病理性tau的去磷酸化和随后的清除方面显示出合理的功效。
随后,他们对选定的嵌合体之一D16进行了进一步的探索。他们发现D16在体外对神经毒性K18-tau种子引起的神经退行性变有显著的疗效。此外,静脉注射D16还能减轻AD小鼠脑内的tau病理,改善记忆缺陷。
这些结果表明,DEPTACs是tau过度磷酸化的靶向调节剂,具有治疗AD和其他tau病的潜力。DEPTACs的设计和优化基于对tau蛋白病理学的深入理解,以及对磷酸酶活性和功能的精确调控。通过这种方法,开发出一种新的治疗策略,它不仅能够针对特定的病理过程,还能够减少对正常细胞功能的潜在影响。D16的成功应用展示了DEPTACs在疾病模型中的治疗潜力,为未来的临床研究和药物开发提供了新的方向。
此外,这项研究还强调了跨学科合作的重要性,结合了分子生物学、神经科学和药物化学等领域的专业知识。通过这种合作,研究人员能够开发出创新的治疗方法,为目前尚无有效治疗手段的疾病提供了新的希望。随着进一步的研究和开发,DEPTACs可能成为治疗阿尔茨海默病和其他tau蛋白病变的有效药物,改善患者的生活质量,并减轻全球健康负担。
Generation of tau dephosphorylation-targeting chimeras for the treatment of Alzheimer’s disease and related tauopathies