
-

生物通官微
陪你抓住生命科技
跳动的脉搏
前列腺癌FFPE组织DNA甲基化EPIC芯片检测的质量控制关键点研究
【字体: 大 中 小 】 时间:2025年07月10日 来源:BMC Research Notes 2.8
编辑推荐:
本研究针对福尔马林固定石蜡包埋(FFPE)前列腺癌组织DNA甲基化检测中质量控制难题,创新性引入第三重质控环节(bisulfite conversion quality check),成功实现255例样本99.6%的EPIC芯片数据合格率。研究证实当FFPE样本DNA质量(Qubit定量)和完整性(Infinium HD FFPE qPCR)达标时,第三重质控价值有限,为临床表观遗传学研究提供了标准化流程参考。
在表观遗传学领域,DNA甲基化作为关键调控机制,与癌症发生发展密切相关。然而利用临床常见的福尔马林固定石蜡包埋(FFPE)组织进行全基因组甲基化分析却面临巨大挑战――这类样本存在DNA降解严重、转化效率不稳定等问题。尤其当使用Illumina MethylationEPIC v1.0芯片(覆盖>850,000个CpG位点)时,传统仅含两重质控(DNA定量与质量评估)的流程可能导致样本浪费和成本增加。
针对这一技术瓶颈,来自澳大利亚的研究团队(通讯作者Melissa C. Southey隶属Cancer Council Victoria等机构)在《BMC Research Notes》发表重要研究。他们借鉴乳腺癌研究经验,首次在前列腺癌FFPE样本中系统评估三重质控体系的价值。研究对象来自Lifestyle and Genetic Risk Factors for Prostate Cancer Study(LGRFPCS)队列的255例前列腺肿瘤样本,通过引入第三重bisulfite转化效率检测(靶向BRCA1基因134bp区域),构建了完整的质控链条。
关键技术包括:1)采用QIAamp DNA FFPE试剂盒进行组织宏切割DNA提取;2)通过Qubit? dsDNA BR Assay(QC1)和Infinium HD FFPE qPCR(QC2)完成前两阶段质控;3)创新性应用BRCA1靶向qPCR(QC3)评估bisulfite转化效率;4)使用MethylationEPIC v1.0芯片检测并通过ENmix管道进行数据标准化。
QC checkpoints
所有样本在QC1阶段均达到近500ng DNA标准(仅2例483/486ng),QC2阶段ΔCt值全部≤6周期,QC3阶段ΔCt均≥4周期,显示样本具有优异的初始质量。
Sample analysis
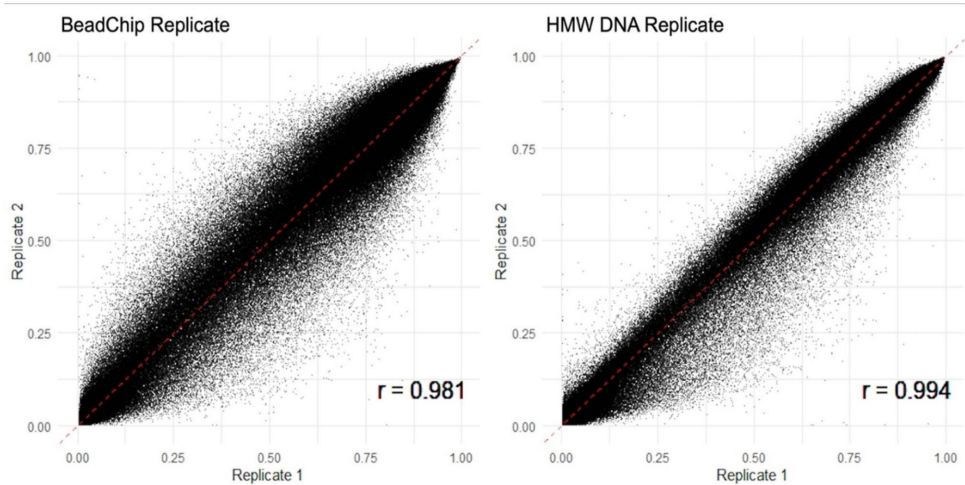
芯片数据质量验证显示:
讨论与意义
该研究首次证实:对于质量稳定的FFPE前列腺癌样本(统一病理中心处理、存储8-13年),标准化的DNA提取流程配合前两重质控已可确保99.6%的EPIC芯片成功率。这为大规模临床表观遗传学研究提供了重要启示:
研究同时揭示了FFPE样本甲基化分析的潜在局限:单个样本的芯片失败可能无法通过现有质控预测,建议在预算允许时增加技术重复。该质控体系的应用将显著提升表观基因组研究的成本效益,尤其对前列腺癌等依赖FFPE样本的肿瘤研究具有重要推广价值。
 生物通微信公众号
生物通微信公众号
知名企业招聘