
-

生物通官微
陪你抓住生命科技
跳动的脉搏
磷脂聚合物偶联物实现抗原蛋白直接胞质递送的新策略及其在免疫调控中的应用
【字体: 大 中 小 】 时间:2025年08月02日 来源:Polymer Journal 2.7
编辑推荐:
本研究针对蛋白质药物难以穿透细胞膜的关键难题,开发了基于2-甲基丙烯酰氧乙基磷酰胆碱(MPC)和甲基丙烯酸正丁酯(BMA)的磷脂模拟聚合物PMBS-OVA偶联系统。通过调控聚合物与卵清蛋白(OVA)的配比,成功实现了在4℃抑制内吞途径条件下仍能完成抗原蛋白的胞质递送,显著增强了主要组织相容性复合体I类(MHC I)的抗原呈递效率,为疫苗开发和免疫治疗提供了新思路。
在生物医药领域,蛋白质类药物如抗体、疫苗抗原和酶制剂等已成为治疗疾病的重要武器。然而这些"生物导弹"面临着一个根本性障碍――它们无法自主穿越细胞膜这道天然屏障。更棘手的是,进入细胞后这些蛋白质往往被困在内吞体中,最终被溶酶体降解。虽然科学家们尝试了各种方法帮助蛋白质"越狱",包括利用细胞穿透肽(CPPs)和pH敏感材料等,但要么效率低下(CPPs的胞质递送效率仅约7%),要么会引发不必要的免疫反应。
日本东北大学的研究人员另辟蹊径,从细胞膜的主要成分――磷脂分子中获得灵感。他们设计了一种仿生聚合物PMBS,其核心成分2-甲基丙烯酰氧乙基磷酰胆碱(MPC)与细胞膜磷脂结构相似,具有优异的生物相容性。通过将这种聚合物与模型抗原卵清蛋白(OVA)偶联,研究人员构建了能直接穿透细胞膜的"蛋白质特洛伊木马"。这项发表在《Polymer Journal》的研究表明,当聚合物与蛋白质的配比达到100:1时,形成的PMBS100-OVA1复合物能在4℃低温(完全抑制内吞作用的条件下)将45kDa的大分子蛋白质递送至树突状细胞胞质,并显著提升MHC I类分子对OVA衍生肽SIINFEKL的呈递效率,而不会刺激炎症因子IL-6和IL-10的产生。
研究采用了三项关键技术:1)通过自由基聚合法合成含活性酯的磷脂聚合物PMBS;2)建立不同配比(1:1、10:1、100:1)的聚合物-蛋白质偶联体系;3)结合流式细胞术和共聚焦显微镜,在生理条件(37℃)和内吞抑制条件(4℃)下系统评估递送效率。特别值得注意的是,实验使用DC2.4小鼠树突状细胞系作为模型,通过检测MHC I-SIINFEKL复合物阳性细胞比例量化抗原呈递效果。

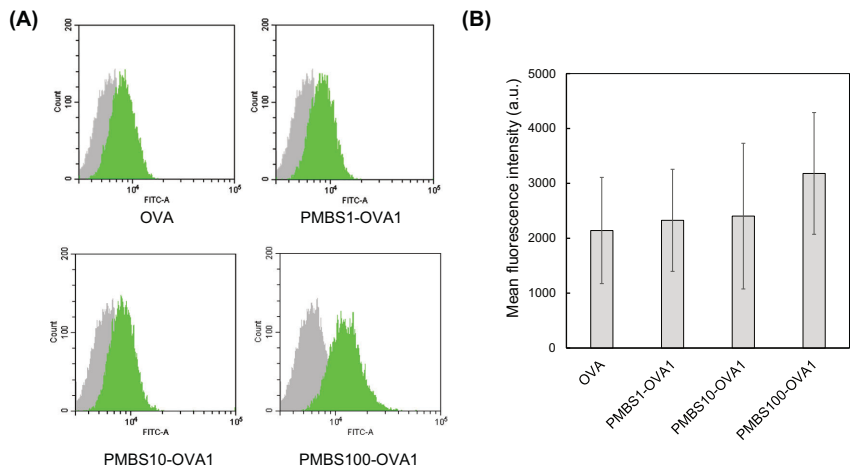
研究结果揭示三个重要发现:首先,ANS-Na荧光探针实验证实所有配比的偶联物均能形成含疏水结构域的多分子聚集体(最大荧光波长蓝移至485nm),其中PMBS100-OVA1的水合直径达200nm(表3)。其次,4℃条件下的流式细胞检测显示,仅PMBS100-OVA1能高效进入细胞(图4),其荧光强度显著高于其他组,共聚焦图像显示OVA广泛分布于胞质并与溶酶体部分共定位(图5)。最后,在37℃正常培养条件下,所有偶联物均可被内吞,但仅PMBS100-OVA1能显著提升MHC I-SIINFEKL阳性细胞比例至SIINFEKL肽处理组的相当水平(图8),且不引起IL-6/IL-10分泌变化(图7)。
这项研究的意义在于:1)首次实现大分子蛋白质(45kDa)的直接胞质递送,突破了传统内吞-逃逸路线的限制;2)创建的PMBS平台具有"隐形"特性,不会激活树突状细胞的炎症反应,这对需要免疫耐受的治疗(如自身免疫疾病)尤为重要;3)通过简单调节聚合物/蛋白质比例即可控制递送途径(内吞或直接穿透),为精准免疫调控提供新工具。Yuta Yoshizaki和Tomohiro Konno团队的工作不仅为蛋白质药物递送开辟了新途径,其设计的磷脂聚合物平台还可拓展应用于疏水性免疫调节剂(如雷帕霉素)的共递送,未来在肿瘤疫苗和自身免疫病治疗领域具有广阔前景。
 生物通微信公众号
生物通微信公众号
知名企业招聘