
-

生物通官微
陪你抓住生命科技
跳动的脉搏
为什么成年人的心脏不能再生
【字体: 大 中 小 】 时间:2022年10月25日 来源:Developmental Cell
编辑推荐:
该研究表明,心脏细胞与周围环境之间的通信中断可以保护该器官免受与压力相关的有害信号(如高血压),但代价是阻止心脏细胞接收促进再生的信号。这项研究发表在今天(10月24日)的《Developmental Cell》杂志上。
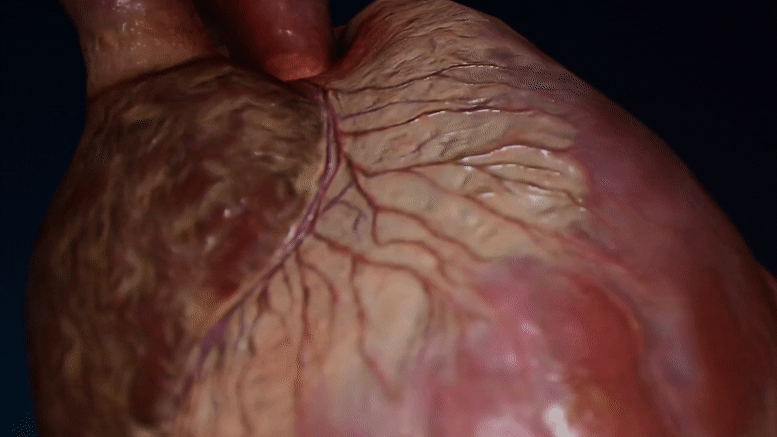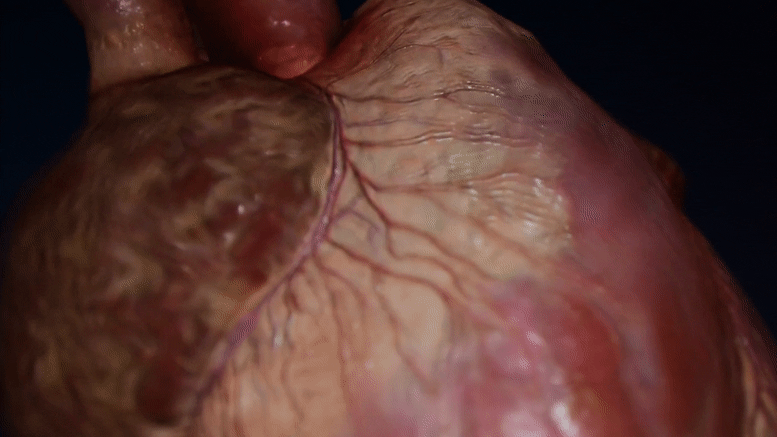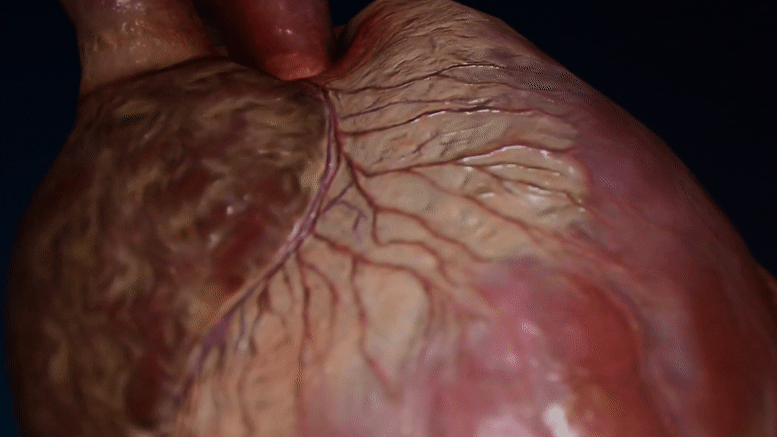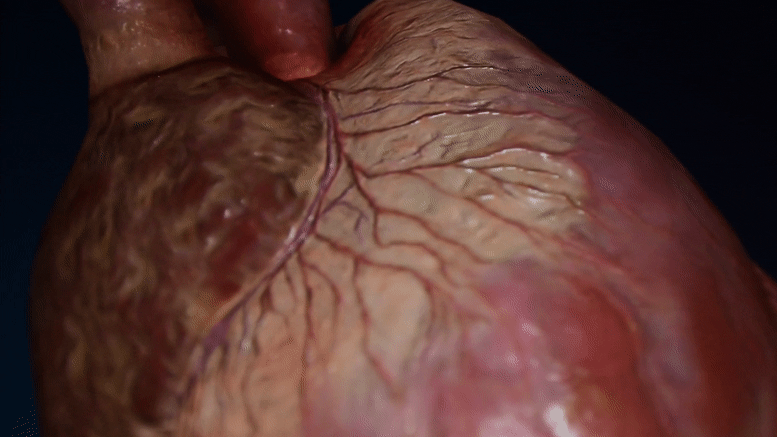
胎儿(左)和婴儿(右)啮齿动物心脏细胞核的电子显微镜图像。随着心脏细胞的发育,核孔的数量减少。(Credit: Han et al., 2022, Developmental Cell, 10.1016/j.devcel.2022.09.017)
一项新的研究表明,使心脏细胞与其环境之间的通信安静下来可以保护心脏免受与压力相关的有害信号的影响,如高血压,但代价是阻止心脏细胞接收促进再生的信号。
随着小鼠心脏细胞的成熟,称为核孔的交流途径数量急剧减少。尽管这可能会保护器官免受破坏性信号的伤害,但也可能会阻止成年心脏细胞的再生。这是根据匹兹堡大学和匹兹堡大学医学院(UPMC)的科学家进行的新研究得出的结论。
该研究表明,心脏细胞与周围环境之间的通信中断可以保护该器官免受与压力相关的有害信号(如高血压),但代价是阻止心脏细胞接收促进再生的信号。这项研究发表在今天(10月24日)的《Developmental Cell》杂志上。
“这篇论文解释了为什么成年心脏不能自我再生,但新生小鼠和人类的心脏可以,”资深作者Bernhard Kühn,医学博士说,“这些发现是一个重要的进步,在基本理解心脏如何随着年龄的增长而发展,以及它如何进化来应对压力。”Kühn是皮特医学院和匹兹堡UPMC儿童医院的儿科教授和心脏再生和治疗儿科研究所主任。
虽然皮肤和人体的许多其他组织在受伤后仍能保持自我修复的能力,但心脏却不是这样。在人类胚胎和胎儿发育过程中,心脏细胞经过细胞分裂形成心肌。但当心脏细胞在成年后成熟时,它们会进入一种无法再分裂的终末状态。
为了进一步了解心脏细胞如何以及为什么会随着年龄的增长而发生变化,Kühn与皮特大学的研究人员和生物医学成像专家Yang Liu博士(医学和生物工程副教授)、Donna Stolz博士(细胞生物学和病理学副教授、生物成像中心副主任)合作,对核孔进行了观察。这些围绕细胞DNA的脂膜上的穿孔调节着分子进出细胞核的通道。
“核膜是一层不渗透的保护层,保护细胞核,就像高速公路上的沥青,”Kühn说,他也是麦高恩再生医学研究所的成员。“就像沥青上的人孔一样,核孔是信息通过屏障进入细胞核的通道。”
Liu使用超分辨率显微镜观察并统计了小鼠心脏细胞或心肌细胞的核孔数量。在整个发育过程中,孔的数量减少了63%,从胎儿细胞的平均1856个到婴儿细胞的1040个,再到成人细胞的仅678个。Stolz证实了这些发现,他使用电子显微镜显示核孔密度在心脏细胞发育过程中下降。
在之前的研究中,Kühn和他的团队证明了一种名为Lamin b2的基因对心肌细胞再生很重要,这种基因在新生小鼠中表达量很高,但随着年龄的增长而下降。
在新的研究中,他们发现阻断小鼠的Lamin b2表达会导致核孔数量的减少。核孔较少的小鼠向细胞核的信号蛋白运输减少,基因表达减少,这表明随着年龄的增长交流减少可能导致心肌细胞再生能力的下降。
Kühn解释说:“这些发现表明,核孔的数量控制着进入细胞核的信息通量。随着心脏细胞的成熟和核孔的减少,到达细胞核的信息越来越少。”
在应对高血压等压力时,心肌细胞的细胞核会接收到修改基因通路的信号,从而导致心脏的结构重构。这种重构是心力衰竭的主要原因。
研究人员使用高血压小鼠模型来了解核孔是如何促进这种重塑过程的。被改造成表达更少核孔的小鼠显示出参与有害心脏重塑的基因通路的调节更少。这些小鼠的心脏功能和存活率也比核孔更多的小鼠好。
Kühn说:“我们对高血压小鼠核孔减少的保护作用的程度感到惊讶。然而,较少的交流途径也限制了那些促进再生的有益信号。”
参考文献: Changes in nuclear pore numbers control nuclear import and stress response of mouse hearts” by Lu Han, Jocelyn D. Mich-Basso, Yao Li, Niyatie Ammanamanchi, Jianquan Xu, Anita P. Bargaje, Honghai Liu, Liwen Wu, Jong-Hyeon Jeong, Jonathan Franks, Donna B. Stolz, Yijen L. Wu, Dhivyaa Rajasundaram, Yang Liu and Bernhard Kühn, 24 October 2022, Developmental Cell.