
-

生物通官微
陪你抓住生命科技
跳动的脉搏
精彩!改造针对癌细胞"谷氨酰胺成瘾"的前体药,让健康细胞不受伤害
【字体: 大 中 小 】 时间:2022年11月18日 来源:Johns Hopkins Medicine
编辑推荐:
研究人员通过设计将一种能有效“饿死”癌细胞但同样伤害健康胃肠组织的“弃药”改造成为能更好靶向癌细胞、使健康组织不受伤害的新药。关键的是,这种改造思路很值得借鉴。
背景
肿瘤细胞的快速生长需要大量的能量、大量的底物以供合成蛋白质和核酸。由于谷氨酰胺能通过三羧酸 (TCA) 循环充当能量来源,并提供碳和氮作为氨基酸、脂质和核苷酸合成以及维持氧化还原平衡的前体,具有重要作用,肿瘤细胞的谷氨酰胺消耗率比正常组织要高,因此全面阻断谷氨酰胺在癌细胞中的利用,具有很大的治疗潜力。
6-Diazo-5-oxo- l - norleucine (DON) 与谷氨酰胺具有高度结构相似性,不仅能选择性地阻断多个使用谷氨酰胺的反应,导致肿瘤细胞饥饿,同时还能增强 T 细胞在肿瘤微环境中的细胞毒性作用,在使用 DON 的首批临床研究之一中,接受 2 周或更长时间 DON 治疗的 47 名患者中有 31 名 (66%) 表现出病情稳定或消退,显示出良好的疗效。可惜的是 DON 这样的广泛代谢抑制剂在高度依赖谷氨酰胺的健康胃肠 (GI)组织中表现出毒性,DON 的临床开发由于其对正常组织特别是胃肠组织的剂量限制性毒性而被放弃(例如,粘膜炎、腹泻和胃出血)。
前体药(prodrug)指药物经过化学修饰、得到体外无活性或活性较小、在体内经酶解或非酶转化释放出活性药物而发挥药效的化合物。
研究亮点
约翰霍普金斯大学医学院的研究人员通过巧妙设计改进了DON这种抗癌药物,使之能更好地靶向癌细胞,而不伤害健康组织。他们的实验报告发表在11月16日的《科学进展》杂志上。
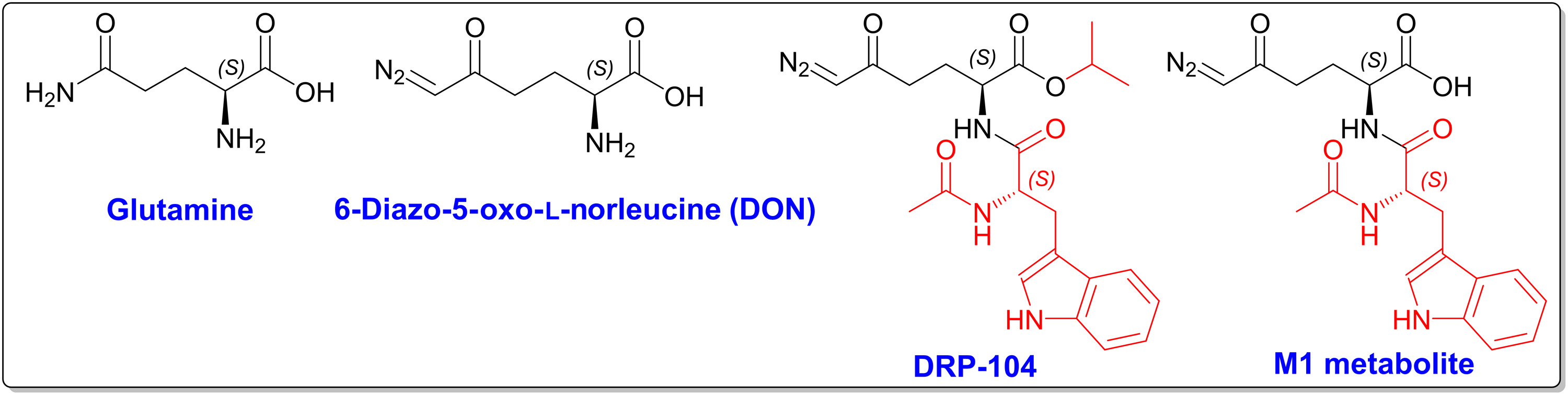
研究人员用一种离散的化学方法来设计 DON 的肿瘤靶向前体药物――DRP-104,使用了两个可以被肿瘤中富含的酶(但胃肠组织不含的酶)切割的“前体基团”――在胺基上添加乙酰化色氨酸,在 DON 羧酸上添加异丙酯。DRP-104 对谷氨酰胺的酶(包括 GLS-1)是无活性的,DRP-104 的去酯化代谢物 M1也没有活性(见下图)。
虽然 DRP-104 在野生型 WT C57BL/6 小鼠血浆中完全不稳定(60 分钟时剩余 0%),但它在 C57BL/6/CES1 -/-小鼠和人血浆中表现出良好的稳定性( 60 分钟时剩余>90% )。值得注意的是,这种种间代谢差异在前体药开发中并不少见。众所周知,羧酸酯酶 1 (CES1) 在啮齿动物血浆中非常丰富,但在高等物种特别是人类血浆中不存在。C57BL/6/CES1 -/-小鼠是通过使 CES1 基因失活而产生的,其血浆中的 CES 活性无法检测到,但组织中的活性正常,使这些小鼠成为模拟人类新陈代谢的更好的临床前模型。在小鼠肠组织匀浆和人小肠S9组织中评估DRP-104稳定性,结果表明在两种肠道基质中,DRP-104 在60分钟内被完全水解为带电且无活性的中间代谢物 M1,DON 释放量小于 10%。
C57BL/6/CES1-/-荷瘤小鼠模型中给予DRP-104 的实验表明,小鼠体内肿瘤中DRP-104被活化为具有抗肿瘤活性的DON,DON的剂量分别比血浆中高 6 倍、比胃肠组织中高11 倍,表现为让肿瘤完全消退而没有胃肠副作用。DRP-104 还能够增强抗 PD-1 免疫疗法的疗效,其作用是 CD8+ T 细胞依赖性的。最值得注意的是,用 DRP-104 单一疗法治愈的小鼠能够完全抵抗肿瘤再次攻击,表明谷氨酰胺拮抗疗法触发了免疫记忆。基于这些有希望的临床前数据,DRP-104 目前正在进行临床试验 (NCT04471415),用于作为单一药物和与免疫疗法联合治疗晚期实体瘤。
“我们的目标是改造一种原有的抗癌药物DON――它显示出强大的疗效但毒性太大,特别是对肠道而言,无法进行临床开发。为此,我们使用了前体药物方法。我们的方法的独特之处在于,我们利用一种新颖的化学设计来创造一种前体药,它在癌细胞中同时被生物激活,但在健康组织(如肠道)中被生物灭活。该研究的作者Barbara Slusher博士说,她是约翰霍普金斯大学医学院的神经学、药理学和分子科学、精神病学、神经科学、医学和肿瘤学教授,也是约翰霍普金斯大学药物发现项目的主任,理学硕士。
这种新修饰的前体药利用了癌细胞的一种共同特性:对谷氨酰胺的旺盛胃口――快速生长的癌细胞使用大量的谷氨酰胺,这种现象被称为“谷氨酰胺成瘾”,但其他快速周转的健康细胞,如肠道内的细胞,也依赖谷氨酰胺。
合著者、神经学和药理学副教授Rana Rais博士说:“DRP-104是谷氨酰胺模拟药物DON (6- diazo -5- oxo - l - nor亮氨酸)的肿瘤靶向前体药,它可以抑制癌细胞中多种利用谷氨酰胺的酶。”Slusher、Rais和他们的团队对DON进行的化学修饰使得这个有前途的药物的开发得以恢复。
“我们在DON中加入了一种叫做促进基团(promoieties)的化学基团,使DON失去活性,直到它到达肿瘤,在那里促进基团被肿瘤中丰富但肠道中没有的酶剪切掉,”Slusher是约翰霍普金斯大学基梅尔癌症中心及癌症免疫治疗研究所的成员。“这种特殊的前体药设计使DON靶向于预期的目的地――肿瘤,对其他地方的健康细胞影响较小。”
在这项新研究中,研究人员将原始的DON药物和增强的DRP-104药物注射到植入肿瘤的小鼠体内。在接受DRP-104治疗的小鼠中,研究人员发现肿瘤中的药物活性是胃肠道(肠道)的11倍。两种药物都完全消灭了肿瘤,但DON对小鼠的肠道毒性大于DRP-104。
Slusher和研究的合著者Rana Rais, Pavel Majer和Jonathan Powell共同创立了一家生物技术公司Dracen制药公司,该公司授权这种新的前体药物进行临床开发。DRP-104正在美国各地进行I/II期临床试验,包括约翰霍普金斯大学吉米尔癌症中心,用于晚期实体瘤患者。Slusher说,她的约翰霍普金斯大学药物发现实验室也在积极寻找其他因毒性问题而在临床试验中失败的药物。他们希望将这种前体药设计应用到治疗其他疾病的药物上。