
-

生物通官微
陪你抓住生命科技
跳动的脉搏
乳腺癌:为什么转移会扩散到骨骼
【字体: 大 中 小 】 时间:2022年04月22日 来源:medical Xpress
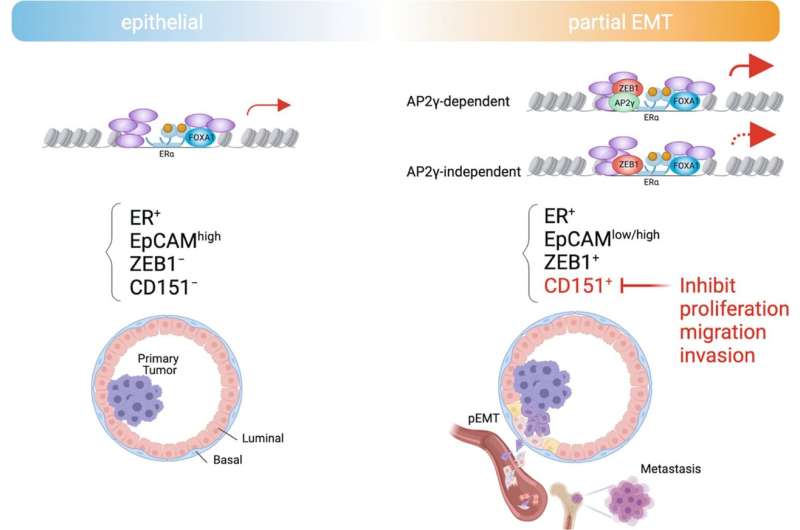
当癌细胞脱离原发肿瘤并转移到其他器官时,这被称为“转移性癌症”。然而,受这些转移影响的器官,部分取决于它们的起源组织。就乳腺癌而言,它们通常在骨骼中形成。日内瓦大学(UNIGE)的一个研究小组与苏黎世联邦理工学院的研究人员合作,试图确定是什么决定了受转移影响的器官,他们发现了一种参与这种现象的蛋白质。这一发现可能会导致抑制转移的治疗方法的发展。这项研究发表在《Nature Communications》杂志上。
从肿瘤的原发部位开始,癌细胞可以侵入它们的微环境,然后通过血液和淋巴管循环到远处的健康组织,形成转移。在转移性乳腺癌的病例中,癌细胞主要寄生在骨头上,但也可以在其他器官中发现,如肝脏、肺部或大脑。
肿瘤细胞的可塑性
虽然对转移过程不同阶段的分子和细胞机制尚未完全了解,但研究表明,细胞可塑性发挥了重要作用。这个术语指的是细胞改变功能和/或形态的能力。因此,转移性肿瘤细胞改变其形状并变得可移动。
科学系分子与细胞生物学系Didier Picard教授的实验室对与乳腺癌相关的转移过程的控制机制感兴趣。他的团队与Nicolas Aceto教授在ETHZ的团队合作,在小鼠身上研究这些过程。生物学家们研究了蛋白质ZEB1在乳腺癌细胞迁移中的潜在作用,众所周知,ZEB1可以增加细胞可塑性。
“与女性不同,移植了人类乳腺癌细胞的小鼠会转移到肺部,而不是骨骼,”该研究的第一作者、分子与细胞生物学部门的研究员纳斯塔兰・穆罕默迪・加哈里(Nastaran Mohammadi Ghahhari)说。“因此,我们试图识别能够诱导骨组织转移的因素,特别是ZEB1因素的影响。”
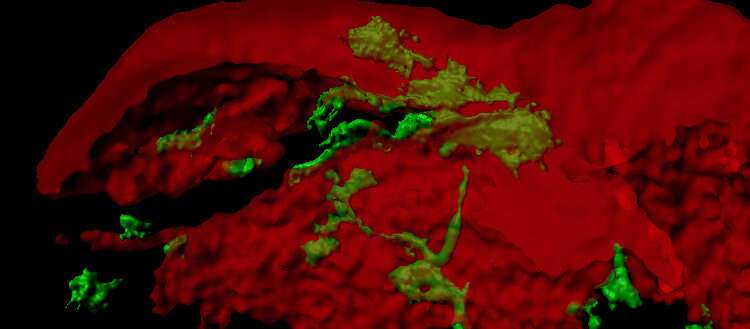
引导骨转移
在体外迁移和侵袭实验中,科学家们发现,与不表达ZEB1的癌细胞不同,表达ZEB1的癌细胞转移到了骨组织。这些结果后来在将人乳腺癌细胞移植到小鼠乳腺中得到证实。如果癌细胞不表达ZEB1,转移主要发生在肺。相反,当ZEB1存在时,转移也发生在骨骼中,就像女性的情况一样。
该研究的通讯作者迪迪埃・皮卡德解释说:“因此,我们可以假设,这种因子在肿瘤形成过程中表达,并指导获得转移特征的细胞向骨骼转移。”
这项研究证实了肿瘤细胞可塑性在转移过程中的重要性,从长远来看,可以考虑新的治疗方法来防止转移的出现。
日内瓦大学提供