
-

生物通官微
陪你抓住生命科技
跳动的脉搏
新品上市∣重组腺相关病毒提取纯化新利器,两种方法按需选择
【字体: 大 中 小 】 时间:2022年05月11日 来源:Takara
腺相关病毒(AAV)不仅是一种生物学研究工具,也作为基因治疗载体而为大家所熟知。在基因治疗这场竞技赛中,腺相关病毒(AAV)载体已经迅速成为体内基因导入主要平台之一(Goswami et al. 2019)1,为治疗常见和罕见遗传性疾病带来了新希望。
AAV是一种非包膜的线性单链DNA病毒,有100多种血清型,对人类无致病性,只有在辅助病毒(如腺病毒或疱疹病毒)存在的情况下才会复制。经过重组和改造的AAV拥有不同的血清型,根据血清型不同而具有不同的宿主范围和病毒特征,可以有效作用于特定细胞类型,包括分裂和非分裂细胞类型。使用者需要根据靶标细胞或者组织类型选择适合的血清型。目前使用频率较高的血清型为AAV2,其它血清型也逐渐被广泛使用。
AAV之所以作为治疗研究的高效基因传递工具而被认可,正是因为它具有对人类无致病性、持续的病毒持久性、具备使用多种重组AAV血清型可靶向特定细胞和组织类型的能力(Büning 2019)2。而要充分发挥这项潜能,AAV必须具有高纯度。除此以外,当使用AAV进行动物个体基因导入时,使用高纯度的病毒粒子可以去除源自病毒包装细胞和培养基的杂质。在向培养细胞导入基因时,使用纯化后的AAV可以消除杂质所带来的影响。
然而,目前许多AAV纯化模式依赖于血清型,需要针对每个血清型进行单独的方法开发和优化,这无疑是繁琐和不便的。我们的AAVpro “All Serotypes” 系列提供2种适用于所有血清型的AAV提取纯化方法,使用方便,可按需选择。
“秘制”提取纯化法
从包装细胞和培养上清液中提取纯化
不同血清型和不同包装细胞培养条件下,AAV粒子在包装细胞和细胞培养液中的分配比例有所不同。对于除AAV2以外的血清型,病毒粒子在细胞培养上清液中可能比在细胞裂解液中更有代表性(Vandenberghe et al., 2010)3。同时从包装细胞和培养上清液中提取纯化AAV粒子,可以获得更高的病毒产量。
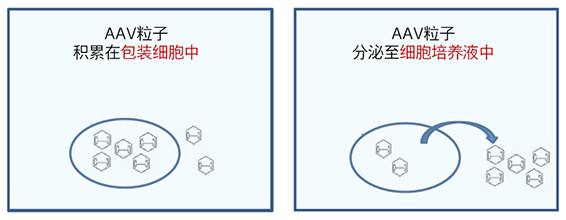
AAVpro Cell & Sup. Extraction/Concentration Pack Maxi (All Serotypes) 通过使用特别的AAV病毒提取方法,从AAV包装细胞和培养上清液中提取病毒粒子,提供更高的病毒产量,不需要像冻融法和超声波破碎法那样繁琐的操作。
AAVpro Purification Pack Maxi(All Serotypes) 可用于进一步纯化AAV病毒提取液,获得高纯度AAV粒子。这种纯化方法可用于从病毒提取液中纯化任何血清型的AAV粒子,无需超速离心。纯化获得的高纯度的AAV粒子,可直接用于体内转导或培养细胞的转导。该试剂盒中已包含了Cryonase冷启动核酸酶。
上述两者搭配使用,可在大约7小时内从包装细胞及其培养上清液中纯化获得高纯度AAV粒子,操作简便节省时间,重要的是可适用于任何血清型。从纯化量上来说,也是非常友好的,包含4次AAV纯化所需要的缓冲液和纯化柱,每次可以纯化5个T225培养瓶收集的包装细胞和培养上清液中的AAV粒子。
冻融提取纯化法
从包装细胞中提取纯化,活细胞或者冷冻细胞
冻融法是从包装细胞中提取AAV粒子的常用方法之一。通常的操作是使用液氮破碎细胞,将细胞置于液氮中冻结,再放至37℃水浴中溶解,剧烈振荡。这样反复冻融3-4 次,需要花费至少30-40分钟的时间。
AAVpro Freeze-Thaw Extraction Buffer(All Serotypes) 是一款经过优化的细胞悬浮液,用于通过冻融法从AAV包装细胞中提取AAV粒子,活细胞或者冷冻细胞都可以。使用该缓冲液悬浮包装细胞,只需要一次冻融操作就能高效提取各种血清型AAV粒子。
如前所述,AAVpro Purification Pack Maxi(All Serotypes) 可用于进一步纯化AAV病毒提取液,获得高纯度AAV粒子。与AAVpro Freeze-Thaw Extraction Buffer(All Serotypes)配合使用,可以在大约4个小时内纯化并浓缩AAV包装细胞中的AAV粒子,以获得高纯度AAV粒子,而无需超速离心等繁琐操作。
无论是哪一种提取纯化方法,我们都对提取纯化后AAV粒子的纯度和感染性能进行了测评。这两种提取纯化方法都可以帮助研究人员获得高纯度的AAV粒子,并且这些高纯度的AAV粒子依然保持其感染能力。研究人员可以根据需求,选择相对应的提取纯化方法。
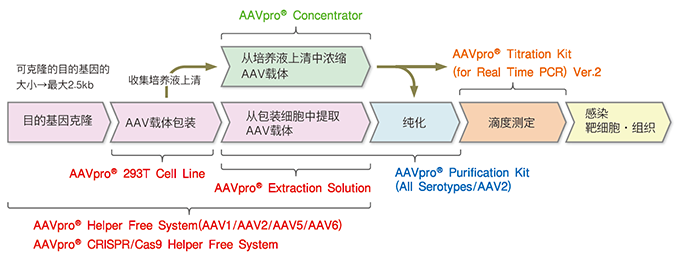
在AAV方面,Takara Bio具有完善的AAV产品解决方案,一站式配齐AAV研究装备。了解更多>>
References
1.Goswami, R. et al., Gene therapy leaves a vicious cycle. Front. Oncol. 9, doi: 10.3389/fonc.2019.00297.
2.Büning, H. and Srivastava, A. Capsid Modifications for Targeting and Improving the Efficacy of AAV Vectors. Mol. Ther. Methods Clin. Dev. 12, 248–265 (2019).
3.Vandenberghe et al., Efficient Serotype-Dependent Release of Functional Vector into the Culture Medium During Adeno-Associated Virus Manufacturing. Human Gene Therapy. 21, 1251–1257 (2010).