
-

����ͨ��
����ץס�����Ƽ�
����������
����ѧԺ�����ܿ����鿪������Cas�л���༭ϵͳ������ʾ��DNAʶ���и����
�����壺 �� �� С �� ʱ�䣺2023��01��20�� ��Դ���廪����ѧԺ
�༭�Ƽ���
����CRISPR-Casϵͳ��Ϊϸ������ϸ���Լ����ɾ���ֿ���Դ�������ֵ�һ����Ӧ������ϵͳ���ѱ��㷺Ӧ���ڻ�������ѧ�о���ũҵ���֡����༲�������Լ����������ȷ��档���������о�����Cas����ø�����ཫCRISPR-Casϵͳ�����Ϊ2�����࣬6�����ͣ�����V��Cas12ϵͳ�����������Ϊ�ḻ�����Ҵ��ڶ��ֽ�С���ӳߴ�ĺ���øϵͳ����CasX (Cas12e����Cas14 (Cas12f����Cas�� (Cas12j���Լ�Cas12i�ȡ������о���ͨ��������ƺͶ�...
CRISPR-Casϵͳ��Ϊϸ������ϸ���Լ����ɾ���ֿ���Դ�������ֵ�һ����Ӧ������ϵͳ���ѱ��㷺Ӧ���ڻ�������ѧ�о���ũҵ���֡����༲�������Լ����������ȷ��档���������о�����Cas����ø�����ཫCRISPR-Casϵͳ�����Ϊ2�����࣬6�����ͣ�����V��Cas12ϵͳ�����������Ϊ�ḻ�����Ҵ��ڶ��ֽ�С���ӳߴ�ĺ���øϵͳ����CasX (Cas12e����Cas14 (Cas12f����Cas�� (Cas12j���Լ�Cas12i�ȡ������о���ͨ��������ƺͶ�������ȷ�����������Щϵͳ�Ļ���༭Ч�ʣ�����Ŀǰ�Ѿ�������Cas12����ֻ��ʶ��T��PAM (T-rich PAM)���������谭��Cas12��������ڻ���༭�Լ������ٴ����ȵ�Ӧ�á�
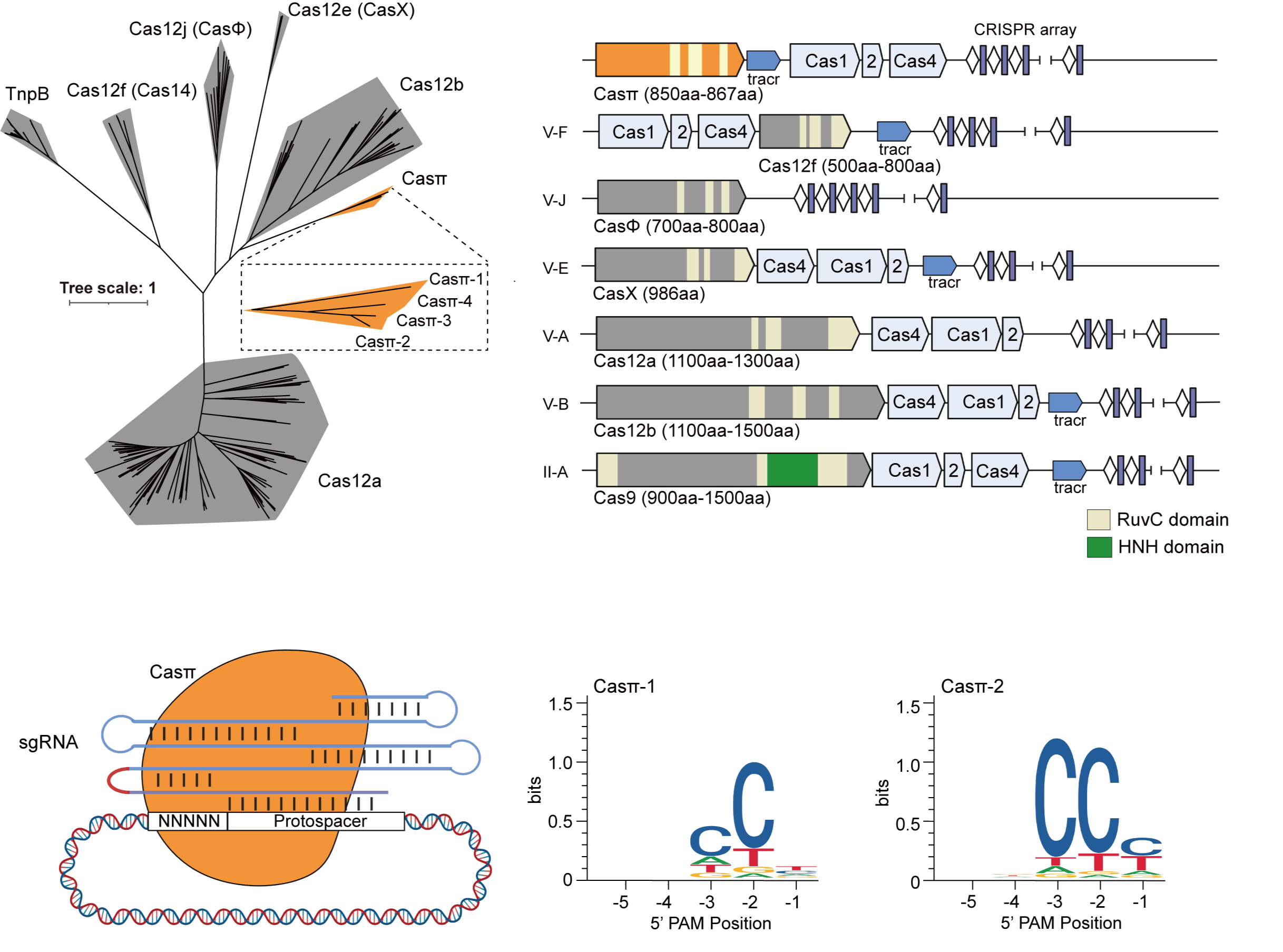
ͼ 1. CRISPR-Cas��ϵͳ���ھ�����PAMɸѡ����
�����ܣ�Jun-Jie Gogo Liu�������鳤�ڹ�עDNA��RNA����ø�о�����غ�����ݹ��ߵĿ�����Ӧ�á��������������ܼ�������߷��ֲ�������һ������ڻ���༭������ʶ��T-rich PAM��С��CasX����ø��Nature, 2019������ͨ�������ʺ�sgRNA�Ľṹ�����һ�������˸�ϵͳ�Ļ���༭Ч�ʣ�Molecular Cell, 2022����
2023��1��17�գ������ܿ������ڡ�ϸ���о�����Cell Research����־���߷�������Ϊ�����յ�Cas�� (Cas12l)���ֻ���ΪDNA�����ṩ��һ�����صĽṹƽ̨��(The compact Cas�� (Cas12l) ��bracelet�� provides a unique structural platform for DNA manipulation)���о����ġ�������һ�����������ġ���ΪCas�� (Cas12l) ������CRISPR-Cas12�������ø�� Cas�к���øͨ��ʶ��CCN PAM���и����DNA�����ڲ��鶯��ϸ����ʵ����Ч�Ļ���༭�����⣬�����黹������Cas�е����sgRNA�����DNA�ĸ�����ṹ����ʾ��ϵͳ����ʶ����ƣ�ΪRNA�����ĺ���øϵͳ�Ľ��������ṩ���µ��ӽǡ�
Ϊ��Ѱ����������֪�����ȫ��CRISPR-Casϵͳ�����������ȹ�����һ���Ż���������Ϣ�ھ����̣���Cas����RuvC�ṹ�����й����������ɷ�ģ�ͣ�HMM�������ö��ֵ�������ά��Cas�����ص��ͬʱ�����Ӳ���ȡ����øõ���ģ�ͽ�϶���CRISPR-CasԤ�ⷽ�����������ڱ��������ij�����ˮ������������У�����һ�����ͷ��²�����Դ��С��CRISPR-Cas��(Cas12l)ϵͳ��Cas�е�����850-867����������ɣ�����II��-V�� CRISPR-Casϵͳ��ͼ1����
������ͨ��PAMɸѡʵ��֤����Cas�к���øʶ��CCN PAM����һ����������������Cas12���嵰��ʶ��T-rich PAM��ͬ����չ��CRISPR����༭���ߵİб��ȣ�ͼ1����Cas�е�˳ʽ�и�ͷ�ʽ�и������㷺ʹ�õ�LbCas12a��1228�����ᣩ�����൱��ϵ�е���������������������һ��С��CRISPR-Cas���״����������ԣ�Cas�к���ø�Ըߵ��¶ȡ���ͬ��Ũ�Ⱥͳ��ߵ���Ũ�Ⱦ��������õ����ܶȣ����ܱ����ֶ������Ӽ������³����ǿ��ΪCas�еĺ�����Ӧ�õ춨�˻�����
Ϊ�˽�һ��̽��Cas��ϵͳ�Ļ���༭DZ�������������ȳ����˸�ϵͳ��ԭ�������е�DNA�и������������������������ccdB��Cas��ϵͳ������Ч���ccdB���ԶԴ˾����������ơ���һ��������������Cas��ϵͳ��HEK293Aϸ��ϵ�������в��������ͻ��GFP����ϵͳλ�� (out-of-frame EGFP cell line) ����Դ����λ����б༭��������������Ȳ������������˱༭����������������δ�������Ż���Cas�пɶ������������������Ч�༭����LbCas12aЧ���൱����߿ɴﵽSpyCas9�༭Ч�ʵ�һ�루ͼ2��������˼���ǣ���Ƭ��ɾ���ı༭�����У�Cas����Ҫ����<25nt�Ķ�Ƭ��ɾ����
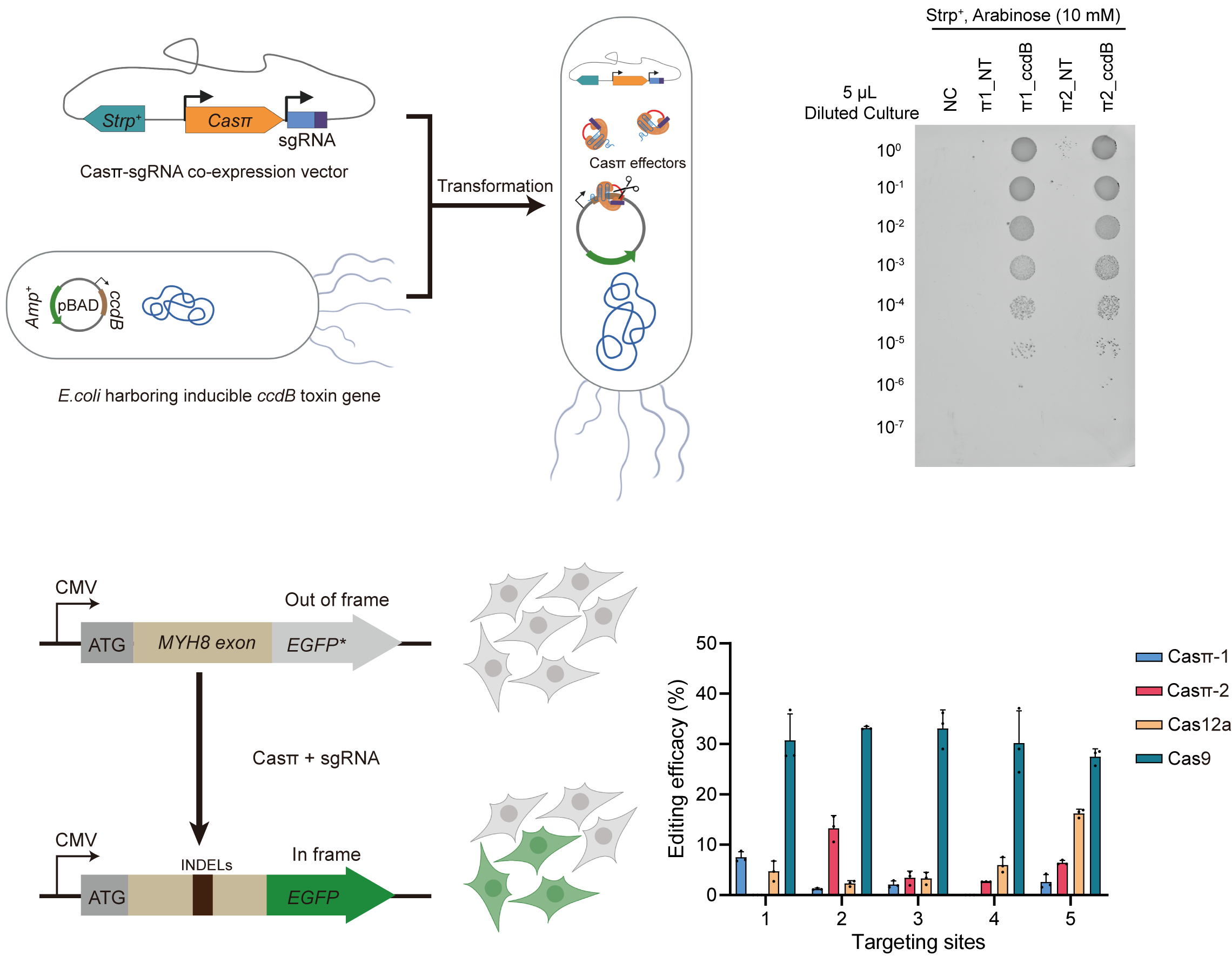
ͼ 2. Cas����ϸ�����������и���鶯��ϸ�����ڵĻ���༭Ч�ʽ��չʾ
��һ����������ͨ���������䶳�羵����������Cas��-sgRNA-DNA��Ԫ������ṹ���ýṹ��������֪�ṹ��CRISPR-Casϵͳ��ȣ������ĸ����͵ġ�δ֪���ܵĵ����ʽṹ��LC��PRS��HNC��PCT�ṹ�����У�PRS�ṹ����Ϊһ������69��������ij�����������������Cas�и����壬ʹCas��-sgRNA-DNA�Ľṹ���֡��ֻ�(bracelet)��״�ṹ����ͬ��II����Cas12��Cas9���嵰�׳����ġ�˫Ҷ�� (two-lobe)���ṹ��ͼ3�������⣬���Ƿ���Cas��ͨ��R390��R392������л�������ʶ��CCN PAM��Ϊǰ�����ﻯѧʵ�����ṩ������֧�š�������ӱ�ĵ��ṹ֮�⣬��ϵͳ��sgRNAҲ���ֳ����صġ�˫��״ (two-arm scaffold)���ṹ��������Ҳ֤�������ڽṹ��sgRNA���м�����Ч����Cas�е�DNA�и���ԡ�Cas��-sgRNA-DNA��Ԫ������ṹ�а���������Cas���ṹ���sgRNA���������Ϊ��һ���Ż������������༭Ч���ṩ�������µ��ӽǡ�
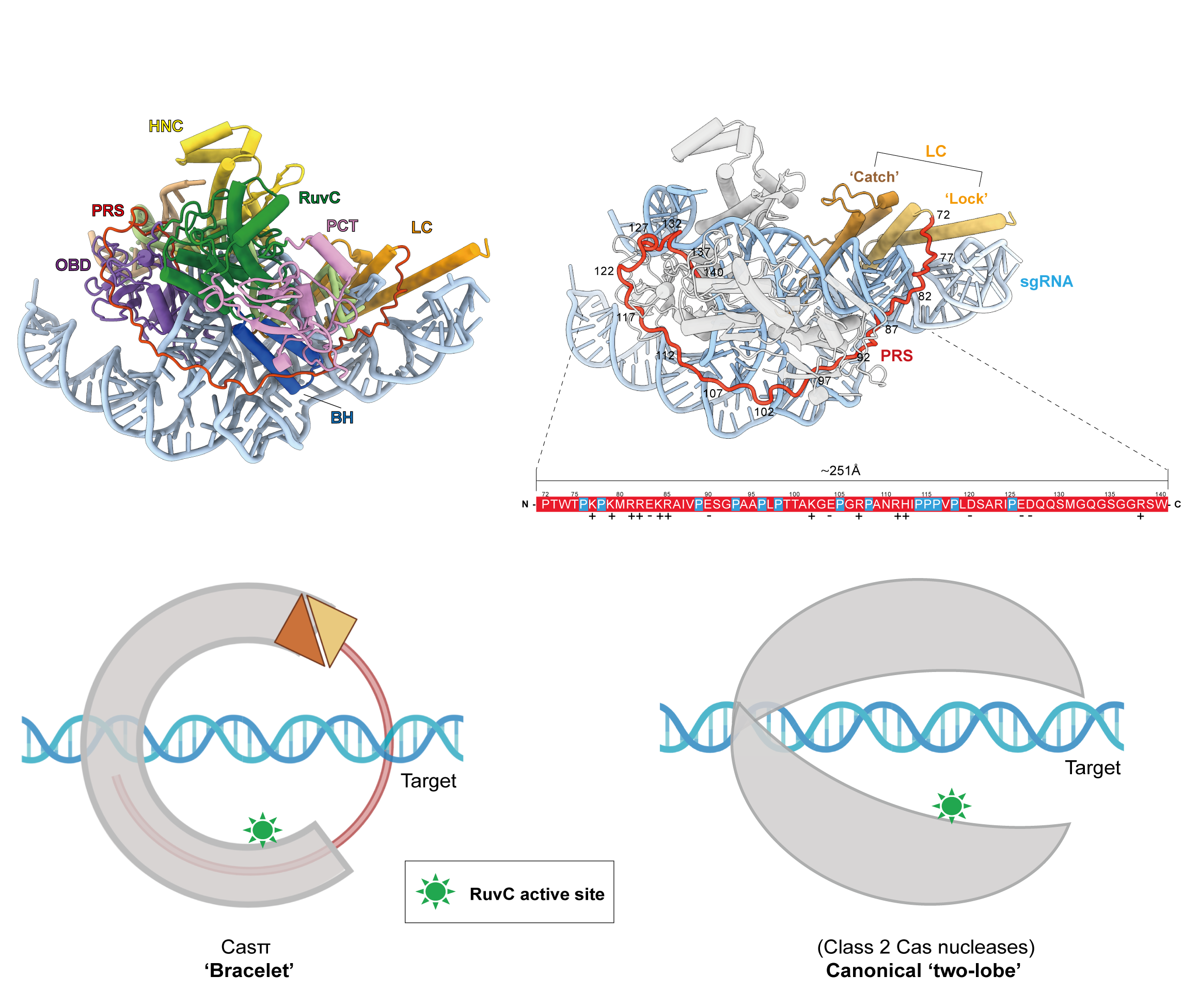
ͼ3. Cas��-gRNA-DNA������ṹ��PRS�ṹ���ֻ�(bracelet)��״�ṹģʽͼ
��Ȥ���ǣ�������ͨ���Ƚϸ�ϵͳ����д����Ե�II�� CRISPR-Cas RNPЧӦ�������е�Cas����gRNA��������������һ���������˳��������ϵ������һ��ЧӦ�������У����Cas����Խ��gRNA��ԽС�������ķ�������������������RNA��CRISPRЧӦ�����в��ɻ�ȱ����Ҫ���ã���������С�ͺ��͵�CRISPR-Casϵͳ�С�ͬʱ����������СCas��������ΪĿ����о�������Ҫ�ʵ�����RNA��������ά��ϵͳ���ԡ���ϡ�RNA ���硱��˵�������������CRISPR-CasЧӦ�����������Դ��RNA��ø�Ľ�����˵������һ�������У����ܴ���һ����RNA�����������ǵ��ף��Ľ����Σ�������������и��������Ҫ�������ã�������ǿRNA��ø���ԣ�ͼ4����������Ҳ��ʶ������Щ�����ϵͳ�����Ѿ������ڣ���ʹ���ڣ���Cas����Ϊ��Ҫ�ο����ھ�����Ҳ�����������ǡ�Ȼ���������ھ�Ŀǰ��CRISPR-CasЧӦ�������ʾ����RNA��������ȡ����ԭ����Ҳ���ܰ�������ͨ���������ԭ�Ǹ����������硣���Ǹ������RNA�����������Ҫִ���ߡ��ɴ˿������ṹ�ԡ�������RNA��δ�������\����չ�У���ֵ�ù�ע��DZ�����ӡ�
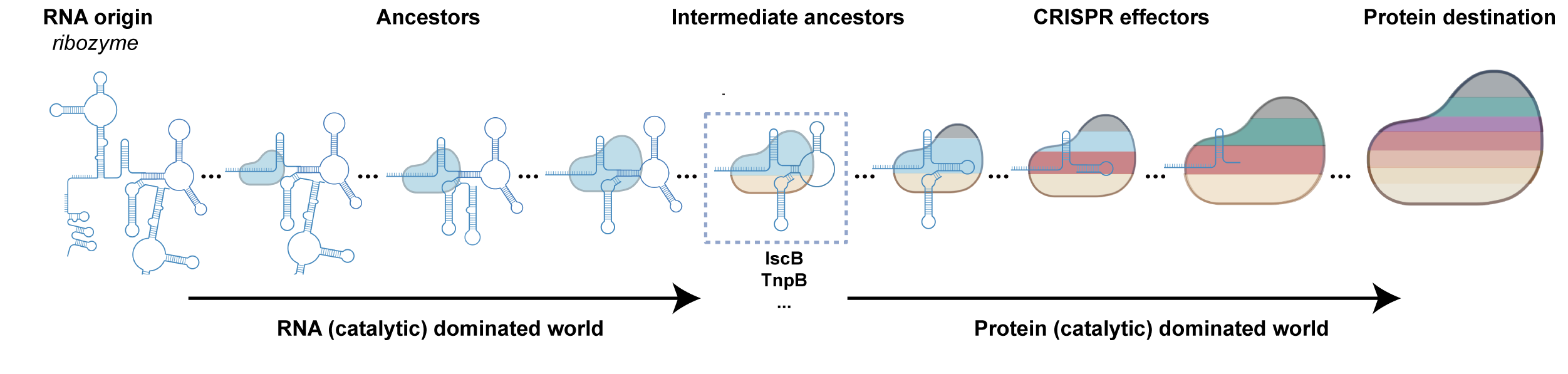
ͼ4. RNAָ���ĺ���øϵͳ����RNA��ͬ�����IJ���
�廪��ѧ����ѧԺ�������������ں��廪��ѧ����ѧԺ���о�Ա����Ϊ���Ĺ�ͬͨѶ���ߣ��廪��ѧ����ѧԺ2020����ʿ�о�����¡�2020����ʿ�о������ƽ������ѧԺ��ʿ���֮�����߾���ṹ����Խѧ��������Ϊ���Ĺ�ͬ��һ���ߣ��廪��ѧ2018����ʿ�о����Է��2019����ʿ�о������ϡ�2022����ʿ�о�����¡�����ѳ�վ��ʿ������ٻ������������������ݸ���������ѧ������ѧ�빤��ѧԺ��˼ͮ�о�Ա������ϼ���뱾���о����廪��ѧ�䶳�羵ƽ̨��ˮľδ��(����)�Ƽ�����˾�����ҵ����ʿ�ѧ���ģ����������廪��ѧ������������ƽ̨Ϊ���о��ṩ���豸�ͼ���֧�֡����о��õ��˹����ص��з��ƻ����л�����ũҵũ�岿��������Ȼ��ѧ�����������ʵ������������֧�֡�
ԭ�����ӣ�https://www.nature.com/articles/s41422-022-00771-2
 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
֪����ҵ��Ƹ