
-

生物通官微
陪你抓住生命科技
跳动的脉搏
上海交大研究团队发现癌细胞借助神经来对抗饥饿疗法
【字体: 大 中 小 】 时间:2023年10月25日 来源:赛业生物
编辑推荐:
上海交通大学医学院附属第九人民医院口腔颌面-头颈肿瘤科季彤/王旭/孙树洋领导的研究团队近日在《Cell Metabolism》杂志上发表论文,首次揭示了癌细胞能够利用伤害性感觉神经(nociceptive nerves)在营养不良的环境中生长,而破坏癌细胞与伤害性感觉神经之间的相互作用可以有效提高饥饿疗法的抗肿瘤效果。
为了对付癌症,科学家在上世纪70年代就提出了著名的“饥饿疗法”,即通过抑制肿瘤生长所需的血管生成,阻断其获得氧气和养分,从而最终“饿死”肿瘤。尽管这种疗法能够对多种癌症产生强烈的抗肿瘤作用,但令人惊讶的是,癌细胞可以利用肿瘤微环境(TME)在营养不良的环境中茁壮成长。
神经也是TME中不可或缺的细胞成分。人们普遍认为,外周神经(包括交感神经、副交感神经和感觉神经)参与了TME的构建,可调控癌症发生和进展。有趣的是,一项最新研究发现,一种依赖于外源性丝氨酸的胰腺癌细胞亚型可利用神经来供应丝氨酸,表明癌症相关神经与TME中的癌症代谢存在着广泛的联系,但这种联系在很大程度上还不为人所知。
上海交通大学医学院附属第九人民医院口腔颌面-头颈肿瘤科季彤/王旭/孙树洋领导的研究团队近日在《Cell Metabolism》杂志上发表论文,首次揭示了癌细胞能够利用伤害性感觉神经(nociceptive nerves)在营养不良的环境中生长,而破坏癌细胞与伤害性感觉神经之间的相互作用可以有效提高饥饿疗法的抗肿瘤效果。

图片来源:《Cell Metabolism》(https://doi.org/10.1016/j.cmet.2022.10.012)
研究材料与方法
此次研究以口腔鳞状细胞癌(OSCC)为模型,对100多名患者的样本开展了分析。研究者还利用OSCC细胞系Cal27和黑色素瘤细胞系B16F10构建了小鼠舌异种移植模型。在分析CGRP蛋白的作用时,研究人员使用了赛业生物提供的Calcaflox/flox和Rosa26Calca/Calca小鼠。他们利用不同的AAV载体在舌黏膜的伤害性感觉神经中表达转基因,并通过高剂量的辣椒素来进行去神经化处理。研究者还使用了PET-CT成像、3D培养和转录组测序等方法。
技术路线
01 通过小鼠舌异种移植模型,发现癌症相关的伤害性感觉神经促进肿瘤生长
02 体外和体内实验表明,伤害性感觉神经介导的促生长作用依赖于低糖环境
03 信号阻断和siRNA等实验表明,神经源性CGRP在低糖环境下介导了伤害性感觉神经对癌细胞的生长促进作用
04 神经源性CGRP在癌细胞中诱导保护性自噬,而自噬依赖于Rap1-GTPase信号通路的激活
05 通过Rimegepant破坏癌细胞与伤害性感觉神经之间的相互作用,可增强营养饥饿疗法的效果
研究结果
伤害性感觉神经在低糖环境下促进癌细胞生长
口腔鳞状细胞癌的特征之一是患者报告疼痛和神经周围浸润(PNI)发生率较高。研究人员在分析小鼠肿瘤和人类患者后发现,OSCC中存在高密度的TRPV1+伤害性感觉神经。降钙素基因相关肽(CGRP)通常可作为伤害性感觉活动的分子指标。他们发现,CGRP在OSCC组织的癌症相关伤害性感觉神经中被检测到,而且CGRP+伤害性感觉神经比例较高的患者总生存率较低,提示伤害性感觉神经在OSCC进展中起作用。
为了进一步研究伤害性感觉神经在癌症进展中的作用,研究人员在小鼠的舌粘膜下层分别了接种了人类OSCC细胞系Cal27和黑色素瘤细胞系B16F10,以建立小鼠舌异种移植模型。所有移植物都检测到了神经生态位和高比例的CGRP+神经。小鼠血浆中的鼠类CGRP从第8天开始缓慢增加,这表明小鼠的伤害性感觉活动升高。在使用高剂量的辣椒素削弱伤害性感觉神经后,Cal27和B16F10肿瘤均变小了,表明癌症相关的伤害性感觉神经有助于肿瘤生长。
接着,研究人员探讨了伤害性感觉神经如何促进肿瘤生长。在小鼠舌异种移植模型中,肿瘤组织中葡萄糖含量的下降幅度比邻近的正常组织明显更大,表明肿瘤在口腔黏膜中快速消耗葡萄糖。同时,舌异种移植物中的应激反应蛋白和糖酵解酶水平更高,表明高的糖酵解活性可能促成了OSCC肿瘤的低糖环境。
在低糖条件下,三叉神经节条件培养基(TG CM)的培养促进了肿瘤细胞的生长。研究人员利用Cal27细胞开展体外实验,表明在低糖环境下,伤害性感觉神经会促进癌细胞增殖。之后,研究者在小鼠身上开展实验,采用30%的葡萄糖水迫使异种移植瘤中的葡萄糖含量升高。研究者发现,肿瘤内葡萄糖含量的增加逆转了去除伤害性感觉神经介导的抗生长作用。这些体外和体内实验表明,伤害性感觉神经介导的促生长作用依赖于低糖环境。
神经源性CGRP介导了伤害性感觉神经的促生长作用
神经可释放多种分子来调节TME,包括代谢物、神经肽和核酸。研究人员推测,培养基中的分泌型活性蛋白介导了伤害性感觉神经的促生长作用。于是,他们使用Rimegepant(CGRP受体拮抗剂)来阻断CGRP信号,发现TG CM介导的细胞生长被显著抑制(图1)。同时,通过siRNA敲低CGRP结合蛋白(CLR或RAMP1)也能达到类似的效果,表明体外伤害性感觉神经对癌细胞的生长促进作用部分源于神经源性CGRP。
体内实验进一步证实了这些结果。研究者利用Calcaflox/flox和Rosa26Calca/Calca小鼠(由赛业生物提供)开展的实验表明,在条件性敲除舌黏膜伤害性感觉神经中的Calca(CGRP编码基因)后,B16F10舌异种移植物的生长受到显著抑制(图1)。这些结果表明,神经源性CGRP在低糖环境下介导了伤害性感觉神经对癌细胞的生长促进作用。
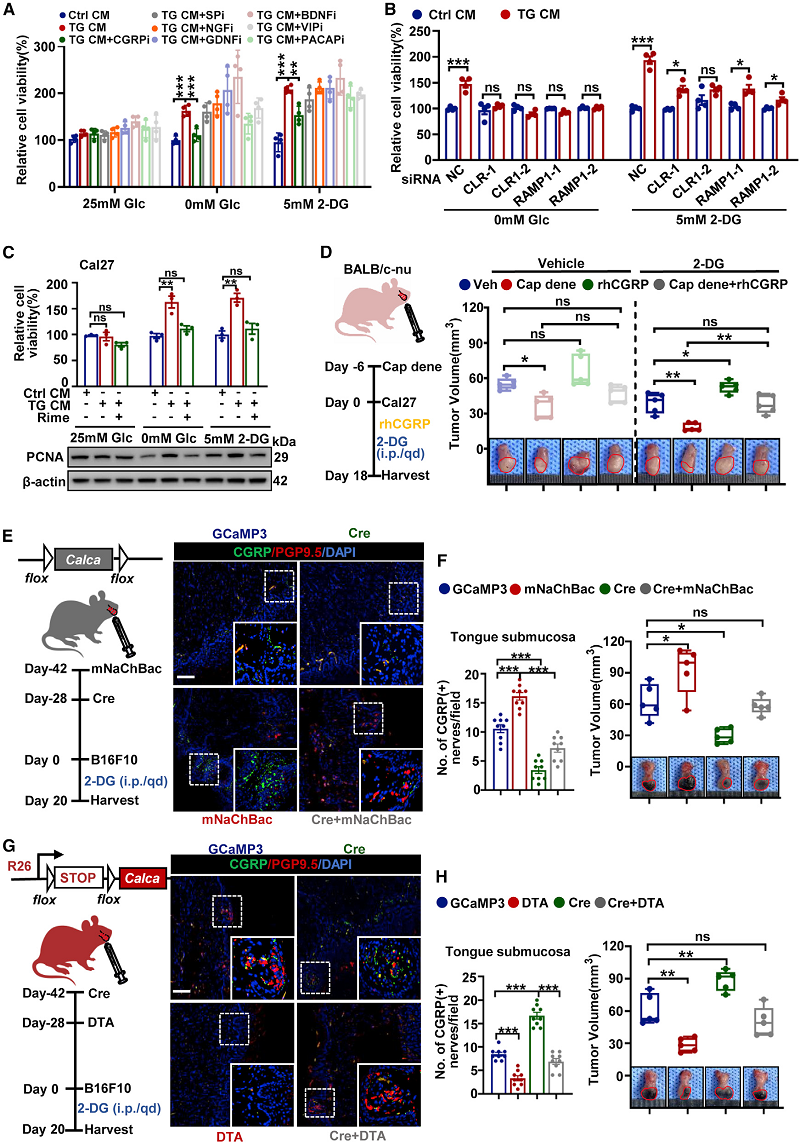
图1 神经源性CGRP介导了伤害性感觉神经对癌细胞的生长促进作用[1]
研究人员进一步分析后发现,在与高CGRP神经生态位邻近的肿瘤区域,Ki67+癌细胞比例更高。肿瘤组织中CALCA水平较高的患者的总生存期和无病生存期较差。与健康供体相比,OSCC患者的术前血浆CGRP水平明显更高。此外,在人类OSCC组织中,CLR和RAMP1都在癌症相关神经生态位周围的癌细胞中表达。由此可见,神经源性CGRP及其受体CLR在OSCC进展过程中异常升高,并与患者结局较差相关。
神经源性CGRP诱导癌细胞的保护性自噬
为了深入了解神经源性CGRP在低糖环境下的作用机制,研究人员比较了在高糖和低糖培养条件下的Cal27细胞的转录组,发现仅在低糖培养条件下表达变化的基因与多条自噬途径显著相关。在低糖培养条件下和2-DG处理后,采用rhCGRP处理Cal27细胞会提高LC3B-II水平,并降低p62水平,且细胞中的自溶酶体和自噬体数量上调。同样地,TG CM可显著诱导OSCC PDE癌细胞的自噬通量,而Rimegepant可拮抗自噬通量。这些结果表明在低糖环境中,伤害性感觉神经通过神经源性CGRP诱导癌细胞的保护性自噬。后续的分析发现,CGRP诱导的细胞保护性自噬依赖于Rap1-GTPase信号通路的激活。Rap1激活通过破坏mTOR与Raptor的相互作用而抑制mTOR的磷酸化。
在低糖环境下,癌细胞利用伤害性感觉神经产生CGRP
接下来,研究团队又反过来思考:癌细胞如何影响TME中的伤害性感觉神经?研究者发现,与癌细胞共培养会导致三叉神经节中的Calca水平升高,而对癌细胞进行低糖培养和2-DG预处理会导致Calca水平明显升高,表明低糖环境会在某种程度上增加癌细胞对伤害性感觉神经的影响。进一步分析发现,在低糖条件下,癌细胞通过上调神经生长因子NGF的表达来促进伤害性感觉神经分泌CGRP,而癌细胞分泌NGF依赖JNK-c-Jun通路。体内实验也证明了这一点,癌细胞在低糖环境下利用伤害性感觉神经产生CGRP。
破坏癌细胞与伤害性感觉神经之间的相互作用
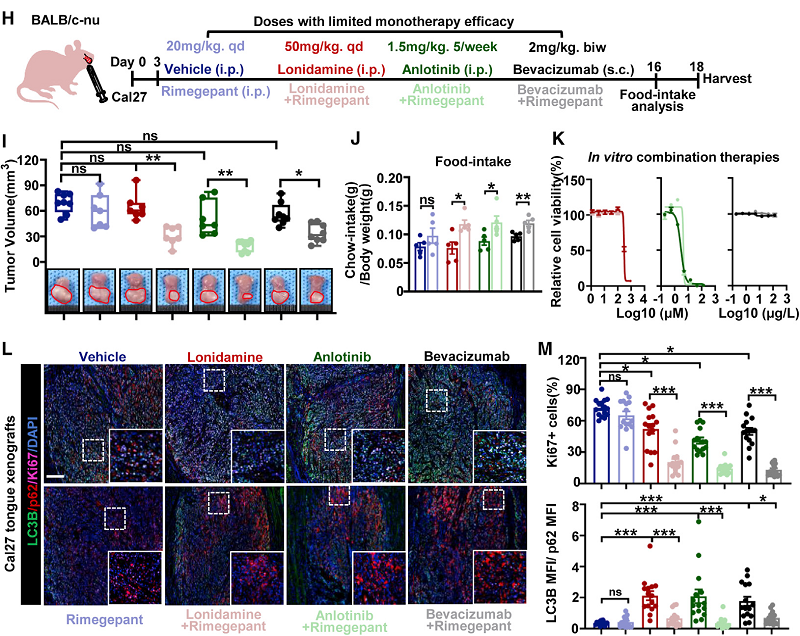
图2 破坏癌细胞与伤害性感觉神经的互作可增强饥饿疗法的抗肿瘤效果[1]
研究人员推测,破坏癌细胞与伤害性感觉神经之间的相互作用可增强营养饥饿疗法的效果。他们发现,糖酵解抑制剂(2-DG、Lonidamine)和血管生成抑制剂(Anlotinib和Bevacizumab)这两类饥饿疗法会加剧癌细胞与伤害性感觉神经之间的恶性循环。不过在与Rimegepant(CGRP受体拮抗剂)联合使用后,饥饿疗法的抗肿瘤效果可有效提高(图2)。Rimegepant目前已在国内外上市,可用于偏头痛的治疗和预防。
研究结论
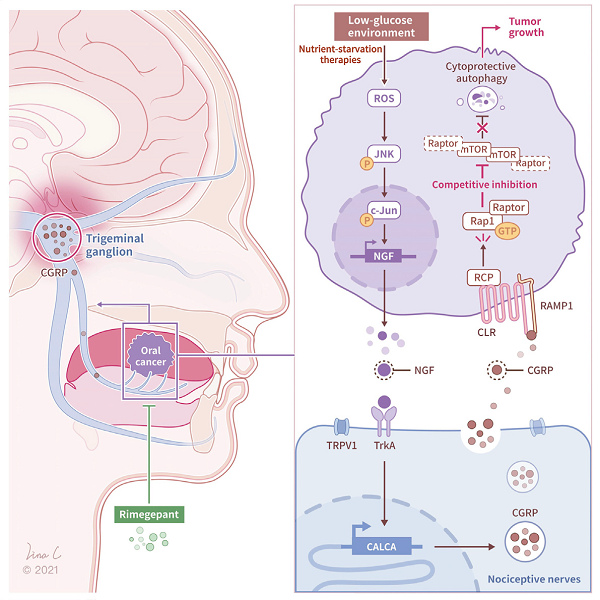
图3 癌细胞在营养不良的环境中生长的机制示意图[1]
总的来说,这项研究发现,缺乏营养的环境启动了癌细胞与伤害性感觉神经之间的恶性循环。癌细胞产生的神经生长因子利用伤害性感觉神经产生CGRP,进而促进癌细胞的保护性自噬。利用一种获批上市的偏头痛药物来阻断神经源性CGRP,可以显著提高饥饿疗法的治疗效果(图3)。
原文检索:
[1] Zhang et al., Cancer cells co-opt nociceptive nerves to thrive in nutrient-poor environments and upon nutrient-starvation therapies, Cell Metabolism (2022), https://doi.org/10.1016/j.cmet.2022.10.012