
-

����ͨ��
����ץס�����Ƽ�
����������
����ϸ�����Ͽռ似�����о���Ա���������������ڵĹؼ�ϸ������
�����壺 �� �� С �� ʱ�䣺2023��12��28�� ��Դ��10x Genomics
�༭�Ƽ���
��������ƪ�����У����ǽ��������������ڽε�ϸ���ͷ����¼��������ӹ��ڵijɹ��Ŵ���̥�̵��γɡ�
�����ּ���ǿǿ�����������������ѧ�еġ�what���͡�where������ʱ���ᷢ��ʲô�������ڡ�����ϸ�����Ͽռ似����ϵ�������з�������Щ���£����ص�����˳���������ּ������Ƶ��о����������������ú���η��Ӹ�������á�
����ƪ�����У����ǽ��������������ڽε�ϸ���ͷ����¼��������ӹ��ڵijɹ��Ŵ���̥�̵��γɡ�
����ͱ����������������ܽӴ�
�ӹ�ϵ������ѧ�ĽǶ�������ĸ��Ӥ��֮������й�ϵ������Զ�����塣̥�̵ķ�����Ҫĸ��̥���ĺ�������˫���ṩϸ�����γ���ʱ���٣��Է����е�̥�����б���������(1)��
������˵����̥��Ƥ����������ϸ����ĸ���ӹ��Ŵ���ʼ��һ���ش�Ľ�����Ŀ(2)����ë�������㣨EVT��ϸ�����������ӹ���ճĤ�㣨�ֳ�Ϊ��Ĥ��������ĸ�嶯�����������������ת��Ϊ���ߴ�����Ѫ�ܡ����������ڼ�ͨ��̥����̥���ṩ������Ӫ������(2)��
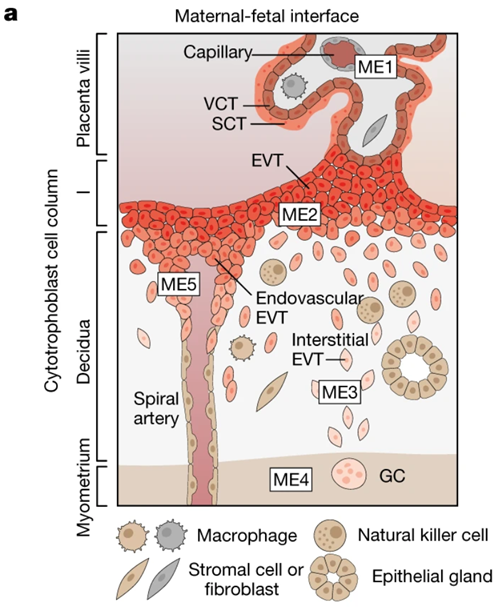
Arutyunyan���������е�ͼ1a��ĸ̥�����ʾ��ͼ��ͼ����ʾ����ë�������㣨EVT��ϸ�����ڽ���ĸ����Ĥ������������ͼƬ��Դ��Arutyunyan A, et al. Spatial multiomics map of trophoblast development in early pregnancy. Nature 616: 143�C151 (2023). doi: 10.1038/s41586-023-05869-0. (CC BY 4.0)
����ĸ����֯�Լ���ĸ��̥�������ܽ���㽨��̥�̵���Щ����Ҳ��һЩ���������R���йأ���ʱ��Щ���������������а�������ǰ�ڡ������ּ�������ĸ��Ѫѹ�쳣��֢״���ܿ�������̥���γɹ�����ĸ�嶯�����ܲ��������(3,4)��
�������̥���γɹ�����ĸ̥�����ϵ�ϸ����ϵ���������˽����R������Ļ���������Ҫ��ͬʱҲ������ȷ����Ԥ��ʩ����ȷ��������������ȫ�����
��ϸ���Ϳռ�ͼ���Ƴ�ĸ̥�����ϵ��������������ײ
Wellcome Sanger�о����ͽ��Ŵ�ѧ��Anna Arutyunyan��Kenny Roberts��Kevin Troul����Frederick Wong��Megan Sheridan��ʿ��ͨѶ����Roser Vento-Tormo��ʿ��ͬ�쵼���о��Ŷ������ĸ̥����������о�(2)��Ϊ�˸��õ��˽�̥���γɹ�����̥��������ϸ����ĸ����Ĥϸ��֮�������ã��о��Ŷ����ø߷ֱ��ʵ�ϸ������ѧ�Ϳռ�ת¼��ѧ�������о������������ӹ��г����е��Ŵ���λ(2)��
���ǵķ������֮ǰ�ĵ�ϸ�����ݺ��²ɼ���̥��-��Ĥ��֯��������Щ�����������к�PCW��5-13�ܵ�18�����壬��������2006����ǰ�ɼ��ij��ڱ�����֯�顣������Щ�浵�����Ѿ��䶳��ʮ���꣬�����ڳ��ڱ��淽���õ�����Chromium��ϸ���������͵�ϸ������ѧATAC + ���������������ȸߣ��о���Ա�ܹ�������������ĵ�ϸ���͵�ϸ��������(2)��
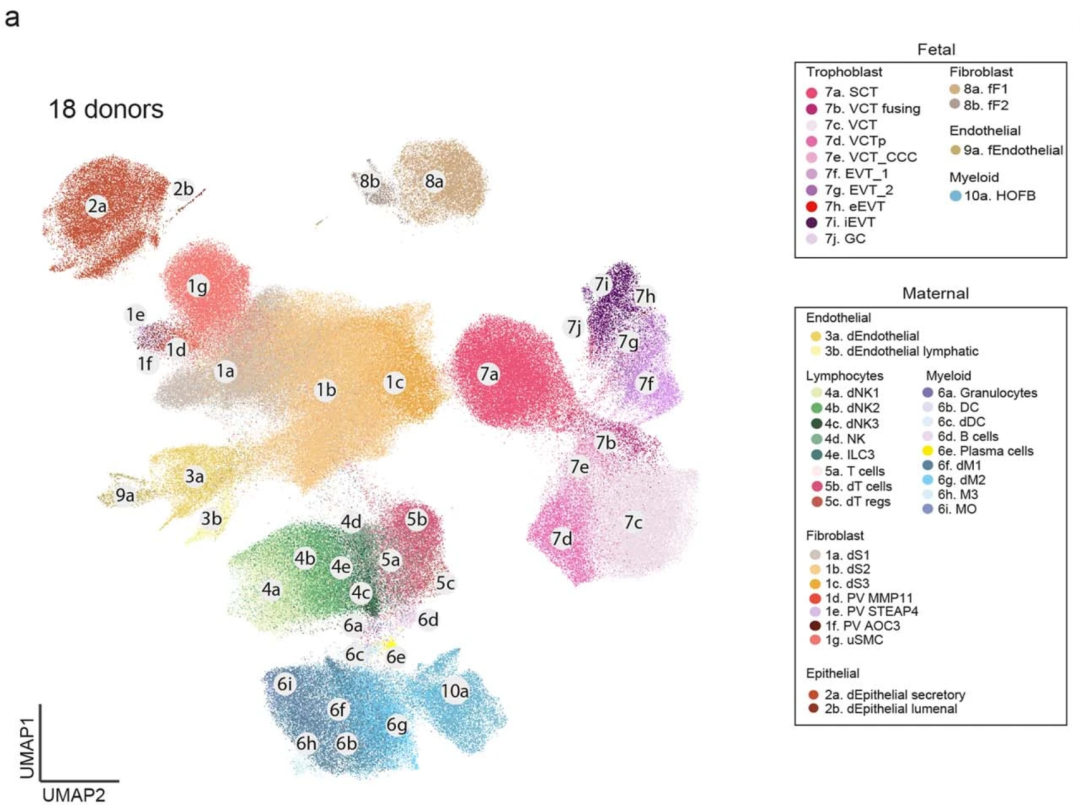
Arutyunyan���������е���չ����ͼ11a����չ����ͼ1c��������18�������ĸ̥����ĵ�ϸ��RNA����scRNA-seq���͵�ϸ����RNA����snRNA-seq�����ݵ�UMAP���������αƽ���ͶӰ��ɢ��ͼ��n = 325,665��ϸ����ϸ���ˣ�������ϸ��״̬��ɫ��ͼƬ��Դ��Arutyunyan A, et al. Spatial multiomics map of trophoblast development in early pregnancy. Nature 616: 143�C151 (2023). doi: 10.1038/s41586-023-05869-0. (CC BY 4.0)
�о��Ŷ����õ�ϸ������������ݼ�CellPhoneDB v4�ȷ������ߣ��о���ĸ̥�����п���Ӱ��������ϸ�����������-��������á����ǹ۲쵽��CXCL16+CD14+ ��Ĥ����ϸ����CXCR6+HLA-G+ EVTϸ��֮�������-������������ϵ�������ϸ���е�̥�̻����������˶��ԵĻ���(2)��
���ǻ������ִ浵��֯�����֯��Ƭ����Visium��Ƭ�ϣ�ͨ��Visium�ռ������\����չ����������ͬһ�Ų�Ƭ�ϵ�̥����̥�̣���ĸ�壨��Ĥ���ӹ����㣩��֯���������Ե���̬ѧע�ͣ���������P13���������������Ƭ(2)��
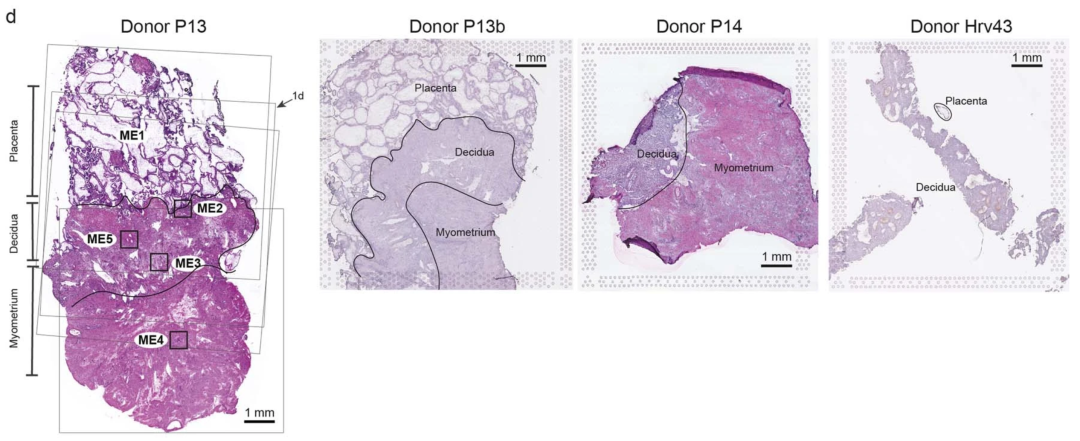
Arutyunyan���������е���չ����ͼ1d��P13��P14��Hrv43������֯����֯ѧ������H&EȾɫ������֯����ע�͡�����P13������Ŵ���λ��~ 8�C9 PCW����ͼ������ɫ����С����ʾ������������λ�ã�dz��ɫ����ʾ��֯��Visium�ռ�ת¼��ѧ�������еĶ�λ����ͷ��ʾͼ1d�н�һ��̽���Ĵ�����Visium��Ƭ������Visium������P13��n = 5����������4�Ŵ���λ���ص���������Ƭ��1������������֯��P13b����Ƭ����P14��n = 2����������λ����ͬ��������Ƭ����Hrv43��n = 1����������ͼƬ��Դ��Arutyunyan A, et al. Spatial multiomics map of trophoblast development in early pregnancy. Nature 616: 143�C151 (2023). doi: 10.1038/s41586-023-05869-0. (CC BY 4.0)
����cell2location�����ݷ������ߣ��о��Ŷ������˵�ϸ������ѧ�Ϳռ����������ݣ��������ض�Visium���ݵ��ڵ�ϸ��״̬�ܶȡ�����������Ƴ�ĸ̥����ķḻ�ռ�ͼ�ף���ӳ��������Ӷ����Ľṹ�ڵĶ���ϸ�����ͼ���������������
ͨ�������л�õ���ƫȫת¼�����ݣ��о��Ŷӷ�����ĸ�������������Ŵ�����ת���Ͷ�����DZ��ϸ���ͷ��ӻ��ơ����ǷŴ��˽���ĸ������������������ϸ���Ŀռ�λ�ã��۲쵽����EFNB1�ļ���EVTϸ����iEVT�������ͬԴ�������EPHB6��ĸ��Ѫ����ϸ��֮���������-��������ã����߿��ܻ��ƶ�iEVT��������(2)���о��Ŷӻ�ע�Ѫ����EVTϸ����eEVT�������ĸ��Ѫ�ܵ���Ƥϸ��֮����ڻ���������-��������ã�eEVT���ؽ������л��������������γɶ���(2)��
���⣬�о��Ŷӻ��ڶ�������Ŀռ�λ�ù۲쵽ϸ���������ֵ�����ã�����COL21A1�CITGA2�����Լ�Notch�ź�ͨ·�ļ�����������JAG1��JAG2�����������NOTCH2��NOTCH3���鵼��Ŀǰ��֪Notch�ź�ͨ·�鵼��Ѫ�����ɹ����з�����ϸ����������ܣ���������ǿ����ǽ鵼ĸ�嶯��ת������Ҫ�ź�ͨ·(2,5)��
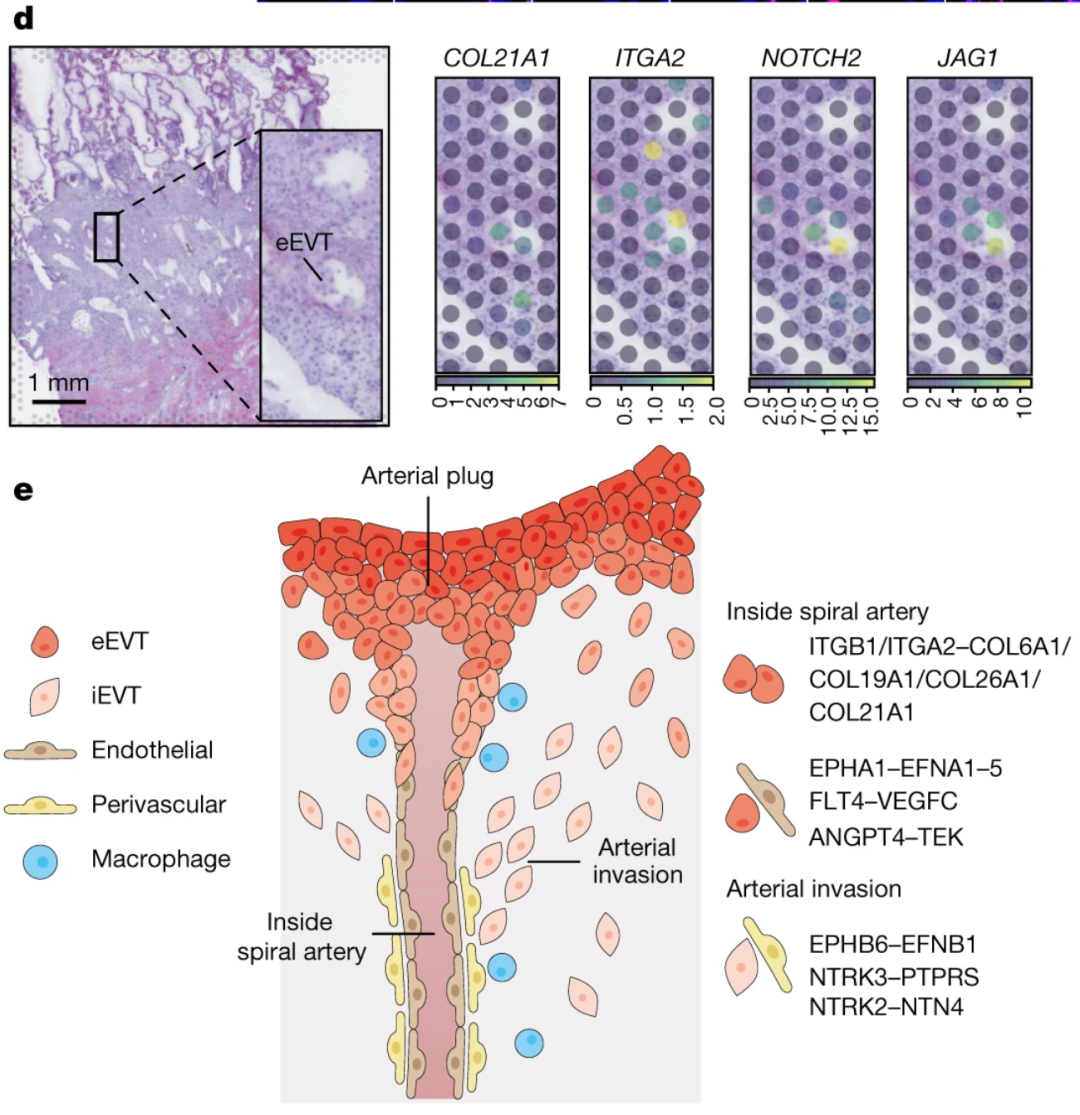
Arutyunyan���������е�ͼ5d,e��d. ͼ����ʾ��P13������֯�Ĵ�������Ƭ��Visium�ռ�ת¼��ѧ�����еĽ���������ϸ��״̬�Ŀռ�λ�ø�������������λ������չ����ͼ1d�еļ�ͷ��ʾ�����ݵ����ɫ��ʾcell2location�������ϸ��״̬�ܶȣ���Visium���ݵ����ض�ϸ��״̬��ϸ������e. �����������ڵ���������ʾ��ͼ��ͻ����ʾ��Ѫ����ϸ��(PV)-iEVT����Ƥϸ��-eEVT�Լ�eEVT-eEVT֮�����������á�ͼƬ��Դ��Arutyunyan A, et al. Spatial multiomics map of trophoblast development in early pregnancy. Nature 616: 143�C151 (2023). doi: 10.1038/s41586-023-05869-0. (CC BY 4.0)
���Ƕ���������ͷ�����˽�Ÿո���
��Ů�Խ����Ķ��������������кܶණ����Ҫ�˽⡣��������ѧ��������ȡ�ó������������Ӧ�ø߷ֱ��ʵĵ�ϸ���Ϳռ乤�ߣ����Ƴ�����ɹ���ֳ������ض�ϸ�����͡�ϸ����ϵ���ź�ͨ·��
�����Ƕ���ֳ��֯�Ļ����˽�һֱ�ͺ����������Щ�¼�����Ӧ�ã������ܹ���ø������......�⽫��Ů�Խ����������Ӱ�졣��
Roser Vento-Tormo��ʿ
Wellcome Sanger�о���ϸ���Ŵ�ѧ�ŶӸ�����
��Щ���������������ڣ����籾�о���ʾ��Ҳ�����������ڣ����һƪ�����ڡ�Clinical and Translational Medicine���ϵ��������õ�ϸ���Ϳռ�ת¼��ѧ����������������ӹ�������֯�����߾��ۣ������������յ��������֢����(6)��

������Щ�Ŷ�Ϊ�ٽ�Ů�Խ����Լ��������Ľ����ͽ������������о����ף����DZ�ʾף�ء�
�ο����ף�
1. Levine N. Five things we know about the placenta��and a few we wish we did. Cedars Sinai Discoveries Magazine (Feb 12, 2021).
2. Arutyunyan A, et al. Spatial multiomics map of trophoblast development in early pregnancy. Nature 616: 143�C151 (2023). doi: 10.1038/s41586-023-05869-0
3. Brosens I, et al. The ��great obstetrical syndromes�� are associated with disorders of deep placentation. Am J Obstet Gynecol 204: 193�C201 (2011). doi: 10.1016/j.ajog.2010.08.009
4. https://www.mayoclinic.org/diseases-conditions/preeclampsia/symptoms-causes/syc-20355745
5. Kretschmer M, et al. Matrix stiffness regulates Notch signaling activity in endothelial cells. J Cell Sci 136: jcs260442 (2023). doi: 10.1242/jcs.260442
6. Ji K, et al. Integrating single-cell RNA sequencing with spatial transcriptomics reveals an immune landscape of human myometrium during labour. Clin Transl Med 13: e1234 (2023). doi: 10.1002/ctm2.123