
-

生物通官微
陪你抓住生命科技
跳动的脉搏
TET2-MBD6-NSUN2轴:染色质结构调控与白血病发生的新机制及其治疗潜力
【字体: 大 中 小 】 时间:2025年01月24日 来源:Signal Transduction and Targeted Therapy 40.8
编辑推荐:
本研究首次揭示TET2通过调控RNA m5C氧化影响染色质开放状态的新机制。研究人员发现TET2突变导致MBD6异常结合m5C,通过BAP1/PR-DUB复合物去泛素化H2AK119ub,形成开放染色质框架并促进白血病发生。该发现为TET2突变血液肿瘤提供了精准治疗靶点。
在血液系统恶性肿瘤的研究领域,表观遗传调控异常一直是科学家们关注的焦点。其中,TET2(Ten-Eleven Translocation 2)作为重要的表观遗传修饰酶,其突变在12-34%的髓系恶性肿瘤中被检出,与DNA低甲基化和开放染色质框架密切相关。然而,TET2如何通过RNA修饰调控染色质状态的分子机制始终是未解之谜。更棘手的是,携带TET2突变的急性白血病患者常表现出化疗抵抗和不良预后,这促使科学家们必须深入探索其背后的生物学基础。
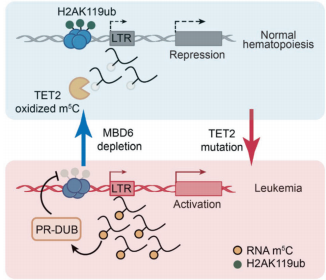
来自Nature的最新研究首次揭示了TET2通过调控RNA m5C(5-甲基胞嘧啶)氧化影响染色质开放状态的全新机制。研究人员发现,在正常造血过程中,TET2通过氧化m5C抑制MBD6(甲基CpG结合蛋白6)的结合,维持组蛋白H2AK119ub的泛素化状态,从而保持染色质的适当紧密结构。然而当TET2发生突变时,MBD6将不受抑制地结合m5C修饰的逆转录转座子RNA,招募BAP1/PR-DUB复合物去除H2AK119ub标记,导致染色质开放和促癌基因的异常表达。
研究团队采用了多种关键技术方法:通过CRISPR-Cas9基因编辑构建TET2敲除模型;采用RNA免疫沉淀测序(RIP-seq)分析m5C修饰RNA的分布;运用染色质可及性测定(ATAC-seq)评估染色质状态变化;并利用人源AML细胞系(如K562)和原代造血干细胞进行功能验证。
研究结果主要包含以下重要发现:
TET2-MBD6相互作用调控机制:实验证实TET2通过氧化m5C阻止MBD6结合,而TET2突变导致MBD6异常激活BAP1/PR-DUB通路。
染色质状态动态变化:NSUN2(RNA甲基转移酶)敲除与TET2过表达均能诱导染色质紧缩,而TET2缺失则显著增加染色质可及性。
白血病细胞生长调控:在TET2突变AML模型中,靶向NSUN2或MBD6可显著抑制细胞增殖,效果类似于NSUN2敲除。
组蛋白修饰异常:TET2敲除导致H2AK119ub水平升高,激活白血病起始相关基因表达谱。
这项发表于《Signal Transduction and Targeted Therapy》的研究具有多重重要意义:首先,它首次阐明RNA m5C氧化在染色质结构调控中的核心作用,拓展了表观遗传调控的认知边界;其次,发现NSUN2-TET2-MBD6-BAP1/PR-DUB这一全新信号轴,为理解TET2突变白血病的发病机制提供了分子基础;最重要的是,该研究鉴定出MBD6和NSUN2作为潜在治疗靶点,为开发针对TET2突变血液肿瘤的精准疗法指明了方向。Wolfram C. M. Dempke和Klaus Fenchel在文中特别强调,这一发现可能改变当前对白血病表观遗传治疗的策略,未来或可开发特异性抑制MBD6-RNA相互作用的小分子药物,为临床难治性病例带来新希望。
 生物通微信公众号
生物通微信公众号
知名企业招聘