
-

生物通官微
陪你抓住生命科技
跳动的脉搏
中国慢性肉芽肿病患者CYBB基因突变谱解析:IFN-γ治疗应答预测新策略
【字体: 大 中 小 】 时间:2025年10月01日 来源:Journal of Clinical Immunology 5.7
编辑推荐:
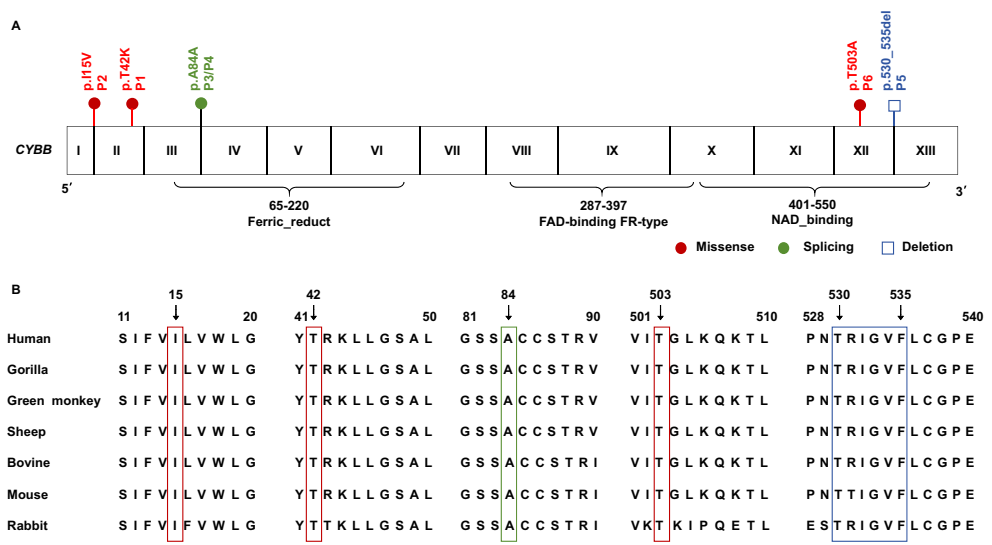
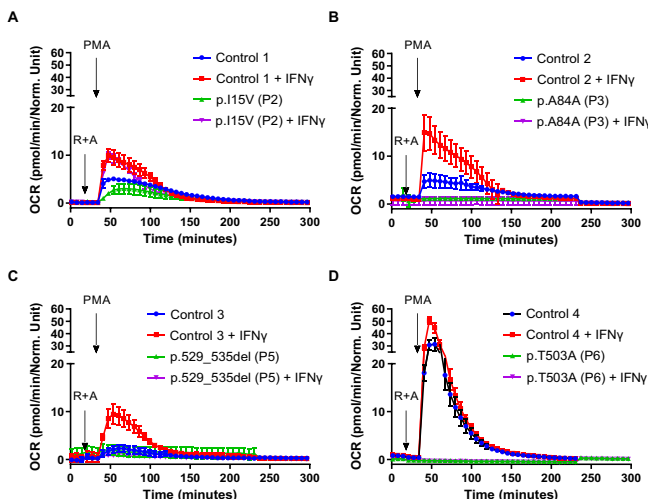
本研究聚焦慢性肉芽肿病(CGD)这一原发性免疫缺陷病,针对中国人群中CYBB基因突变导致NADPH氧化酶功能缺陷的机制展开深入探索。研究人员通过对5个无亲缘关系中国家庭的6例患者进行基因测序与功能验证,发现包括c.1507A>G(p.T503A)和c.1587_1605del(p.529_535del)在内的两种新突变,并首次证实 synonymous突变c.252G>T(p.A84A)实际引起外显子跳跃。更重要的是,研究通过中性粒细胞呼吸爆发实验证明IFN-γ仅能挽救p.I15V突变者的功能缺陷,为临床精准预测IFN-γ疗效提供了关键实验依据。


 生物通微信公众号
生物通微信公众号
知名企业招聘