
-

生物通官微
陪你抓住生命科技
跳动的脉搏
无需减重即可实现糖尿病前期缓解:2型糖尿病预防的新路径
【字体: 大 中 小 】 时间:2025年10月01日 来源:Nature Medicine 50
编辑推荐:
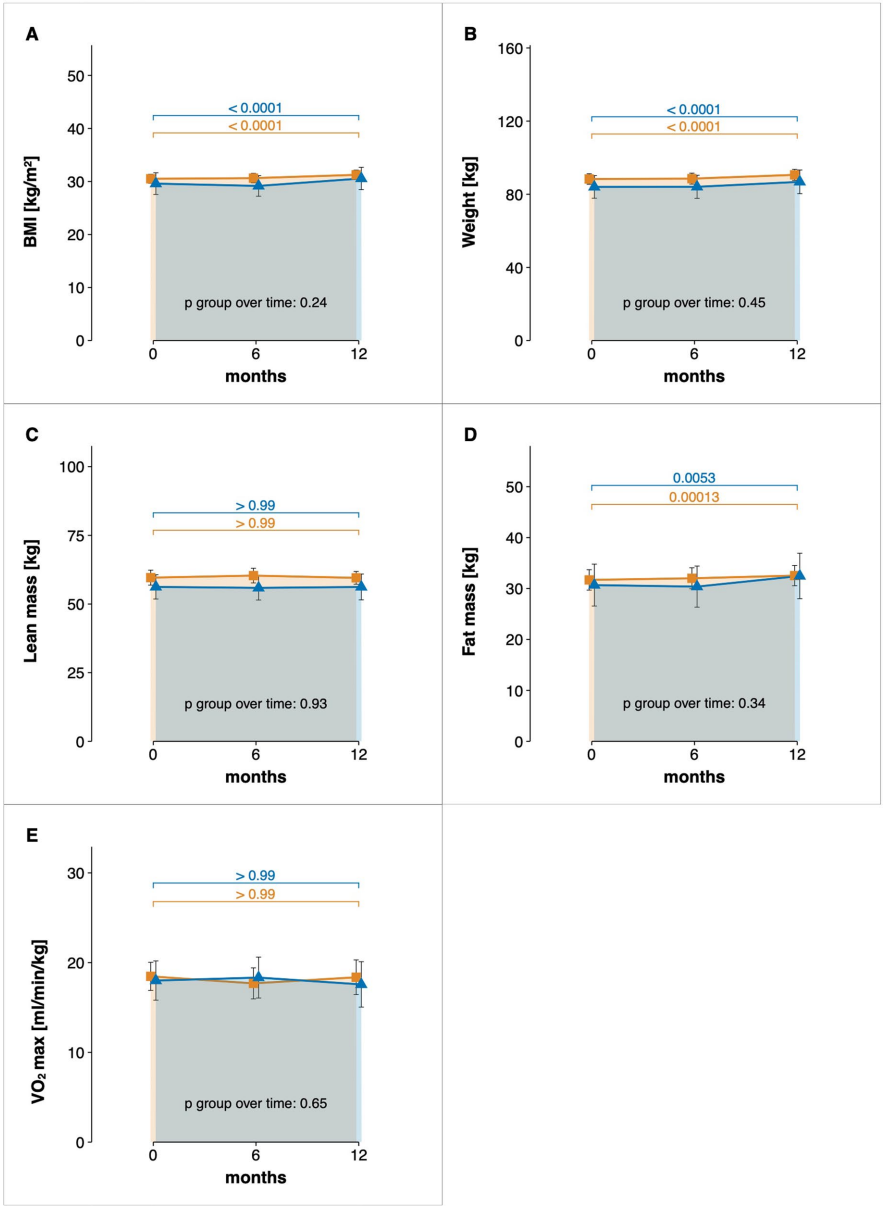
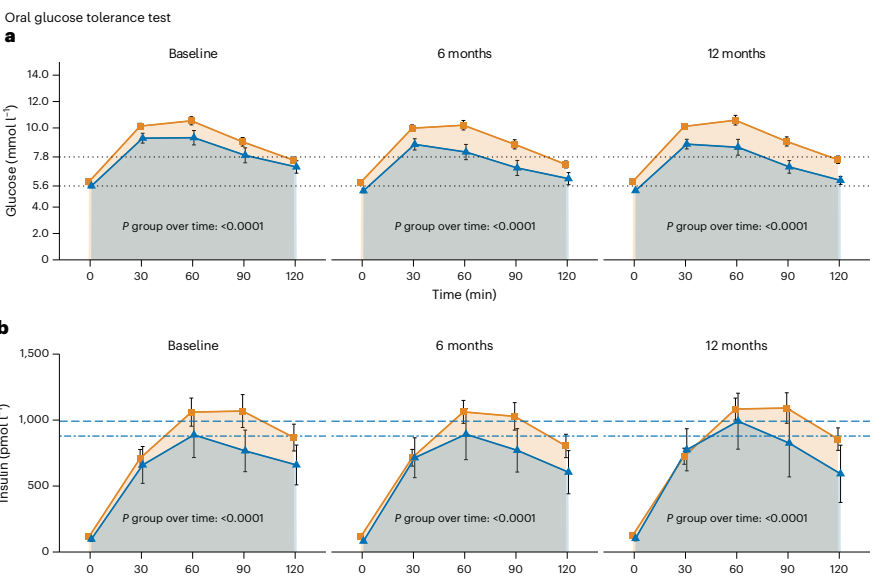
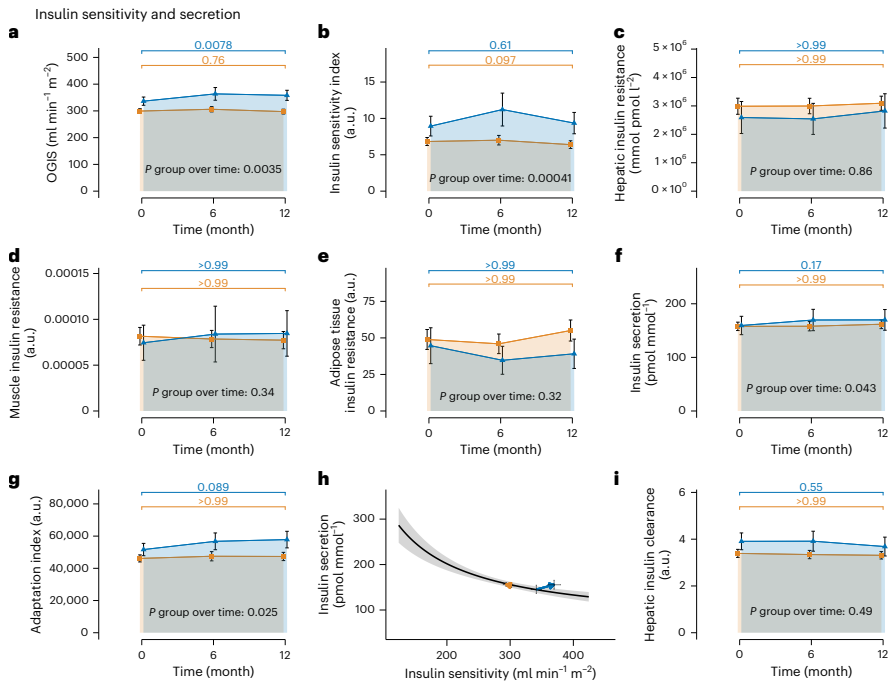
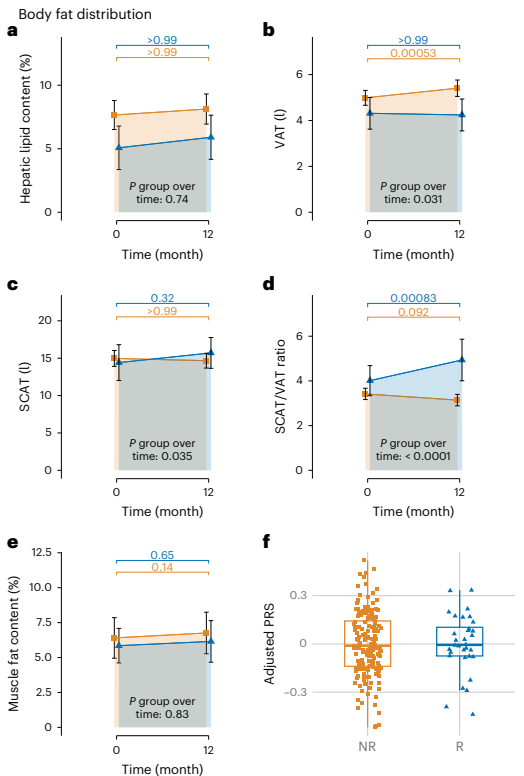
语 为解决传统2型糖尿病(T2D)预防策略过度依赖减重目标的局限性,研究人员通过前瞻性多中心干预研究(PLIS)和美国糖尿病预防计划(DPP)验证,发现糖尿病前期缓解(定义为血糖指标恢复正常)可通过改善胰岛素敏感性、β细胞功能及GLP-1敏感性独立于体重变化实现,且与内脏脂肪向皮下脂肪的转移密切相关。该研究强调将血糖目标纳入临床指南对优化T2D精准预防的意义。
 生物通微信公众号
生物通微信公众号
知名企业招聘