
-

生物通官微
陪你抓住生命科技
跳动的脉搏
核苷修饰与离子化脂质组成的协同效应对mRNA疫苗翻译效率及免疫反应的调控机制研究
【字体: 大 中 小 】 时间:2025年10月01日 来源:npj Vaccines 6.5
编辑推荐:
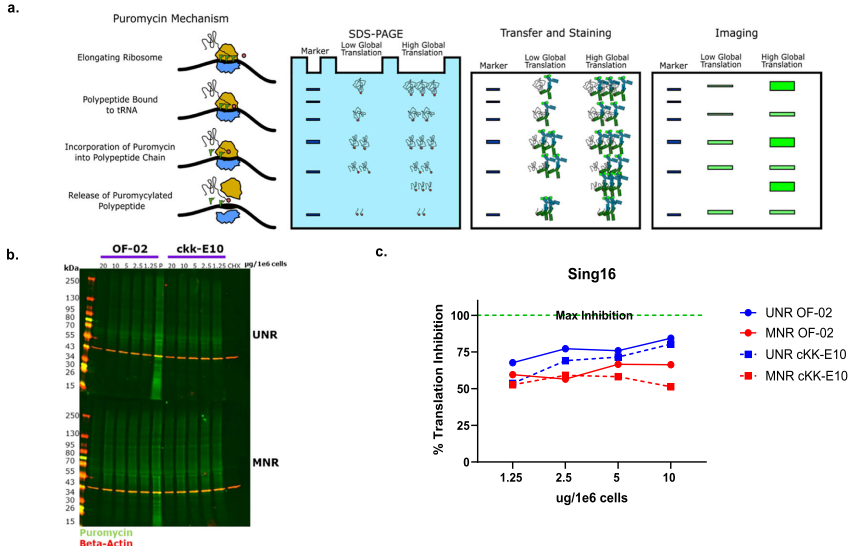
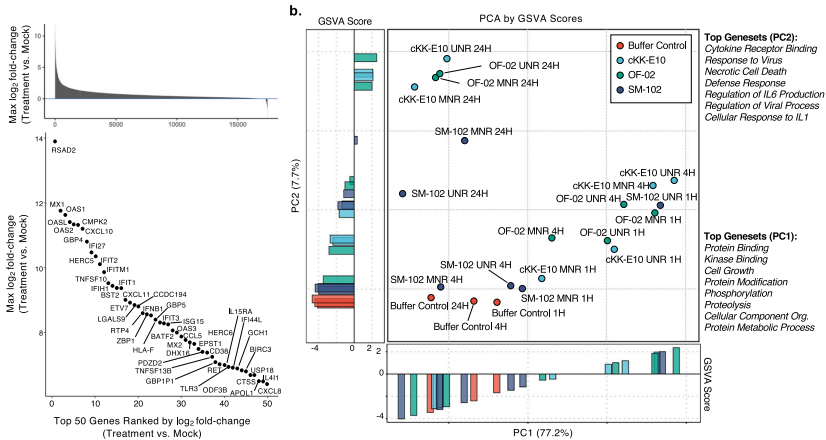
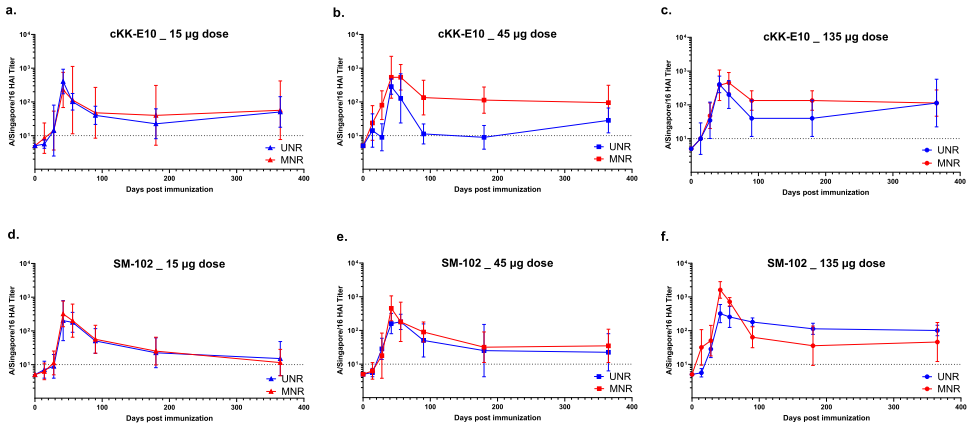
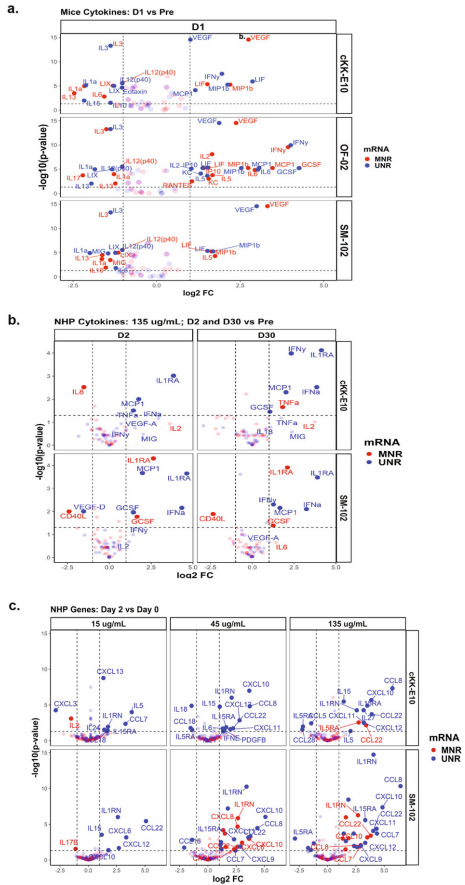
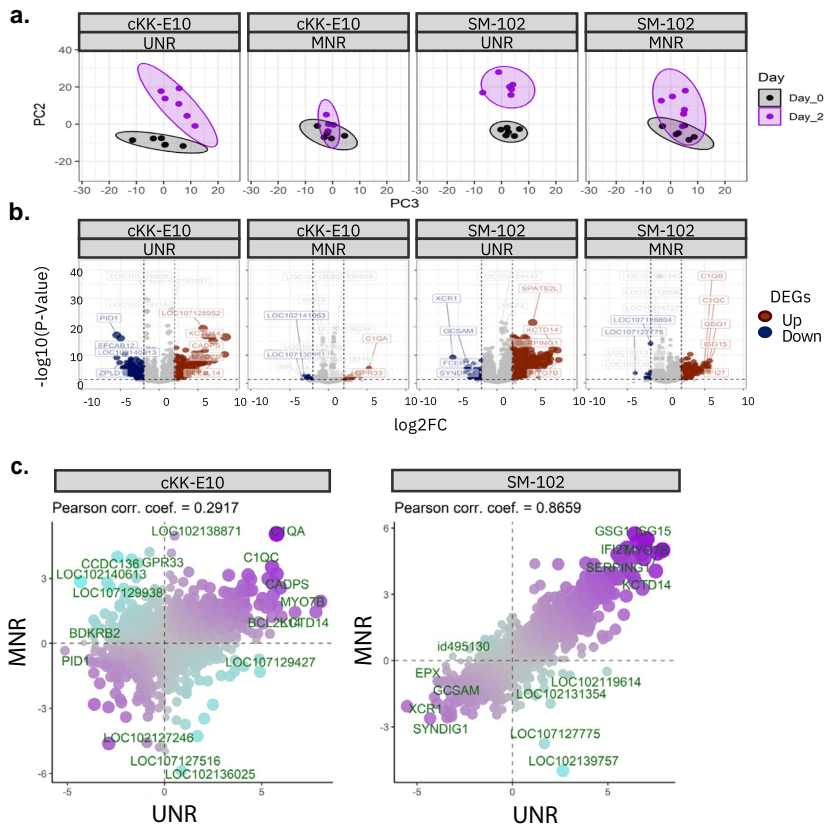
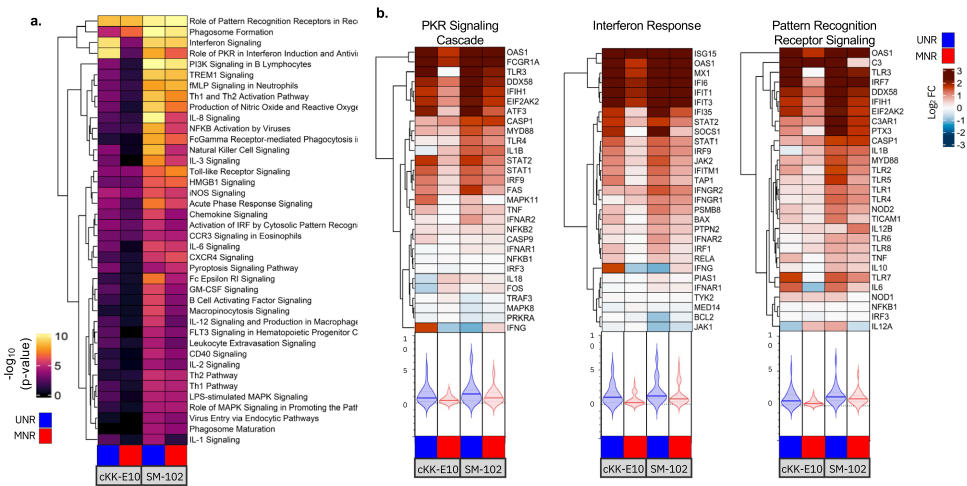
本研究针对mRNA疫苗中核苷修饰(m1ψ)与离子化脂质(LNP)组成对翻译效率、先天免疫激活及免疫原性的协同影响机制展开研究。通过体外实验和小鼠/NHP模型证实,m1ψ修饰可增强蛋白表达并降低dsRNA介导的免疫识别,而LNP组成(OF-02/cKK-E10/SM-102)显著影响干扰素信号通路激活与抗体持久性。该研究为优化mRNA疫苗安全性与有效性提供了关键策略。



 生物通微信公众号
生物通微信公众号
知名企业招聘