
-

生物通官微
陪你抓住生命科技
跳动的脉搏
TEAD3通过GAS6-TYRO3轴重编程丙酸代谢驱动黑色素瘤进展的机制研究
【字体: 大 中 小 】 时间:2025年10月02日 来源:Journal of Experimental & Clinical Cancer Research 12.8
编辑推荐:
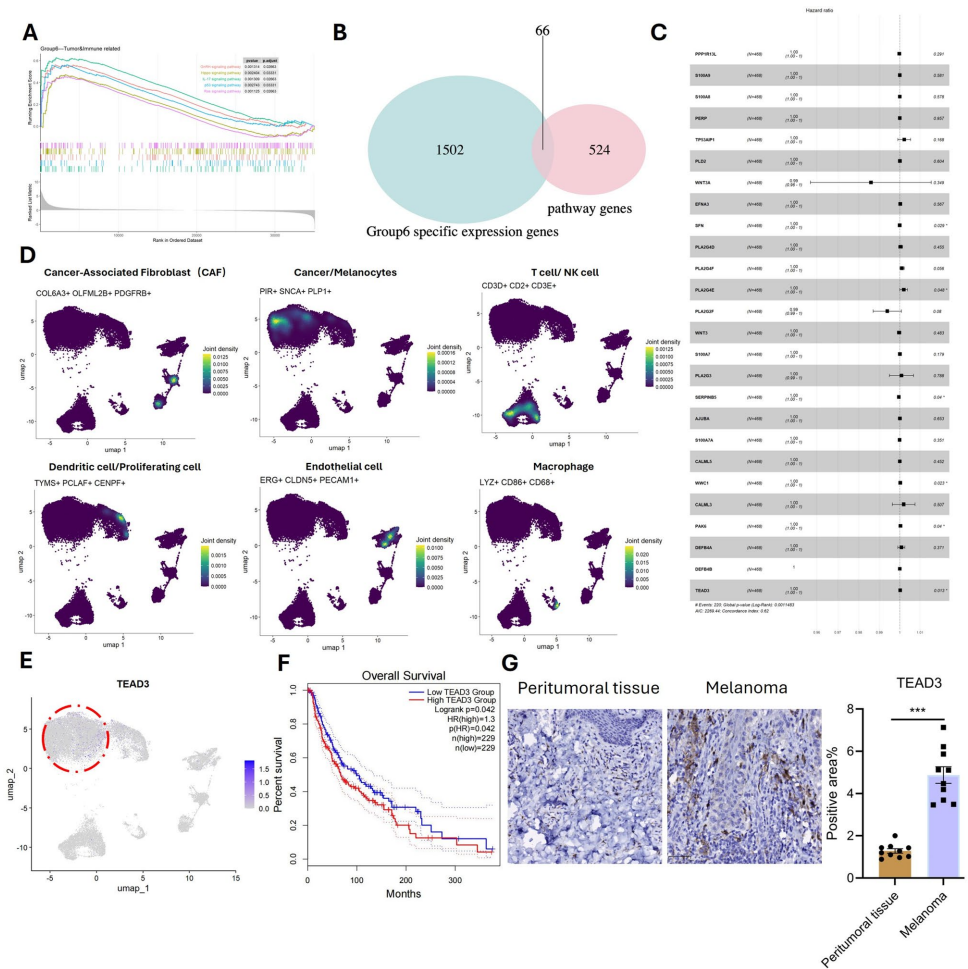
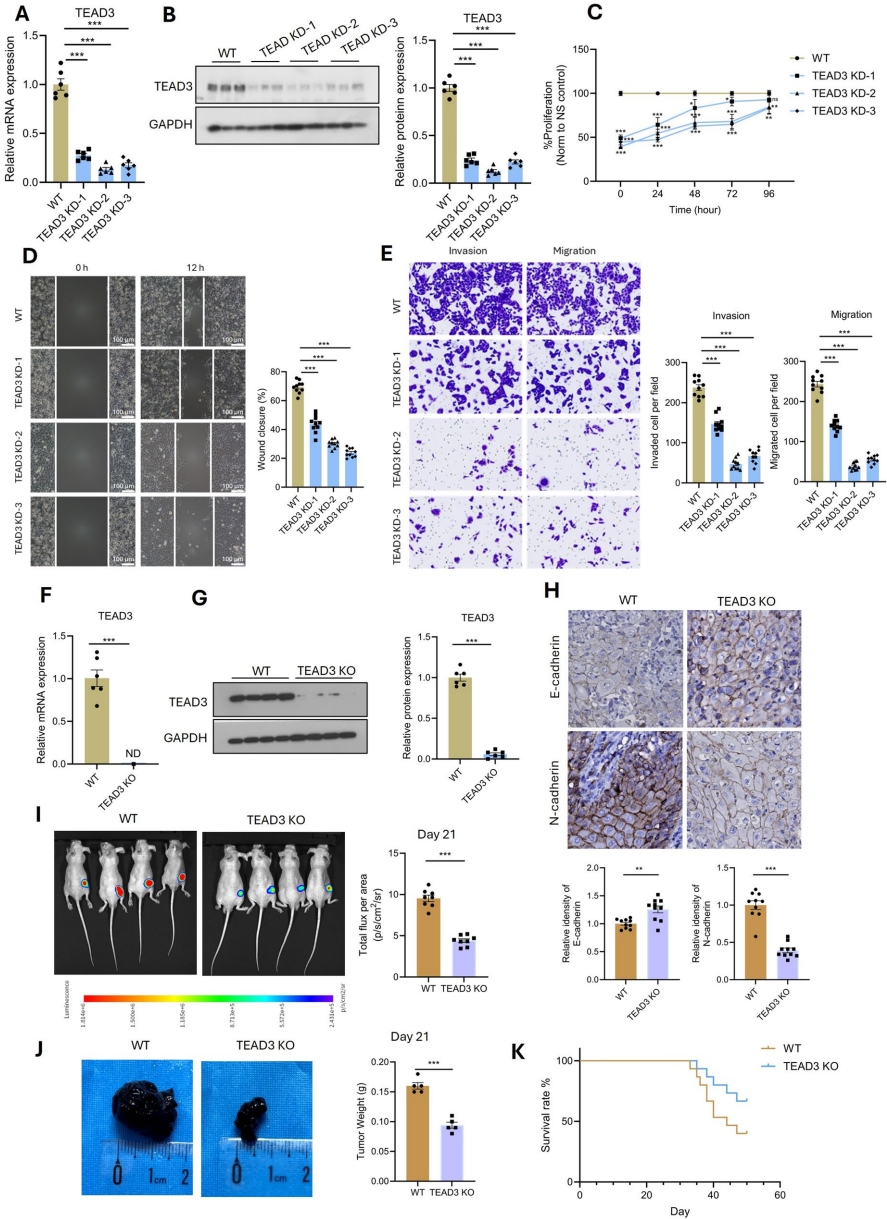
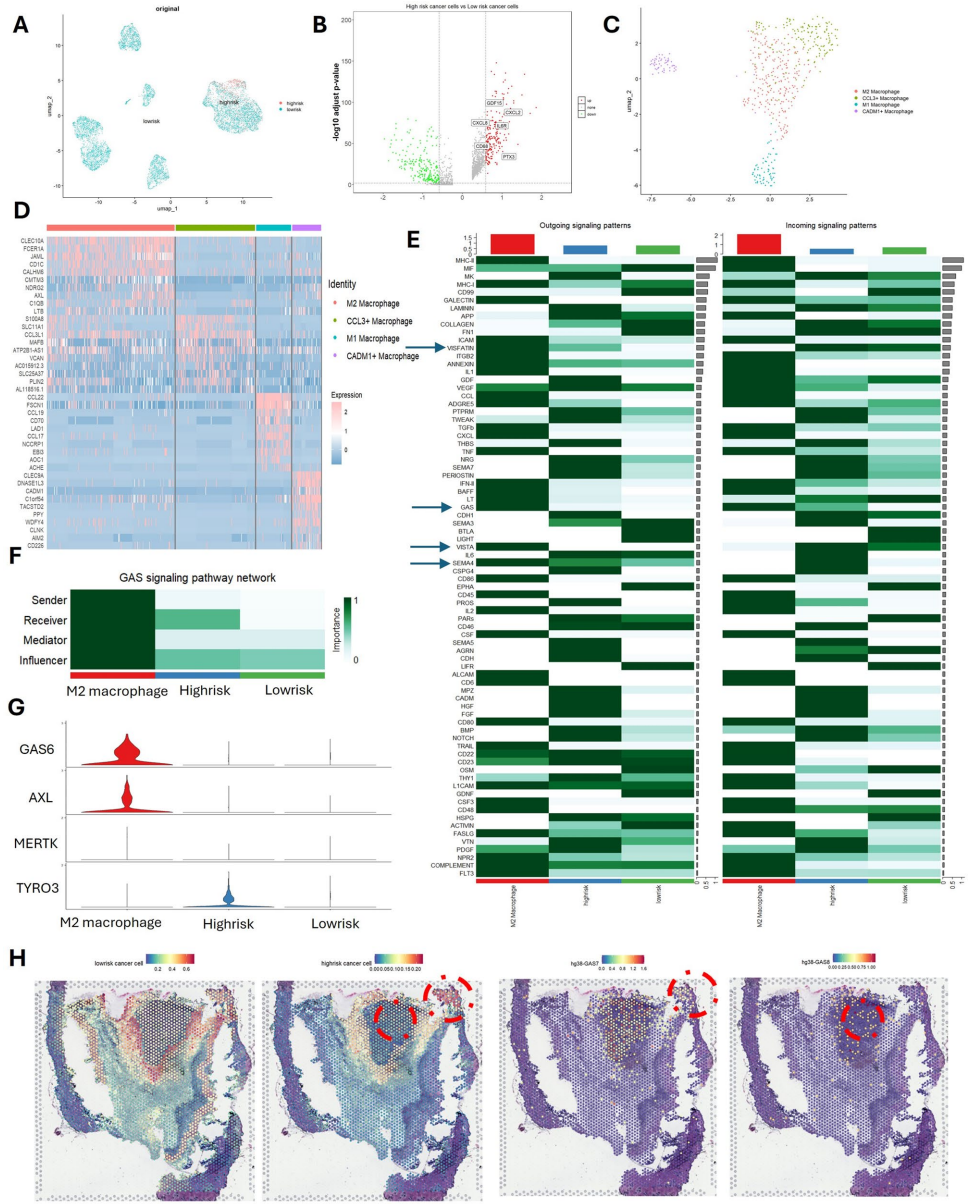
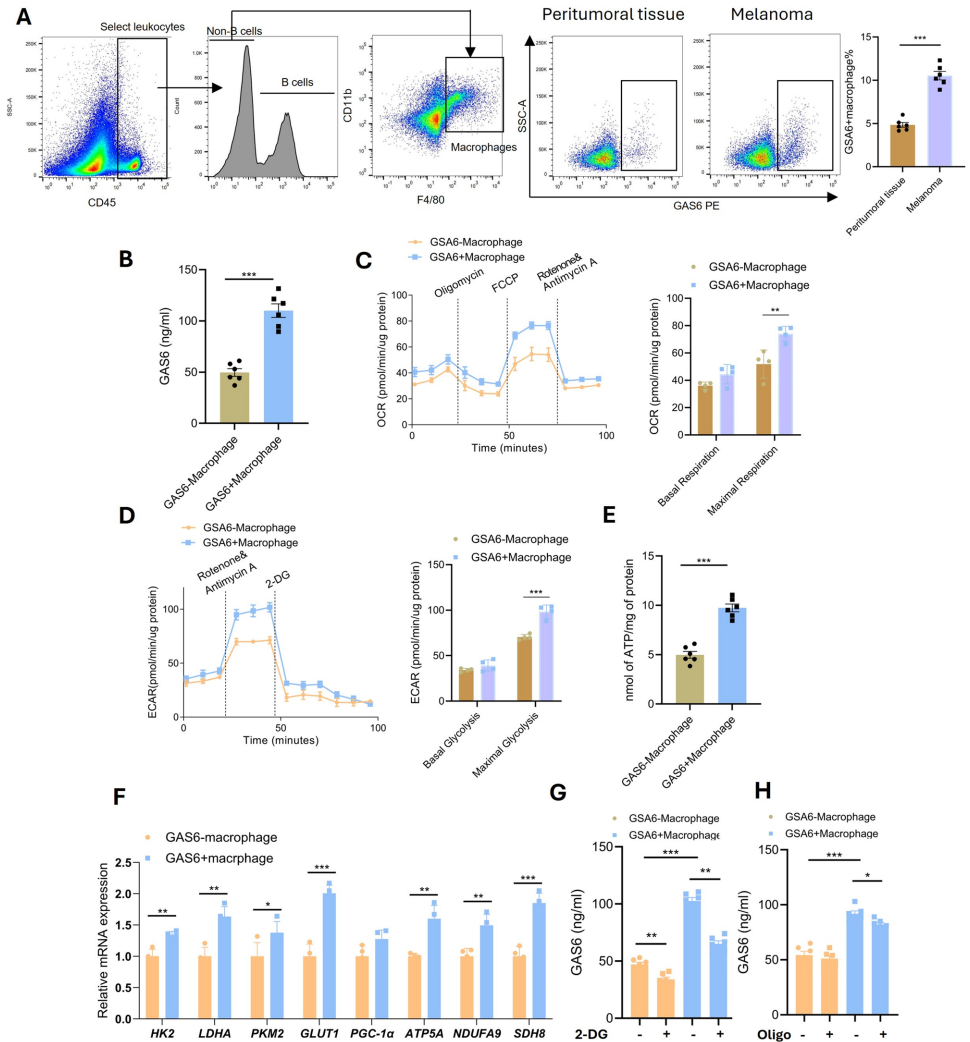
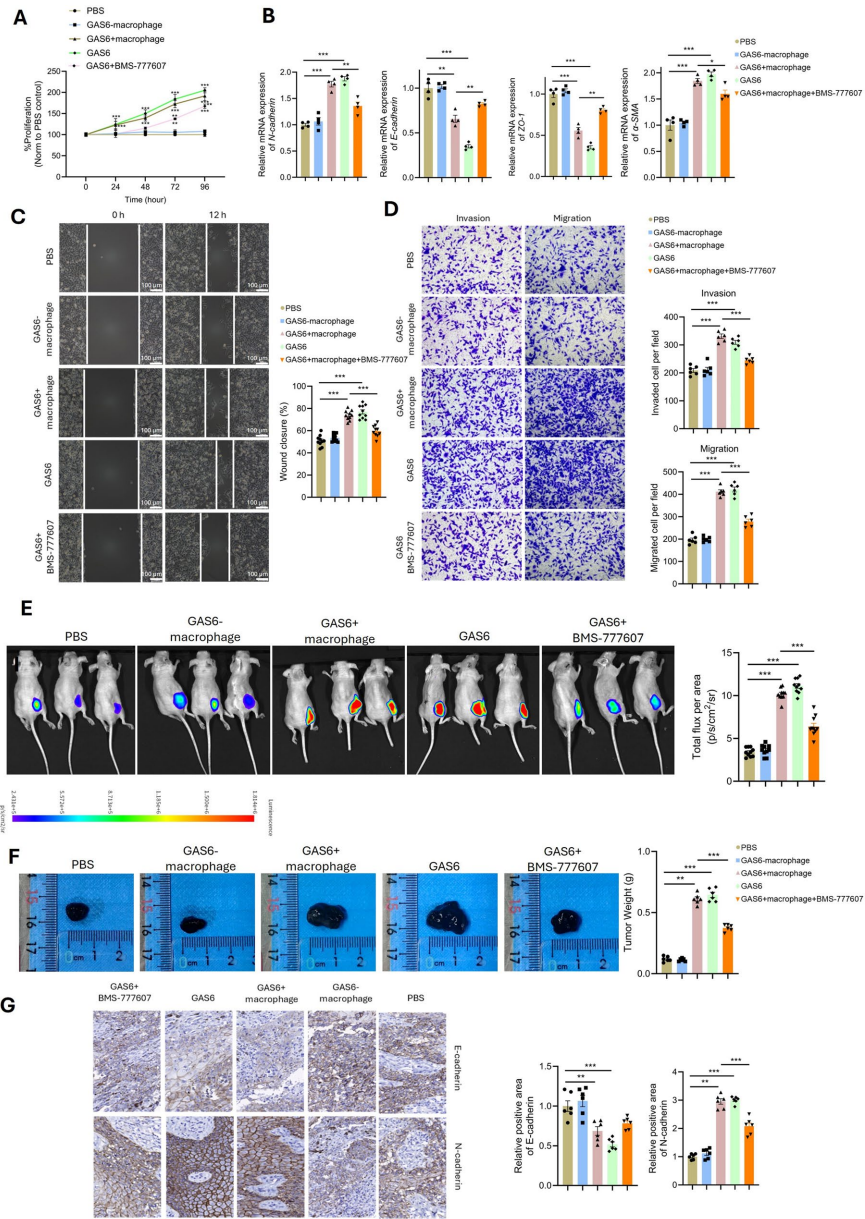
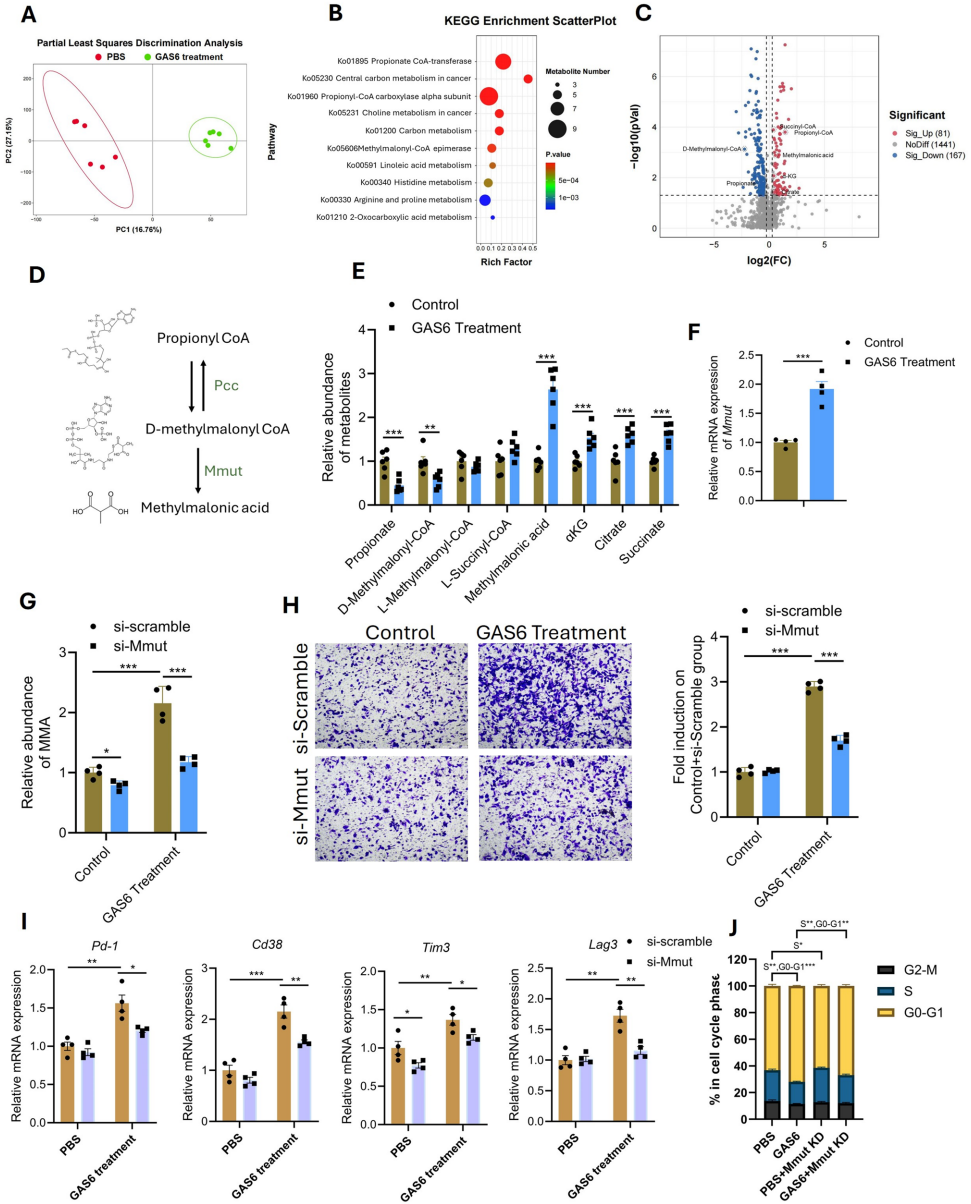
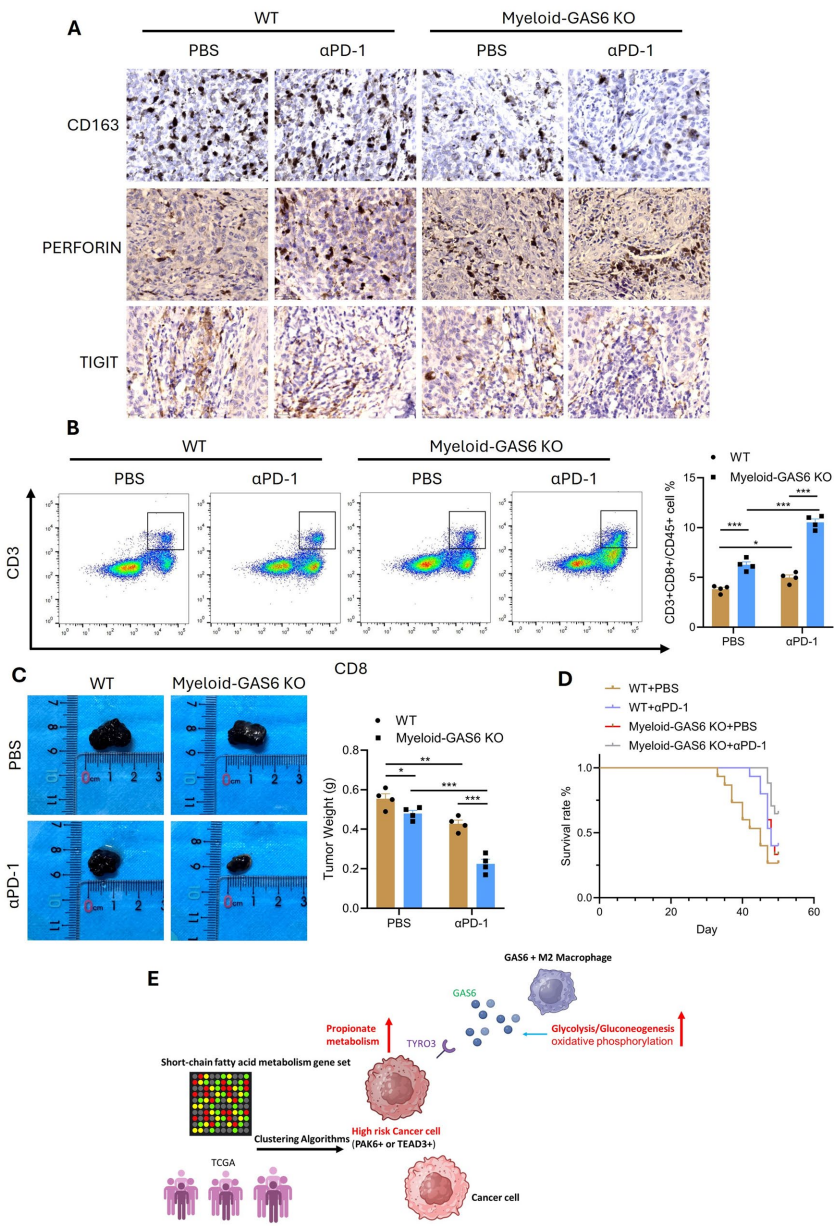
本研究针对黑色素瘤异质性及免疫治疗抵抗难题,通过多组学分析发现高危亚型(Group 6)存在短链脂肪酸代谢紊乱,首次揭示TEAD3high肿瘤细胞通过GAS6-TYRO3配体-受体轴与M2巨噬细胞互作,诱导Mmut介导的甲基丙二酸积累促进肿瘤进展。髓系特异性GAS6敲除可增强抗PD-1疗效,为靶向代谢-免疫轴联合治疗提供新策略。
 生物通微信公众号
生物通微信公众号
知名企业招聘