
-

����ͨ��
����ץס�����Ƽ�
����������
ɳ����ԭ��ͨ����������ϸ����л�ر�̺������幦�ܵ���ԭ���Թ�����Ƥϸ������Ӧ��Ļ����о�
�����壺 �� �� С �� ʱ�䣺2025��10��10�� ��Դ��World Journal of Microbiology and Biotechnology 4
�༭�Ƽ���
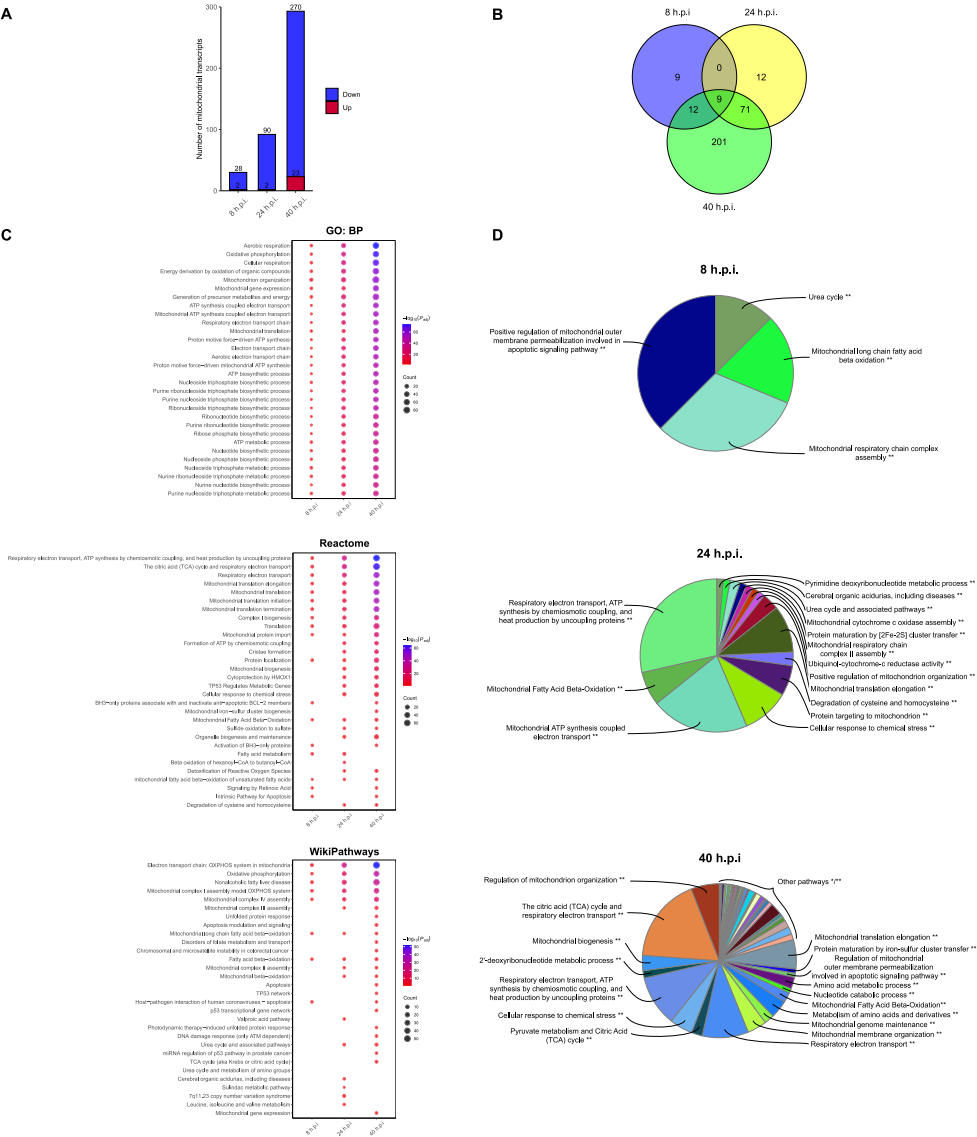
���������Ƽ���Ϊ̽��ɳ����ԭ�壨Chlamydia trachomatis����Ⱦ������ϸ����л��Ӱ�죬�о���Ա����ԭ���Թ�����Ƥϸ��ģ�Ϳ�չ����ѧ�������о����֣���Ⱦ�����������������幦�ܺ�������ѭ����TCA cycle���������������ữ��OXPHOS�����ǽͽ⣬��������֢�ź�ͨ·�����о���ʾ������ͨ����л�ر�����Ʋ�ԭ����ֳ���»��ƣ�Ϊ�����лͨ·�Ŀ���Ⱦ�����ṩ�������ݡ�




 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
֪����ҵ��Ƹ