
-

生物通官微
陪你抓住生命科技
跳动的脉搏
循环肿瘤细胞基因组多样性与BCL9L突变状态预测转移性结直肠癌总生存期
【字体: 大 中 小 】 时间:2025年10月10日 来源:Cellular Oncology 4.8
编辑推荐:
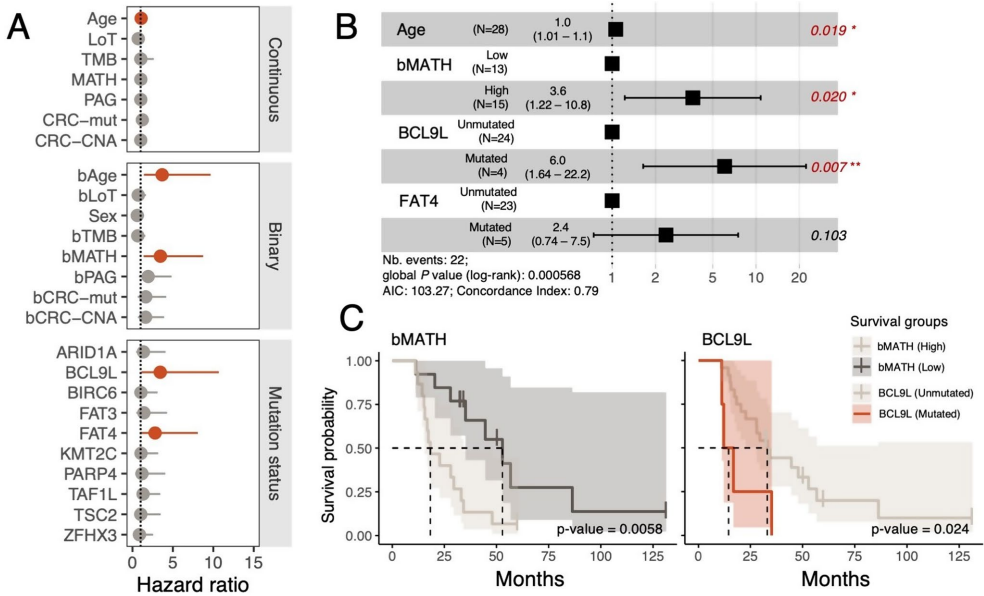
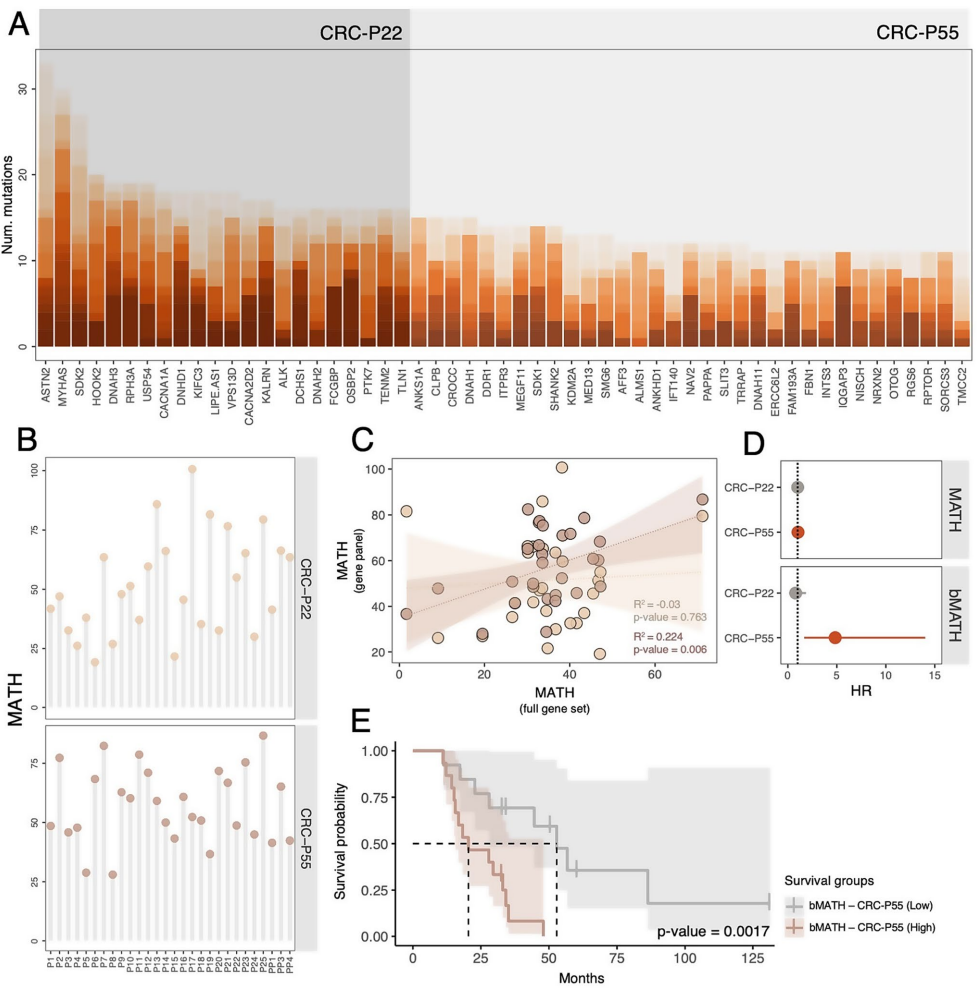
为解决转移性结直肠癌(mCRC)缺乏非侵入性生物标志物的临床难题,研究人员通过循环肿瘤细胞(CTCs)全外显子测序开展基因组多样性研究,发现高MATH评分(突变等位基因肿瘤异质性评分)和BCL9L基因非沉默突变与患者总生存期缩短显著相关,为mCRC预后分层提供了新型液体活检策略。


 生物通微信公众号
生物通微信公众号
知名企业招聘