
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:模型知情药物开发中药物计量学作用的范围综述
【字体: 大 中 小 】 时间:2025年10月18日 来源:Journal of Pharmacokinetics and Pharmacodynamics 2.8
编辑推荐:
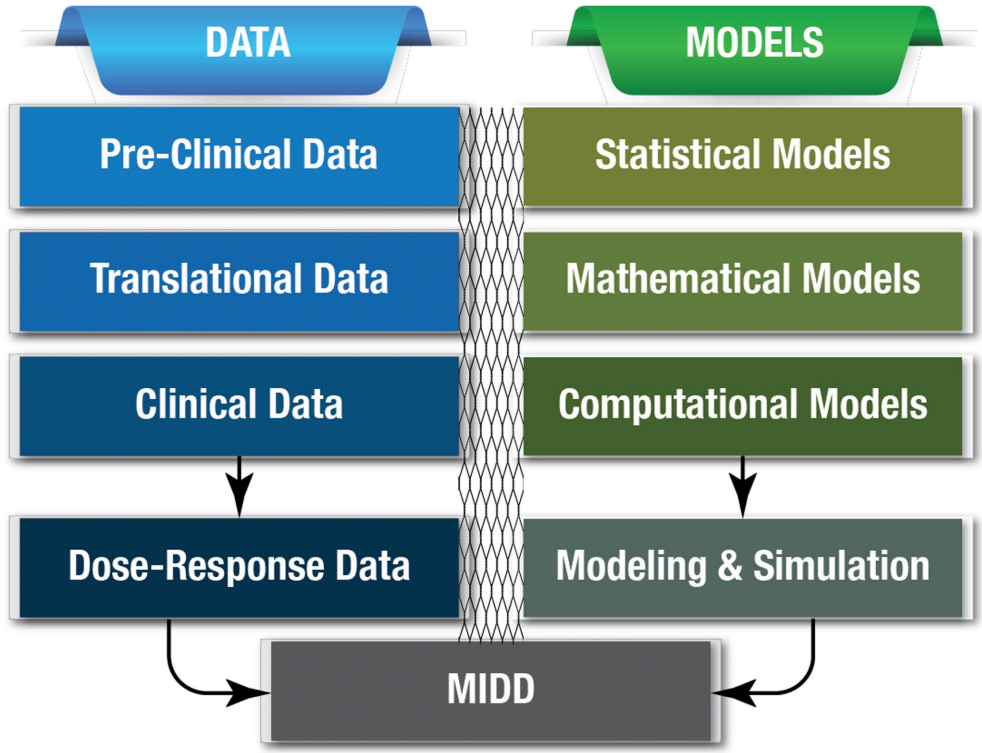
本综述系统梳理了模型知情药物开发(MIDD)框架,重点聚焦药物计量学(Pharmacometrics)在其中的核心作用。文章详细解读了国际人用药品注册技术协调会(ICH)M15 MIDD指南草案,并通过涵盖单克隆抗体(如atezolizumab、nivolumab)、小分子药物(如brexpiprazole、mavacamten)及长效注射剂(如aripiprazole lauroxil)等多个治疗领域的案例研究,生动展示了MIDD如何通过定量建模与仿真(M&S)整合非临床与临床数据,优化给药方案、支持儿科外推、加速罕见病药物审批,从而显著提升药物研发效率和监管决策的科学性。


 生物通微信公众号
生物通微信公众号
知名企业招聘