
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:哮喘的免疫疗法
《Cellular & Molecular Immunology》:Immunotherapy for asthma
【字体: 大 中 小 】 时间:2025年10月28日 来源:Cellular & Molecular Immunology 19.8
编辑推荐:
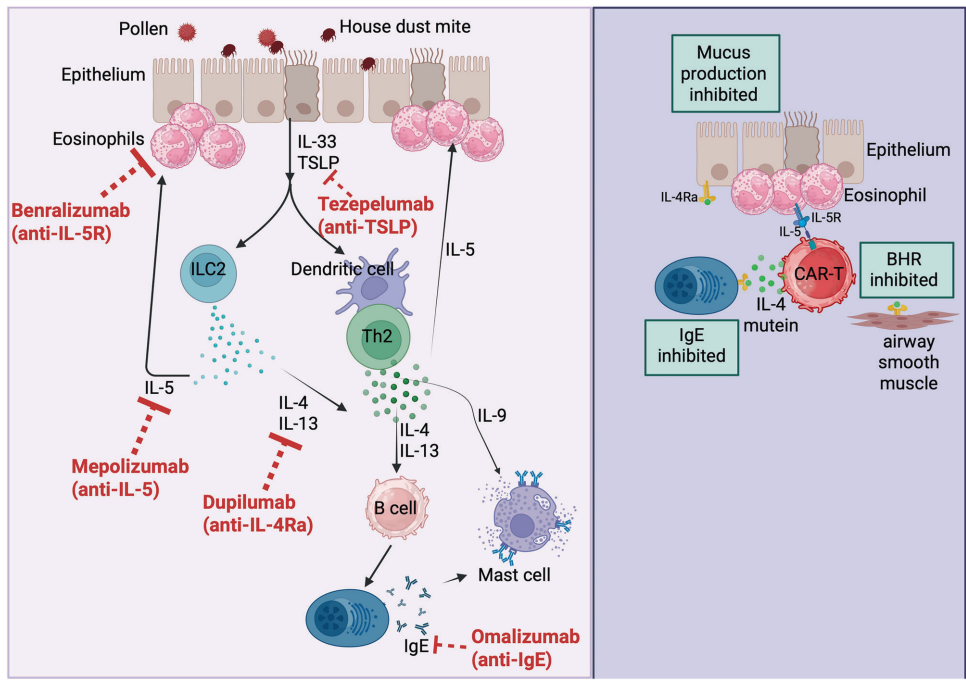
本综述系统阐述了哮喘的不同内型分型(T2high和T2low)及其免疫学机制,并全面梳理了过敏原特异性免疫疗法(AIT)和各类生物制剂(如抗IgE、抗IL-5/5R、抗IL-4Rα、抗TSLP等)的作用机制与临床疗效。文章还展望了CAR-T细胞疗法等新兴策略,强调了基于内型的个体化精准治疗是未来哮喘管理的发展方向,为改善难治性哮喘患者的预后提供了重要见解。


 生物通微信公众号
生物通微信公众号