
-

生物通官微
陪你抓住生命科技
跳动的脉搏
帕金森病生物诊断新纪元:机遇与挑战并存
《Cell Death & Disease》:Are we ready for a biological diagnosis of Parkinson’s Disease?
【字体: 大 中 小 】 时间:2025年11月08日 来源:Cell Death & Disease 9.6
编辑推荐:
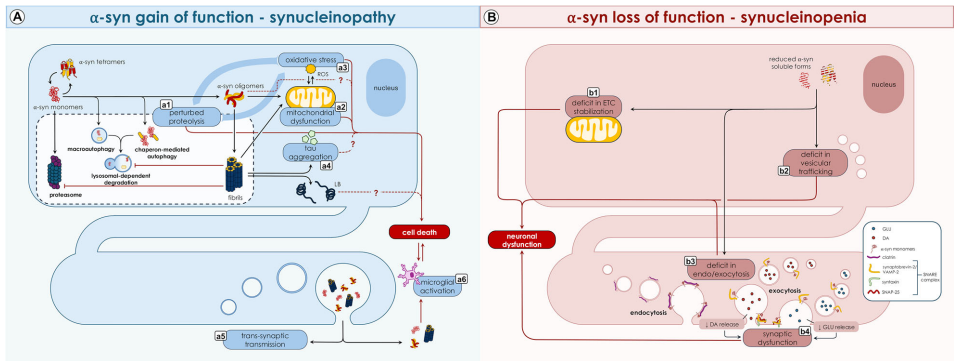
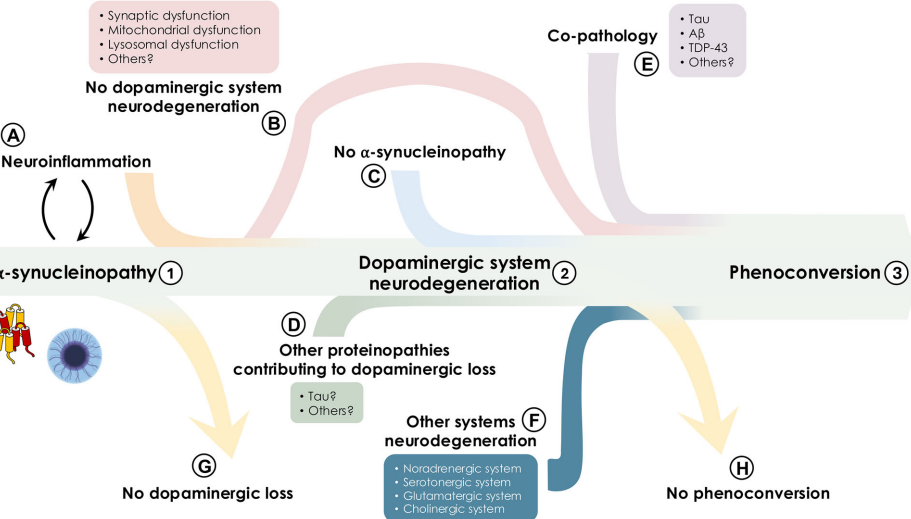
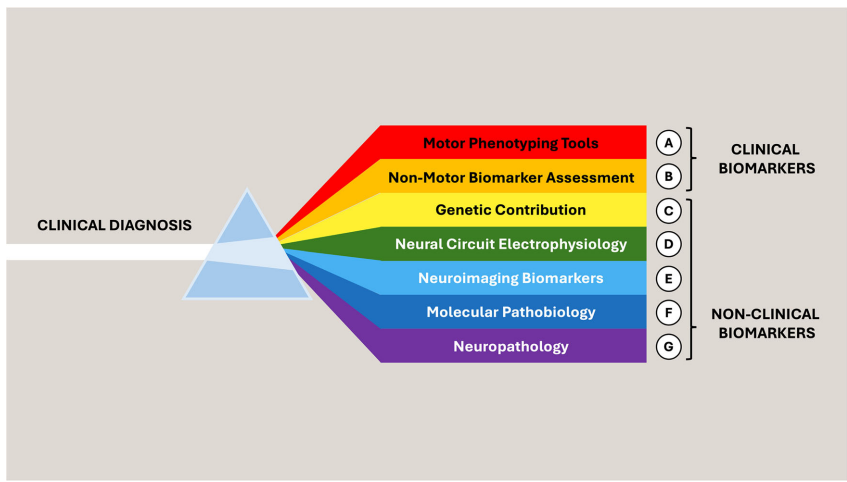
【编辑推荐】本文聚焦帕金森病(PD)诊断范式从临床向生物学的重大转变,深入剖析NSD-ISS与SynNeurGe两大生物诊断框架的科学基础与临床应用挑战。研究人员通过系统回顾PD诊断标准演变历程,揭示α-突触核蛋白(a-syn)生物标记物检测技术的突破性进展,同时指出当前生物定义在解释疾病复杂性、技术可及性和伦理层面存在的显著局限。这项研究为PD精准医疗发展提供了关键的路标,强调在推进生物诊断的同时必须正视其现实约束。
 生物通微信公众号
生物通微信公众号