人类多能干细胞跨个体基因调控的基因组规模单细胞CRISPRi图谱
《Cell Genomics》:A genome-scale single-cell CRISPRi map of trans gene regulation across human pluripotent stem cell lines
【字体:
大
中
小
】
时间:2025年12月02日
来源:Cell Genomics 9
编辑推荐:
本刊推荐:为解析人类基因调控网络,研究人员开展了首个跨多个遗传背景的基因组规模CRISPR干扰筛选,结合单细胞RNA测序技术,系统绘制了转座基因调控图谱。研究发现蛋白质复合物是缓冲遗传变异影响的关键枢纽,并揭示了遗传背景对基因扰动效应的调控作用,为疾病机制研究和精准医疗提供了重要资源。
在生命科学领域,理解基因如何调控细胞功能一直是核心挑战。随着人类基因组计划的完成,科学家们已经绘制出人类基因的完整图谱,但如何解读这本"生命天书"中的调控密码仍是未解之谜。特别是当涉及到疾病研究时,我们需要了解基因突变如何影响细胞功能,以及为什么相同的突变在不同个体中可能产生不同的效应。
近年来,诱导多能干细胞(iPSC)技术的出现为人类疾病建模带来了革命性的变化。这些细胞可以通过重编程成人细胞获得,具有分化为各种细胞类型的潜力,为研究难以获取的细胞类型(如神经元)提供了可能。然而,尽管科学家已经在iPSC中发现了数千个影响基因表达的遗传变异位点(称为表达数量性状位点,eQTL),但对于这些变异如何影响下游细胞通路和功能的调控网络,我们仍然知之甚少。
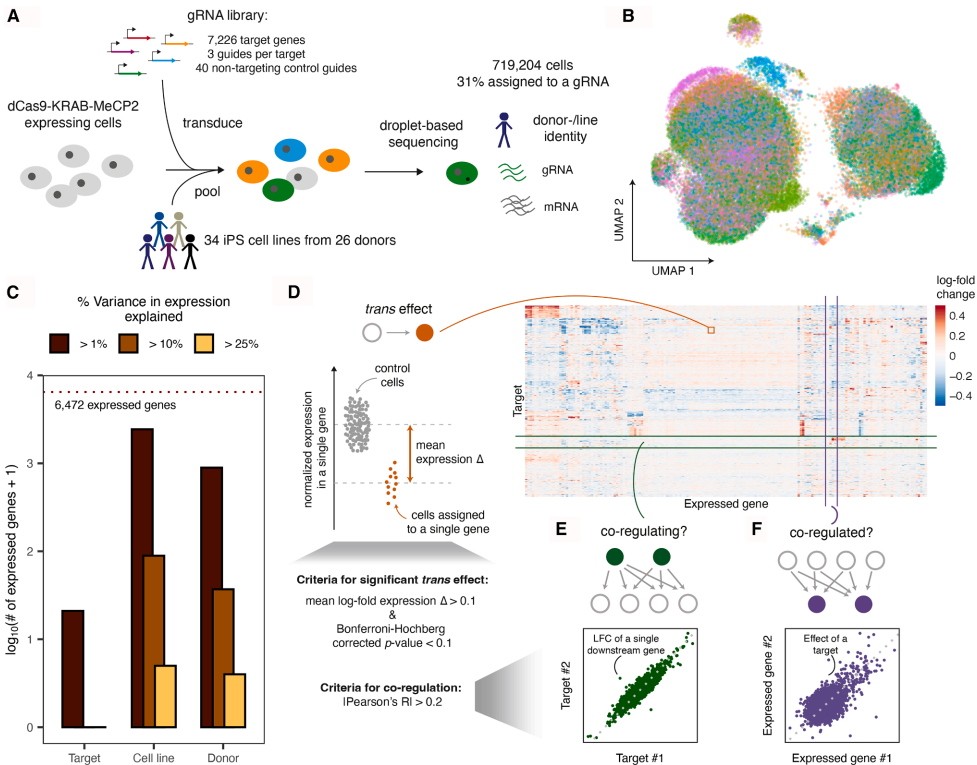
为了突破这一瓶颈,来自Wellcome Sanger研究所等机构的研究团队在《Cell Genomics》上发表了开创性研究。他们成功构建了首个跨多个健康人类遗传背景的基因组规模CRISPR干扰(CRISPRi)扰动图谱,结合单细胞RNA测序(scRNA-seq)技术,系统揭示了基因扰动对转录组的广泛影响。
研究人员采用了创新的实验设计,在34个来自26个健康供体的iPSC细胞系中靶向了7,226个基因。这些靶基因包括在iPSC或癌细胞系中显示生长缺陷的基因,以及在iPSC中高表达的基因。通过使用CRISPRi技术进行基因敲低,并利用单细胞RNA测序读取结果,研究团队成功获得了219,206个被成功分配至特定细胞系和靶向引导RNA的细胞,以及499,998个对照细胞。
研究的关键技术方法包括:基因组规模的CRISPRi筛选平台构建、多供体iPSC细胞的培养与扰动、单细胞RNA测序技术的应用、基于自然遗传变异的细胞分型分析、扰动效应的量化统计方法,以及蛋白质相互作用的结构预测分析。所有iPSC样本均来自HipSci联盟的健康供体队列。
研究人员通过精心设计的实验方案,成功建立了大规模基因扰动筛选的技术体系。质量控制后,他们获得了每个引导RNA中位数8个细胞、每个基因中位数25个细胞的覆盖度。方差分解分析显示,与细胞系和基因组背景相比,CRISPRi敲低引起的转录变化相对较小,表明在感染后3-6天的观察时间内,CRISPRi靶向主要诱导的是细微的转录变化而非完全的细胞状态转变。
研究发现,约51%的靶基因(3,374/6,674)在敲低后至少产生一个显著的转座效应,平均每个靶基因产生2.57个效应。具有最多转座效应的基因涉及多能性维持、转录和剪接等基础生物学功能。值得注意的是,靶基因的必要性是预测其转座效应数量的最重要特征,这与在其他细胞类型中的发现一致。
研究最引人注目的发现之一是遗传背景在调节基因扰动效应中的重要作用。通过针对444个基因在10个供体(每个供体2个细胞系)中的精密筛选,研究人员发现供体成分在2,941个转座效应(占测试的4.3%)中解释了显著比例的方差,这些被称为可遗传效应。这些可遗传的转座效应主要涉及多能性维持基因、剪接基因以及与罕见疾病相关的基因。
面向基因组和群体规模单细胞CRISPR筛选的设计、实施和分析
研究还系统评估了大规模筛选中的关键实验因素,发现引导RNA身份对观察到的转座效应影响最大,其次是CRISPRi效率。研究人员强调,细胞数量、个体细胞混合策略以及检测时间点的选择都是确保数据质量的关键考量。
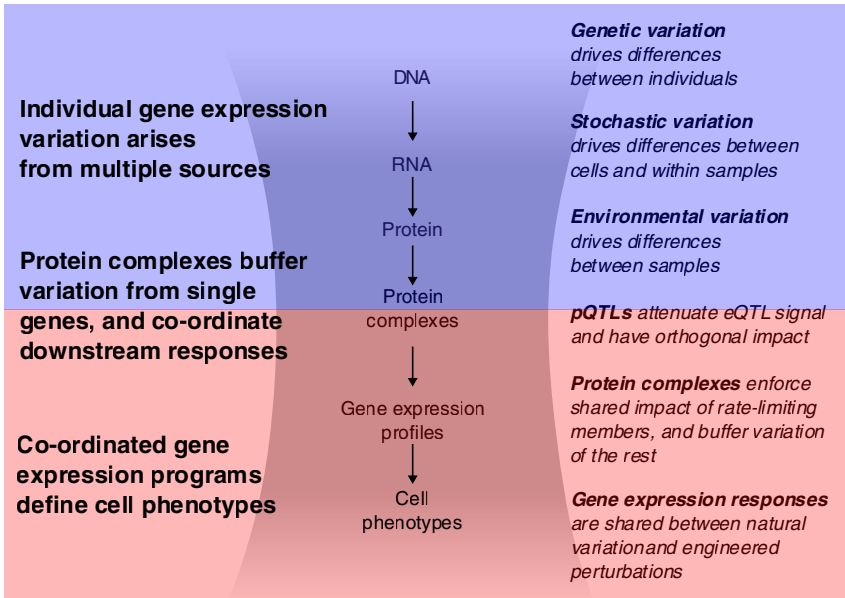
这项研究标志着基因组规模CRISPR筛选与群体水平单细胞RNA测序读取相结合的崭新开端。蛋白质复合物作为整合转录变化和调节下游效应的关键枢纽,在缓冲基因表达变异性方面发挥重要作用。研究发现,尽管基因表达存在差异,但蛋白质水平的缓冲机制确保持续的细胞功能稳定性。
该研究的创新性在于首次将自然遗传变异与工程化扰动及单细胞测序读取相结合,为理解人类基因调控提供了全新视角。研究发现,扰动效应的相似性能够准确反映蛋白质复合物的成员关系,而结合AlphaFold2结构预测,可以高置信度地预测蛋白质相互作用事件。
然而,研究也存在一定局限性,包括供体数量有限、脱靶效应的普遍存在以及目标基因与细胞数量之间的权衡。这些因素限制了检测更细微扰动效应的能力,也为未来研究指明了方向。
这项工作为构建个体特异性扰动响应的基础模型迈出了重要一步,未来在细胞模型、类器官和原代细胞中应用这种方法,将推动我们对疾病原因的理解,并解开遗传效应的复杂性。尽管需要仔细的技术优化,但这些数据对于构建个体特异性扰动响应基础模型、预测和控制细胞行为至关重要,最终将为精准医疗和疾病治疗提供有力支持。
 生物通微信公众号
生物通微信公众号
 生物通新浪微博
生物通新浪微博
今日动态 |
人才市场 |
新技术专栏 |
中国科学人 |
云展台 |
BioHot |
云讲堂直播 |
会展中心 |
特价专栏 |
技术快讯 |
免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号


 生物通微信公众号
生物通微信公众号