
-

…ķőÔÕ®ĻŔőĘ
Ň„ń„◊•◊°…ķ√ŁŅ∆ľľ
ŐÝ∂ĮĶń¬Ų≤ę
LAT1◊™‘ňĶįį◊ĶńĹŠĻĻĽýī°Ĺ“ ĺŅĻį©“©őÔ ∂Īū”ŽįĪĽýňŠ◊™‘ňĶń∑÷◊”Ľķ÷∆
°ĺ◊÷ŐŚ£ļ īů ÷– –° °Ņ Īľš£ļ2025ńÍ02‘¬15»’ ņī‘ī£ļNature Communications
Īŗľ≠Õ∆ľŲ£ļ
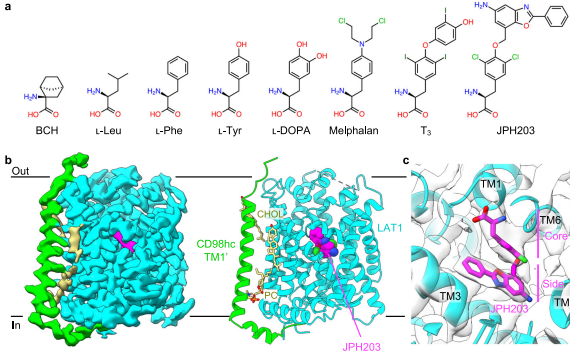
°°°°Īĺ—–ĺŅ’Ž∂‘L–ÕįĪĽýňŠ◊™‘ňĶįį◊1(LAT1/SLC7A5)‘ŕį©÷Ę÷őŃ∆÷–ĶńĻōľŁ◊ų”√£¨Õ®Ļżņš∂≥ĶÁĺĶľľ űĹ‚őŲŃňJPH203Ķ»“÷÷∆ľŃ”ŽLAT1ĹŠļŌĶńŃý÷÷ĹŠĻĻ£¨Ĺ“ ĺŃňł√◊™‘ňĶįį◊»ż÷÷ĻĻŌůŌ¬ĶńĶ◊őÔ ∂Īū”Ž“÷÷∆Ľķ÷∆°£—–ĺŅ∑ĘŌ÷ŅĻį©“©őÔJPH203Õ®Ļż∂ņŐōĶńU–ÕĻĻŌůĹęLAT1ňÝ∂®‘ŕŌÚÕ‚Ņ™∑Ň◊īŐ¨£¨∂Ýĺ≠Ķš“÷÷∆ľŃBCH‘Ú”’ĶľĪ’»ŻĻĻŌů£¨≤Ż√ųŃň≤ĽÕ¨“÷÷∆ľŃĶń∑÷◊”◊ų”√≤Ó“ž°£ł√≥…ĻŻő™…Ťľ∆į–ŌÚLAT1ĶńŅĻį©“©őÔŐŠĻ©Ńň÷ō“™ĹŠĻĻĽýī°£¨¬Řőń∑ĘĪŪ”ŕ°∂Nature Communications°∑°£
‘ŕį©÷Ę…ķőÔ—ßŃž”Ú£¨L–ÕįĪĽýňŠ◊™‘ňĶįį◊1(LAT1/SLC7A5)“Ľ÷ĪĪĽ ”ő™ľęĺŖ«ĪѶĶń÷őŃ∆į–Ķ„°£’‚÷÷Őō ‚Ķń◊™‘ňĶįį◊≤ĽĹŲłļ‘ū‘ň šĪō–ŤįĪĽýňŠ£¨ĽĻń‹◊™‘ňľ◊◊īŌŔľ§ňōT3/T4ļÕ∂ŗ÷÷ŅĻį©“©őÔ£¨»Á÷őŃ∆∂ŗ∑Ę–‘Ļ«ňŤŃŲĶń¬Ū∑®ņľ(melphalan)°£łŁ“ż»ň◊ĘńŅĶń «£¨LAT1‘ŕīů∂ŗ ż∂Ů–‘÷◊ŃŲ÷–Ļż∂»ĪŪīÔ£¨ő™į©ŌłįŻŐŠĻ©‘Ų÷≥ňý–ŤĶń"”™—Ý≤ĻłÝ"£¨ Ļ∆š≥…ő™ŅĻį©“©őÔŅ™∑ĘĶń"√ų–«į–ĪÍ"°£»Ľ∂Ý≥§∆ŕ“‘ņī£¨Ņ∆—ßľ“√«∂‘LAT1»Áļő«Ý∑÷Ķ◊őÔļÕ“÷÷∆ľŃ°ĘŐōĪū «ŃŔī≤ŌŗĻō“©őÔĶń∑÷◊”Ľķ÷∆÷™÷ģ…ű…Ŕ£¨’‚—Ō÷ō÷∆‘ľŃňį–ŌÚ“©őÔĶńņŪ–‘…Ťľ∆°£
ņī◊‘¬ŪŅňňĻ°§∆’ņ Ņň…ķőÔőÔņŪ—–ĺŅňý(Max Planck Institute of Biophysics)Ķ»ĽķĻĻĶń—–ĺŅÕŇ∂”Õ®Ļżņš∂≥ĶÁĺĶľľ ű£¨≥…Ļ¶Ĺ‚őŲŃňLAT1”Ž≤ĽÕ¨ŇšŐŚĹŠļŌĶńŃý÷÷łŖ∑÷Īś¬ ĹŠĻĻ£¨įŁņ®ŅĻį©“©őÔJPH203(”÷≥∆nanvuranlat)°Ęĺ≠Ķš“÷÷∆ľŃBCH“‘ľįŐž»ĽĶ◊őÔL-ĪĹĪŻįĪňŠ(L-Phe)Ķ»°£’‚–©ĹŠĻĻĹ“ ĺŃňLAT1‘໿÷÷≤ĽÕ¨ĻĻŌůŌ¬ĶńĺęŌłĪšĽĮ£¨ő™ņŪĹ‚∆š◊™‘ňļÕ“÷÷∆Ľķ÷∆ŐŠĻ©Ńň‘≠◊”ňģ∆ĹĶńľŻĹ‚°£’‚ŌÓÕĽ∆∆–‘—–ĺŅ∑ĘĪŪ‘ŕ°∂Nature Communications°∑…Ō£¨ő™Ņ™∑Ę–¬“ĽīķŅĻį©“©őÔĶž∂®Ńň÷ō“™Ľýī°°£
—–ĺŅ»ň‘Ī≤…”√∂ŗŌÓĻōľŁľľ ű£ļ1)ĹęLAT1-CD98hcłīļŌőÔ÷ōĻĻĶĹļ¨”–Ķ®ĻŐīľĶńń…√◊÷¨÷ ŇŐ÷–£¨ń£ń‚Őž»Ľń§Ľ∑ĺ≥£Ľ2)Ņ™∑ĘŐō“ž–‘ŅĻŐŚFab∆¨∂ő◊ųő™ņš∂≥ĶÁĺĶĪÍľ«£Ľ3)Õ®Ļż∂ŗŐŚĺŘĹĻŌłĽĮŐŠłŖŅÁń§”Ú∑÷Īś¬ £Ľ4)ņŻ”√∑«÷ř◊¶ůł¬—ńłŌłįŻŌĶÕ≥ĹÝ––Ļ¶ń‹–‘—ť÷§ Ķ—ť£Ľ5)≤…”√≤Ó“ž”≥…šľľ ű—ť÷§ŇšŐŚĹŠļŌ°£
—–ĺŅĹŠĻŻ≤Ņ∑÷£¨ ◊Ō»‘ŕ"LAT1”ŽJPH203ĹŠļŌĶńĹŠĻĻĽýī°"÷–∑ĘŌ÷£¨’‚÷÷ŅĻį©“©őÔÕ®Ļż∂ņŐōĶńU–ÕĻĻŌůĹęLAT1"ňÝňņ"‘ŕŌÚÕ‚Ņ™∑Ň◊īŐ¨°£JPH203Ķń5-įĪĽý-2-ĪĹĽýĪĹ≤Ę∂ŮŖÚ≤ŗĽý“‚Õ‚Ķō√Ľ”–ĹÝ»Ž‘§≤‚Ķń"‘∂∂ňŅŕīŁ"£¨∂Ý «Õ∆ľ∑ŅÁń§¬›–ż3(TM3)≤Ę ĻTM10Õš«ķ°£ĻōľŁ≤–ĽýPhe252”ŽJPH203ń©∂ňĪĹĽý–ő≥…T–Õ¶–-¶–∂—Ľż£¨∂ÝTyr259‘Ú”Ž∆š¬»‘≠◊”–ő≥…¬ĪľŁ°£’‚–©ŌŗĽ•◊ų”√Ļ≤Õ¨Ķľ÷¬Ķ◊őÔĹŠļŌŅŕīŁņ©īů£¨ĻŐ∂®ŃňLAT1ĶńŅ™∑ŇĻĻŌů°£
‘ŕ"PheļÕ¬Ū∑®ņľ‘ŕŅŕīŁ÷–ĪŪŌ÷≥Ų≤ĽÕ¨≥Ő∂»ĶńŌŗĽ•◊ų”√"≤Ņ∑÷£¨—–ĺŅ∑ĘŌ÷…ķņŪĶ◊őÔL-PheĹŲ”ŽGly255–ő≥…∑∂Ķ¬Ľ™Ń¶◊ų”√£¨∂ÝŅĻį©“©¬Ū∑®ņľĶńbis-(2-¬»““Ľý)įĪĽý≤ŗŃī‘Ú”ŽTM3°ĘTM6aļÕTM10–ő≥…Ņ’ľšőĽ◊Ť°£’‚÷÷ŃĘŐŚ◊Ťį≠Ĺ‚ ÕŃňő™ļő¬Ū∑®ņľňš»Ľń‹ĪĽ◊™‘ňĶęňŔ¬ ĹŌ¬ż£¨Õ¨ Ī“≤ĺŖ”–“÷÷∆ĽÓ–‘°£ŐōĪū÷ĶĶ√◊Ę“‚Ķń «£¨¬Ū∑®ņľĶńŃĹłŲ¬»““Ľý∑÷Īū÷łŌÚ…ŌŌ¬∑ĹŌÚ£¨”ŽTyr259ļÕAsn404–ő≥…¬ĪľŁ£¨’‚–©∂ÓÕ‚ŌŗĽ•◊ų”√Ōř÷∆ŃňĻĻŌůĪšĽĮ°£
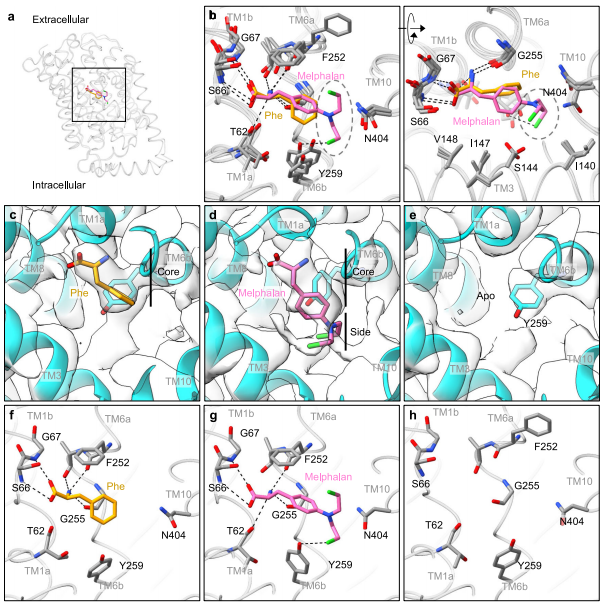
"∑«—°‘Ů–‘ŌĶÕ≥L“÷÷∆ľŃBCH”’ĶľĪ’»Ż◊īŐ¨"Ķń∑ĘŌ÷”»ő™ĻōľŁ°£”ŽJPH203≤ĽÕ¨£¨BCH ĻLAT1≥ Ō÷ÕÍ»ęĪ’»ŻĻĻŌů£¨ŇšŐŚĪĽÕÍ»ę√‹∑‚‘ŕń§÷–°£BCHĶńĹĶĪý∆¨ÕťĽý”ŽSer144°ĘIle147ļÕVal148Ĺ”ī•£¨∂ÝPhe252ŌŮ"ł«◊”"“Ľ—ýł≤ł«‘ŕBCH…Ō∑Ĺ°£TM10–ż◊™‘ľ70°„–ő≥…÷Ī¬›–ż£¨ ĻPhe400”ŽBCH≤ŗ√śĹ”ī•°£’‚–©ĪšĽĮ ĻŅŕīŁł’ļ√ń‹»›ń…BCH£¨”ŽJPH203“ż∆ūĶńŅŕīŁņ©’Ň–ő≥…Ō √ų∂‘Ī»°£

◊™‘ň Ķ—ť÷§ ĶŃňĹŠĻĻĻŘ≤ž£ļ‘ŕ"JPH203◊Ť∂Ō◊™‘ň∂ÝBCH”’Ķľ∑īŌÚ◊™‘ň"≤Ņ∑÷£¨—–ĺŅ∑ĘŌ÷BCHń‹ŌŮĶ◊őÔ“Ľ—ý”’ĶľL-ŃŃįĪňŠ(L-Leu)Õ‚ŇŇ£¨∂ÝJPH203‘ÚÕÍ»ę◊Ť∂Ō◊™‘ň°£’‚÷§ ĶBCH «Ņ…◊™‘ňĶńĺļ’ý–‘“÷÷∆ľŃ£¨∂ÝJPH203 «’ś’żĶń◊Ť∂ŌľŃ°£
‘ŕ"◊™‘ňĽķ÷∆÷–ĶńĹŠĻĻ÷ōŇŇ"≤Ņ∑÷£¨—–ĺŅ≤∂◊ĹĶĹLAT1ī”ŌÚÕ‚Ņ™∑ŇĶĹŌÚńŕŅ™∑ŇĶńÕÍ’ŻĻĻŌůĪšĽĮ°£ŐōĪū∑ĘŌ÷N∂ň50łŲ≤–ĽýĶń»Ī ß Ļ◊™‘ňĽÓ–‘Õͻꅕ ߣ¨ŐŠ ĺł√«Ý”Ú‘ŕĻĻŌůĪšĽĮ÷–ĶńĻōľŁ◊ų”√°£īňÕ‚£¨Ķ®ĻŐīľ‘ŕTM9-TM12Ń—Ō∂÷–ĶńĻĻŌůŐō“ž–‘ĹŠļŌ£¨Ĺ‚ ÕŃňő™ļőĶ®ĻŐīľń‹‘Ų«ŅLAT1ĽÓ–‘°£
’‚ŌÓ—–ĺŅĶń÷ō“™“‚“Ś‘ŕ”ŕ£ļ1) ◊īőĹ“ ĺŃňŅĻį©“©őÔJPH203”ŽLAT1Ķńĺę»∑ĹŠļŌń£ Ĺ£¨≤Ż√ųŃň∆šłŖ—°‘Ů–‘ļÕ«Ņ–ß“÷÷∆ĶńĹŠĻĻĽýī°£Ľ2)∑ĘŌ÷ŃňBCH”’ĶľĪ’»ŻĻĻŌůĶń∂ņŐōĽķ÷∆£¨Ĺ‚ ÕŃň’‚÷÷ĺ≠Ķš“÷÷∆ľŃń‹ĻĽ◊ųő™∑īŌÚ◊™‘ňĶ◊őÔĶń‘≠“Ú£Ľ3)≤Ż√ųŃň≤ĽÕ¨īů–°Ķ◊őÔ(»Á¬Ū∑®ņľ)◊™‘ňňŔ¬ ≤Ó“žĶńĹŠĻĻĺŲ∂®“Úňō£Ľ4)ő™…Ťľ∆–¬“ĽīķŅ…◊™‘ň“©őÔĽÚ«Ņ–ß“÷÷∆ľŃŐŠĻ©Ńň«ŚőķĶńĹŠĻĻń£įŚ°£’‚–©∑ĘŌ÷≤ĽĹŲÕ∆∂ĮŃňį©÷Ęį–ŌÚ÷őŃ∆Ķń∑Ę’Ļ£¨“≤ő™ņŪĹ‚ń§◊™‘ňĶįį◊ĶńĻ§◊ųĽķ÷∆ŐŠĻ©Ńň÷ō“™∑∂ņż°£
—–ĺŅĽĻŐŠ≥ŲŃň–Ū∂ŗ÷ĶĶ√…Ó»ŽŐĹňųĶń∑ĹŌÚ£ļ»ÁmetaőĽ»°īķĽý»Áļő”įŌž“÷÷∆ľŃ—°‘Ů–‘°ĘĶ®ĻŐīľĶųĹŕĽÓ–‘Ķńĺę»∑Ľķ÷∆°Ę“‘ľį»ÁļőņŻ”√’‚–©ĹŠĻĻ–ŇŌĘ…Ťľ∆łŁ”––ßĶńŅĻį©“©őÔĶ»°£ł√ÕŇ∂”Ĺ®ŃĘĶńń…√◊÷¨÷ ŇŐŌĶÕ≥ő™ļů–Ý—–ĺŅŐŠĻ©Ńň”–ѶĻ§ĺŖ£¨”–ÕŻīŔĹÝ∂‘LAT1ľį∆šňŻń§◊™‘ňĶįį◊ĶńłŁ…Ó»Ž»Ō ∂°£
 …ķőÔÕ®őĘ–ŇĻę÷ŕļŇ
…ķőÔÕ®őĘ–ŇĻę÷ŕļŇ
÷™√Ż∆ů“Ķ’–∆ł
ĹŮ»’∂ĮŐ¨ | »ň≤Ň –≥° | –¬ľľ ű◊®ņł | ÷–ĻķŅ∆—ß»ň | ‘∆’ĻŐ® | BioHot | ‘∆Ĺ≤Ő√÷Ī≤• | ĽŠ’Ļ÷––ń | ŐōľŘ◊®ņł | ľľ űŅž—∂ | √‚∑— ‘”√
įś»®ňý”– …ķőÔÕ®
Copyright© eBiotrade.com, All Rights Reserved
Ń™ŌĶ–ŇŌš£ļ
‘ŃICPĪł09063491ļŇ