
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:猪繁殖与呼吸综合征病毒(PRRSV)与宿主细胞的策略与博弈
【字体: 大 中 小 】 时间:2025年06月12日 来源:Virology Journal 4
编辑推荐:
这篇综述系统阐述了PRRSV(猪繁殖与呼吸综合征病毒)入侵宿主细胞的分子机制及其免疫逃逸策略,重点解析了病毒利用CD163、MYH9等受体及HSPA8、RAB18等宿主因子完成内化与复制的途径,同时揭示了Nsp1β、Nsp4等效应蛋白通过降解SLA-I(猪白细胞抗原I类)和抑制干扰素(IFN)信号通路实现免疫抑制的分子基础,为开发新型疫苗和抗病毒靶点提供了理论依据。
PRRSV通过"受体组合拳"入侵宿主细胞:CD163的SRCR5结构域与病毒GP2a/GP4蛋白结合后,招募钙蛋白酶1(calpain 1)启动病毒脱壳;同时,MYH9的C端与GP5相互作用形成纤维状聚集体,协同HS(硫酸乙酰肝素)增强病毒吸附。有趣的是,TIM1/4受体通过识别病毒包膜磷脂酰丝氨酸(PS),激活Rac1/Cdc42-Pak1信号轴促进胞饮作用,而miR-142-3p可通过抑制Rac1表达阻断该过程。
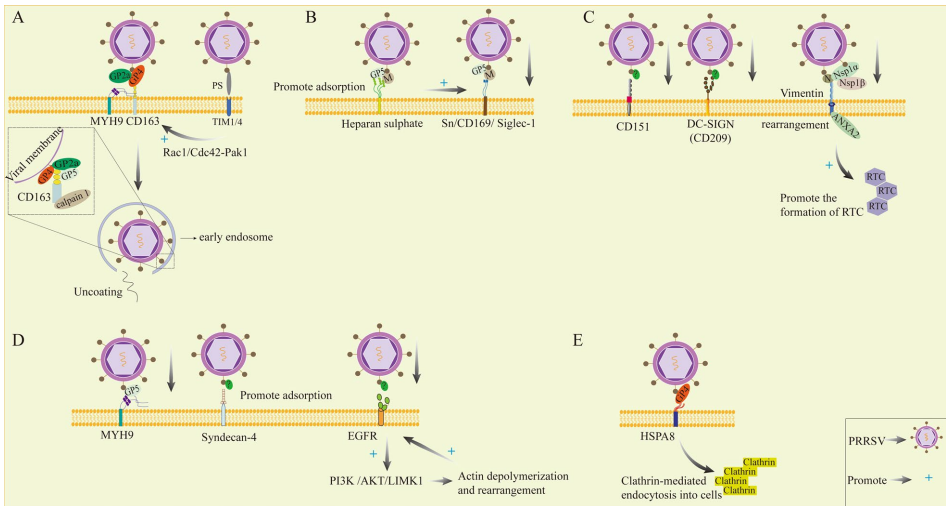
病毒在胞内建立"复制堡垒":Nsp2与GRASP65相互作用释放RAB2,通过ULK1磷酸化激活LC3介导的自噬;Nsp9则通过AKT-mTOR-S6K1通路促使PDCD4泛素化降解,解除其对病毒基因转录的抑制。更巧妙的是,Nsp1β通过降解p21蛋白推动细胞进入S期,劫持宿主DNA合成系统。代谢重编程尤为突出――GP5结合GAPDH维持糖酵解活性,Nsp1β则稳定HIF-1α促进乳酸生成,后者通过抑制MAVS信号削弱抗病毒反应。
PRRSV展现"免疫隐身术":Nsp1a与HOIP/HOIL-1L形成复合物降解NEMO,阻断NF-κB信号;Nsp4切割NEMO的E349/S350位点抑制IFN-β产生。在抗原呈递层面,Nsp1a诱导SLA-I泛素化降解,而Nsp4通过抑制β2
M转录双重打击MHC-I类分子呈递功能。值得注意的是,Nsp11的核糖核酸内切酶活性可降解STAT2,破坏ISGF3复合体形成,实现干扰素信号通路的全面压制。

宿主细胞发展出多层次防御:BST2(骨髓基质抗原2)通过蛋白酶体降解病毒Nsp12和E蛋白;IFITM3通过棕榈酰化修饰促进胆固醇积累,阻断病毒膜融合。非编码RNA也参与抗病毒――lnc-CAST通过组蛋白H3K27ac修饰激活CXCL8表达招募中性粒细胞,而MAHAT lncRNA与DDX6协同抑制ZNF34增强I型干扰素产生。
新型检测技术如CRISPR-Cas13系统可实现PRRSV变异株的多重检测,而单细胞测序能解析感染相关的免疫细胞亚群。在治疗策略上,敲除CD163 SRCR5结构域可培育抗PRRSV转基因猪,但需考虑伦理接受度。针对病毒效应蛋白(如Nsp1α的ZF结构域)的小分子抑制剂,以及靶向宿主因子(如RAB18-CMA通路)的调控剂,正成为抗病毒药物开发的新方向。
该研究系统揭示了PRRSV与宿主的复杂互作网络,为理解病毒持续感染机制和开发新型防控策略提供了重要理论基础。
 生物通微信公众号
生物通微信公众号
知名企业招聘