
-

生物通官微
陪你抓住生命科技
跳动的脉搏
硒纳米颗粒联合放射治疗作为肝细胞癌新型辅助疗法的机制研究及临床转化潜力
【字体: 大 中 小 】 时间:2025年06月15日 来源:Journal of the Egyptian National Cancer Institute 2.1
编辑推荐:
本研究针对肝细胞癌(HCC)治疗中化疗药物索拉非尼(SFB)毒性大、放疗选择性差等临床难题,创新性地采用硒纳米颗粒(SeNPs)联合γ/UV放射治疗策略。通过MTT法、流式细胞术和Western blot等技术证实,SeNPs(12.66nm)与高剂量辐射(γ 0.2Gy/UV 180s)联用可显著增强p53介导的凋亡通路,使细胞活力降低至50.3%,同时诱导细胞周期G2/M期阻滞和线粒体细胞色素C释放。该研究为开发低毒高效的HCC联合治疗方案提供了新思路。
肝细胞癌(HCC)是全球第四大癌症死因,尤其在肝硬化患者中死亡率居高不下。尽管分子靶向药物索拉非尼(Sorafenib)已被批准用于晚期HCC治疗,但其水溶性差、需要高剂量给药导致的皮疹、腹泻和高血压等副作用严重限制了临床应用。更棘手的是,传统放疗虽对HCC敏感,但由于缺乏肿瘤选择性,常损伤周围正常肝组织,诱发辐射诱导性肝病(RILD)。如何在提高疗效的同时降低毒性,成为HCC治疗领域亟待突破的瓶颈。
针对这一临床困境,埃及Beni-Suef大学的研究团队创新性地将目光投向硒纳米颗粒(SeNPs)。这种兼具低毒性和高生物相容性的纳米材料,不仅本身具有抗癌活性,还能通过"高Z元素"特性增强放射敏感性。研究人员假设:SeNPs可能通过调节活性氧(ROS)水平和p53通路,与放疗产生协同效应,从而在降低辐射剂量的同时提高肿瘤杀伤效果。为验证这一设想,团队在《Journal of the Egyptian National Cancer Institute》发表了突破性研究成果。
研究采用化学还原法合成12.66nm的球形SeNPs,通过透射电镜(TEM)和马尔文粒径分析仪确认其理化特性。实验设计包含11组HepG2细胞处理方案:空白对照、溶剂对照、索拉非尼单药组、SeNPs单药组、不同剂量γ/UV单独照射组(γ 0.1Gy、γ 0.2Gy、UV 90s、UV 180s)以及SeNPs与各剂量辐射的联合组。主要技术路线包括:MTT法检测细胞活力、流式细胞术分析细胞周期和p53表达、Western blot检测线粒体和胞浆细胞色素C分布、琼脂糖凝胶电泳观察DNA片段化。
【Se-nanoparticles characterization results】
TEM和扫描电镜(SEM)显示合成的SeNPs呈均匀球形,平均粒径12.66nm,Zeta电位-6.39mV表明其具有适中的稳定性。


【MTT results】
联合治疗组展现出显著优于单药的效果:γ 0.2Gy+SeNPs组细胞活力仅0.58%,UV 180s+SeNPs组为50.3%,均显著低于相应单独照射组(p<0.0001)。值得注意的是,γ 0.2Gy单用组已显示极强细胞毒性(0.58%活力),但联合SeNPs后能减少辐射剂量需求。


【P53 and cell cycle analysis by flowcytometry】
流式细胞术揭示关键机制:γ 0.2Gy+SeNPs组p53表达高达75%,是索拉非尼组(38%)的2倍。


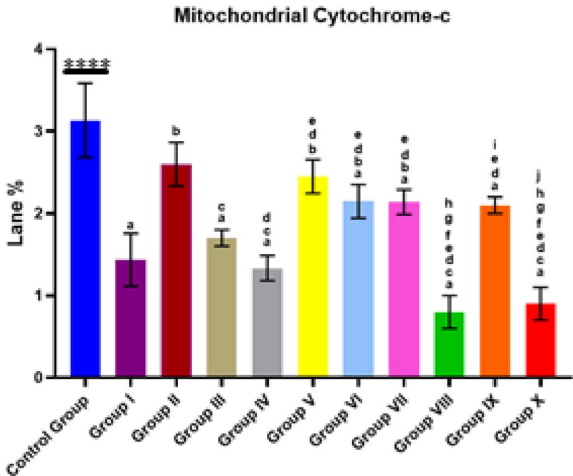
【Cytochrome C by western blotting】
Western blot证实线粒体-胞浆细胞色素C重分布:γ 0.2Gy+SeNPs组线粒体细胞色素C降至0.8%,同时胞浆中升高至2.24%,表明强烈激活线粒体凋亡通路。

【DNA fragmentation】
琼脂糖电泳显示:UV 180s+SeNPs组DNA片段化最显著,而SeNPs单药组片段化程度最低,证实辐射是触发DNA损伤的关键因素。

这项研究通过多角
 生物通微信公众号
生物通微信公众号
知名企业招聘