
-

生物通官微
陪你抓住生命科技
跳动的脉搏
裸盖菇素预防自杀的分子机制:基于网络药理学与分子对接的多靶点通路解析
【字体: 大 中 小 】 时间:2025年06月17日 来源:Translational Psychiatry 5.8
编辑推荐:
本研究针对传统抗抑郁药物起效慢、副作用大等临床难题,创新性地采用网络药理学与分子对接技术,揭示了裸盖菇素(psilocybin)通过HTR2A/2C/7和PRKACA等核心靶点调控5-羟色胺能突触和钙信号通路的多靶点抗自杀机制。研究人员通过构建药物-疾病-靶点-通路网络,结合分子对接验证,为开发快速起效的抗自杀药物提供了全新理论依据,相关成果发表于《Translational Psychiatry》。
每年全球有约80万人因自杀身亡,其中抑郁症患者占比高达40-50%。传统抗抑郁药虽被广泛使用,却面临着起效缓慢(通常需4-6周)、有效率不足50%以及心脏毒性等副作用明显的困境。更令人担忧的是,自杀者脑干中5-HT及其代谢物5-HIAA浓度显著低于正常人群,而现有5-HT受体激动剂治疗效果有限。在这种临床背景下,裸盖菇素――一种存在于"神奇蘑菇"中的致幻剂成分,因其在治疗抵抗性抑郁症中展现出的"突破性疗法"潜力,引起了科学界的广泛关注。美国FDA已将其列为抑郁症的"突破性疗法",但关于其预防自杀的具体分子机制仍是一片空白。
为解决这一科学难题,来自中国的研究团队在《Translational Psychiatry》发表了一项开创性研究。研究人员采用多学科交叉的研究策略,首先通过PharmMapper等6大数据库筛选裸盖菇素的潜在作用靶点,同时从DisGeNET等平台获取自杀相关靶点。运用STRING数据库构建蛋白互作网络后,采用Cytoscape的CytoNCA插件进行拓扑分析,筛选出13个核心靶点。随后通过DAVID工具进行GO和KEGG富集分析,最终采用AutoDock Vina进行分子对接验证。所有分析均基于公共数据库数据,无需伦理审批。
研究结果部分呈现了系统性发现:
靶点筛选与网络构建:从117个裸盖菇素靶点和2185个自杀相关靶点中,鉴定出55个共同靶点。通过蛋白互作网络分析,最终锁定13个关键靶点,其中SRC、HTR2A和HTR1A的节点度值最高(分别为17、16和16)。

通路富集分析:GO分析显示G蛋白偶联5-HT受体信号通路是最显著富集的生物过程(p<0.05)。KEGG分析则揭示5-羟色胺能突触通路和钙信号通路是最关键的两条通路,涉及HTR2A、HTR2C、HTR7和PRKACA四个核心靶点。

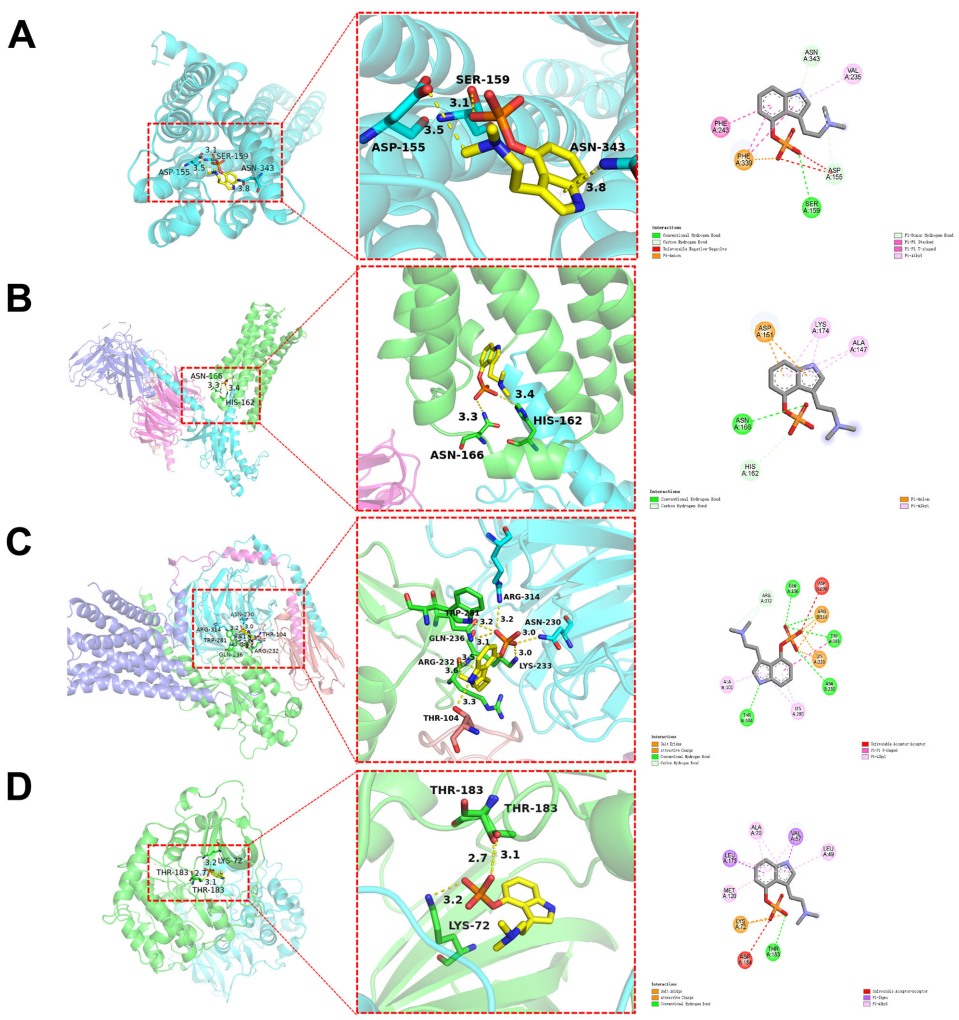
分子对接验证:对接结果显示裸盖菇素与PRKACA结合能最低(-7.5 kcal/mol),与HTR2A的结合能为-7.4 kcal/mol,均表现出稳定结合特性。HTR7通过8个氢键与裸盖菇素形成复杂相互作用。
在讨论部分,研究团队提出了创新性机制解释:裸盖菇素可能通过三重机制发挥抗自杀作用:(1)直接激活5-HT2A
受体,迅速提升前额叶皮层谷氨酸、GABA和多巴胺水平;(2)通过PRKACA调控cAMP-PKA信号轴,影响神经元可塑性;(3)协同调节钙离子(Ca2+
)信号转导,纠正MDD患者中存在的钙信号紊乱。特别值得注意的是,该研究首次将PRKACA(cAMP依赖性蛋白激酶催化亚基α)确认为裸盖菇素的新靶点,这为理解其快速起效特性提供了全新视角。
该研究的临床意义在于:为开发起效更快(可能数小时内)、作用更持久的抗自杀药物提供了明确的靶点线索。相比需要长期服用的SSRIs类药物,裸盖菇素单次给药即可产生持续数周的疗效,这种"一针见效"的特性对急性自杀干预具有重大价值。但研究也指出需警惕药物滥用风险,建议未来研究应着重阐明成瘾回路与抗自杀回路的交叉机制。这项研究不仅为抑郁症和自杀预防领域带来了新希望,也为网络药理学方法在精神药物研发中的应用提供了典范。
 生物通微信公众号
生物通微信公众号
知名企业招聘