
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:人工智能在胰腺癌组织病理学和诊断中的应用――对临床决策和生物标志物发现的启示?
【字体: 大 中 小 】 时间:2025年06月18日 来源:Cell Division 2.8
编辑推荐:
这篇综述系统探讨了人工智能(AI)和机器学习(ML)在胰腺导管腺癌(PDAC)诊疗中的前沿应用,重点分析了卷积神经网络(CNN)在组织病理学图像识别、分子分型和多模态数据整合中的突破性进展(AUC达0.9836),同时指出数据异质性和临床转化面临的挑战。
人工智能照亮胰腺癌诊疗迷雾
引言
人工智能(AI)和机器学习(ML)正以前所未有的速度重塑癌症诊断领域。作为计算机科学的前沿分支,AI系统通过模拟人类认知功能,能够从海量数据中识别隐藏模式并建立预测模型。ML作为AI的核心子集,通过自主学习和持续优化,在胰腺癌(PC)这种具有高度异质性的恶性肿瘤诊疗中展现出独特价值。
胰腺癌的临床困境
胰腺导管腺癌(PDAC)占所有胰腺恶性肿瘤的90%,其中位生存期仅11.7个月。这种疾病的残酷性源于三个关键特征:早期症状隐匿导致60%患者确诊时已届晚期;显著的形态学和分子异质性(单个肿瘤内可存在多种亚型);对化疗的固有耐药性。目前仅有15-20%患者适合根治性手术,而传统标志物CA19-9的敏感性和特异性均不足(约70%)。
AI在组织病理学的突破
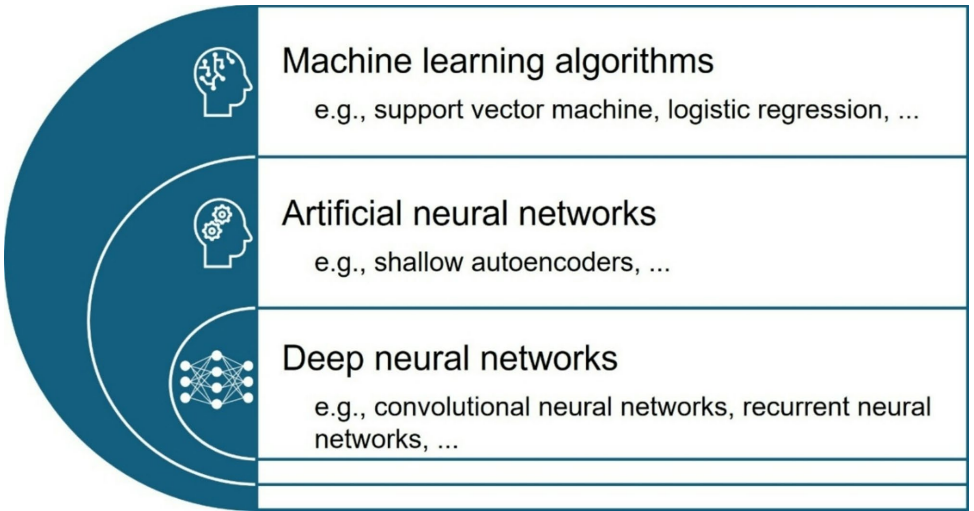
卷积神经网络(CNN)已成为数字病理学的革命性工具:
• 诊断准确性:Fu等开发的CNN模型在231例全切片图像(WSI)分析中达到100%的准确率,Naito团队在532例样本中实现AUC 0.9836
• 治疗反应预测:Janssen等构建的多中心模型(含528例新辅助治疗后病例)可识别残留癌细胞(F1分数0.78)
• 分子分型:Ahmadvand团队通过207张WSI准确区分PDAC基底样和经典型(平衡准确度96.19% vs 83.03%)
生物标志物发现新范式
ML算法正颠覆传统生物标志物开发模式:
• 蛋白质组学:Athanasiou团队鉴定的血清蛋白标志物对早期PDAC的AUC达0.95
• 代谢组学:Wolrab开发的脂质组模型区分PDAC与健康人的准确率94.18%
• 微生物标记:Chen等整合肠道菌群与CA19-9的模型AUC提升至0.977
多模态数据融合
Chen等开创性研究证明,整合组织学图像与分子特征数据可显著提升预后预测(C-index 0.653 vs 单模态0.580-0.593)。这种"1+1>2"的效应在肝癌和胶质瘤研究中得到验证,但需警惕低信息量数据导致的过拟合风险。
挑战与展望
当前面临三大瓶颈:①标注数据获取困难(需病理专家逐帧验证)②扫描仪和染色差异导致的泛化性问题(外部验证准确度可能骤降31.84%)③伦理监管空白。未来方向包括:建立PDAC特异性图像库(如CAMELYON模式)、开发不确定性量化算法、开展前瞻性临床试验(ISGPP-2框架)。
这场由AI驱动的诊疗革命正在改写胰腺癌管理范式。从WSI分析到液体活检,从单模态诊断到多维度预测,智能算法不仅缩短了诊断时间窗,更揭示了传统方法难以捕捉的疾病本质特征。随着PANDA等国际挑战赛的推进,一个基于深度学习的精准医疗新时代正在到来。
 生物通微信公众号
生物通微信公众号
知名企业招聘