
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Olink蛋白质组学揭示TNFRSF9作为腹主动脉瘤新型炎症标志物的诊断价值
【字体: 大 中 小 】 时间:2025年06月18日 来源:iScience 4.6
编辑推荐:
本研究通过Olink蛋白质组学技术,首次发现TNFRSF9与IL-6在腹主动脉瘤(AAA)患者血清中显著共表达,结合动物模型验证其作为诊断标志物的潜力。研究揭示了TNFRSF9通过T细胞介导的炎症反应参与AAA发病的新机制,为这一缺乏有效药物治疗的疾病提供了新的诊断靶点和治疗方向。
腹主动脉瘤(Abdominal Aortic Aneurysm, AAA)被称为人体内的"沉默炸弹",这种血管壁异常扩张的疾病在破裂前往往没有明显症状,但一旦破裂死亡率高达80%-90%。目前临床诊断主要依赖影像学检查,缺乏有效的血液标志物,药物治疗更是空白。这种困境背后,是科学家们对AAA发病机制认知的不足――尽管已知慢性炎症是关键驱动因素,但具体哪些炎症因子起主导作用仍不清楚。
山西医科大学第二医院的研究团队在《iScience》发表的最新研究中,采用Olink邻近延伸检测(Proximity Extension Assay, PEA)技术对28例临床样本(18例AAA患者vs 10例健康人)进行92种炎症相关蛋白筛查,结合GSE183464转录组数据和动物实验,首次将肿瘤坏死因子受体超家族成员9(TNFRSF9)鉴定为AAA的新型诊断标志物。研究发现TNFRSF9与经典炎症因子IL-6的组合诊断模型曲线下面积(AUC)高达0.95,并通过单细胞测序揭示TNFRSF9主要富集于AAA组织中的T细胞,为理解AAA的免疫调控机制开辟了新视角。
关键技术包括:1)Olink PEA技术检测血清炎症蛋白谱;2)LASSO回归筛选特征蛋白;3)ELISA验证临床样本标志物表达;4)弹性蛋白酶诱导的小鼠AAA模型;5)单细胞RNA测序分析组织细胞亚群。
Olink蛋白质组学揭示血清炎症特征
研究团队通过高灵敏度的Olink炎症面板检测,在AAA患者中发现38个差异表达蛋白(DEPs),其中26个上调(如IL-6、CXCL10)、12个下调。GO分析显示这些蛋白显著富集于细胞因子-细胞因子受体相互作用通路和JAK-STAT信号通路。
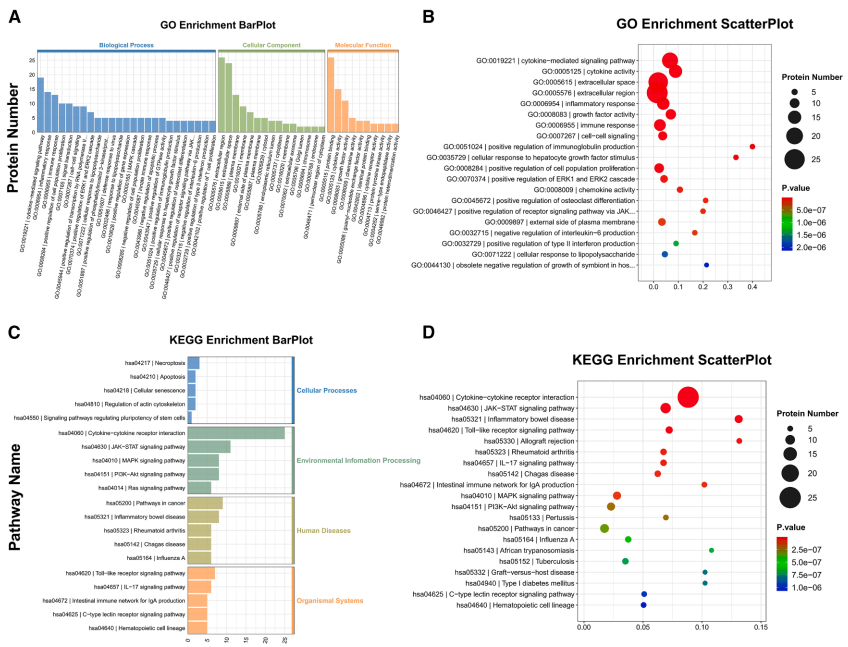
TNFRSF9与IL-6的协同诊断价值
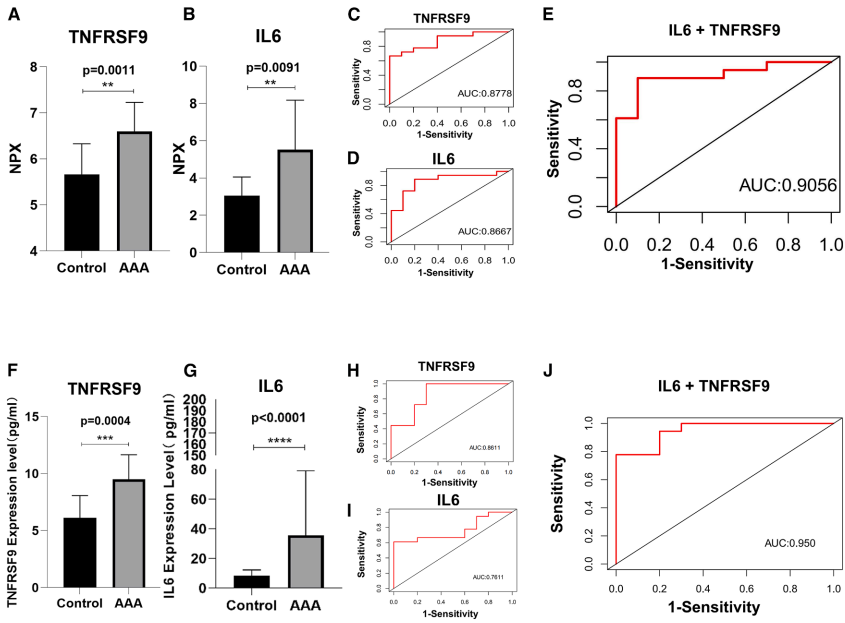
LASSO回归筛选出的13个特征蛋白与GSE183464转录组数据交叉验证,锁定TNFRSF9和IL-6在mRNA和蛋白水平均显著上调。ROC分析显示两者联合诊断效能显著优于单一指标(Olink AUC=0.9056;ELISA AUC=0.95)。
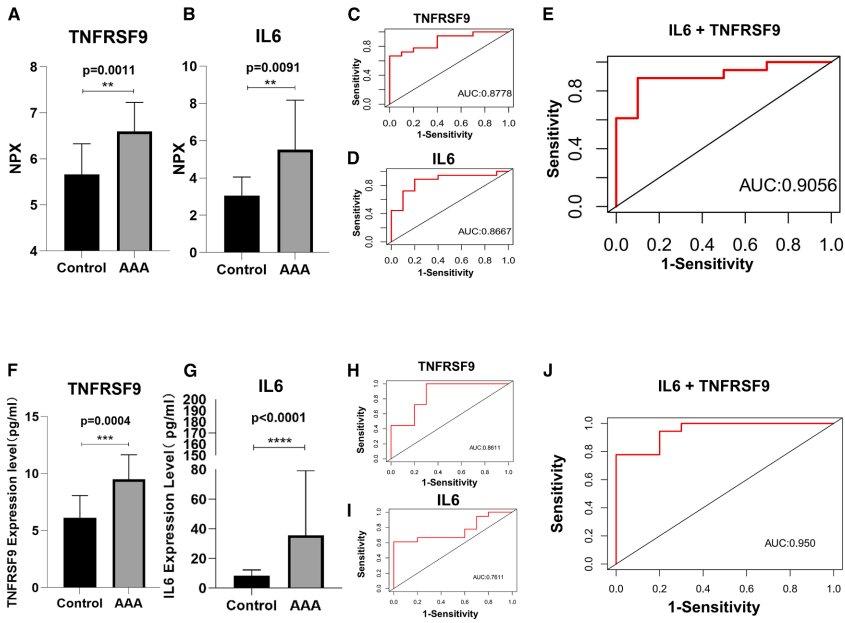
动物模型验证TNFRSF9作用机制
在弹性蛋白酶+BAPN诱导的小鼠AAA模型中,血清TNFRSF9水平较对照组升高3.2倍(p<0.01)。免疫组化和Western blot证实其在主动脉壁表达增加,单细胞测序显示Tnfrsf9主要富集于病变组织的T细胞亚群。
这项研究首次建立TNFRSF9与AAA的关联,其重要意义体现在三方面:1)提供新型血清诊断组合,弥补影像学检查的局限性;2)揭示T细胞通过TNFRSF9参与血管壁炎症的新机制;3)为开发靶向免疫调节疗法提供理论依据。值得注意的是,虽然TNFRSF9在肿瘤免疫治疗领域已被广泛研究,但其在心血管疾病中的作用仍是全新发现。研究也存在样本量较小、未纳入其他血管疾病对照等局限,未来需要通过多中心队列验证这一标志物的特异性。
从临床转化角度看,这种基于Olink技术的标志物筛选策略,为其他缺乏诊断标志物的疾病研究提供了范式。特别是TNFRSF9作为可溶性受体,可能比细胞因子更稳定,更适合临床检测。该研究不仅为AAA早期筛查带来希望,其发现的炎症网络更为靶向治疗研发指明方向――或许未来通过阻断TNFRSF9信号通路,就能遏制AAA的致命性进展。
 生物通微信公众号
生物通微信公众号
知名企业招聘