
-

生物通官微
陪你抓住生命科技
跳动的脉搏
miR-217通过调控OPG/RANKL/RANK通路参与绝经后骨质疏松症进展的机制研究
【字体: 大 中 小 】 时间:2025年06月19日 来源:Journal of Orthopaedic Surgery and Research 2.8
编辑推荐:
本研究针对绝经后骨质疏松症(PMO)的发病机制,揭示了miR-217通过靶向抑制OPG表达,进而调控OPG/RANKL/RANK信号通路影响骨代谢平衡的关键作用。研究人员通过MC3T3-E1细胞模型和OVX大鼠实验证实,抑制miR-217可显著促进成骨分化、改善骨代谢指标,为PMO治疗提供了新的分子靶点。
骨骼健康如同一座精密的建筑,需要成骨细胞与破骨细胞的动态平衡来维护。然而女性绝经后雌激素水平骤降,这座"建筑"便面临崩塌风险――绝经后骨质疏松症(Postmenopausal Osteoporosis, PMO)随之而来。这种以骨量减少、骨微结构破坏为特征的疾病,每年导致数百万女性发生脆性骨折,严重威胁生命质量。尽管现有治疗手段能缓解症状,但探索更精准的分子机制仍是当务之急。近年来,微小RNA(miRNA)作为基因表达的精细调控者,在骨代谢领域崭露头角,其中miR-217的生物学功能尚存争议,其在PMO中的作用更是一片未知的蓝海。
南京中医药大学附属第一医院的研究团队在《Journal of Orthopaedic Surgery and Research》发表的研究,如同解开了一把关键锁匙。研究人员首先构建了MC3T3-E1细胞分化模型和卵巢切除(OVX)大鼠模型,采用实时定量PCR(RT-qPCR)、Western blot(WB)、双荧光素酶报告基因等技术,系统揭示了miR-217通过OPG/RANKL/RANK轴调控PMO进展的分子机制。
主要技术方法
研究采用小鼠成骨细胞系MC3T3-E1进行体外实验,通过转染miR-217模拟物/抑制剂调控基因表达;建立OVX大鼠模型模拟PMO,通过尾静脉注射antagomiR进行干预。关键技术包括:RT-qPCR检测miRNA/mRNA表达、CCK-8和流式细胞术分析细胞增殖凋亡、双荧光素酶验证miR-217与OPG的靶向关系、ELISA检测血清骨代谢标志物(BALP/PINP/CTX-I)及WB分析NF-κB/MAPK通路蛋白磷酸化水平。
研究结果
细胞分化中的表达规律
RT-qPCR显示,随着MC3T3-E1细胞成骨分化,miR-217表达呈时间依赖性下降(***
p<0.001),而Runx2、ALP、Osterix等成骨标志基因表达显著升高(*
p<0.05)。这提示miR-217可能作为负向调控因子参与成骨分化进程。
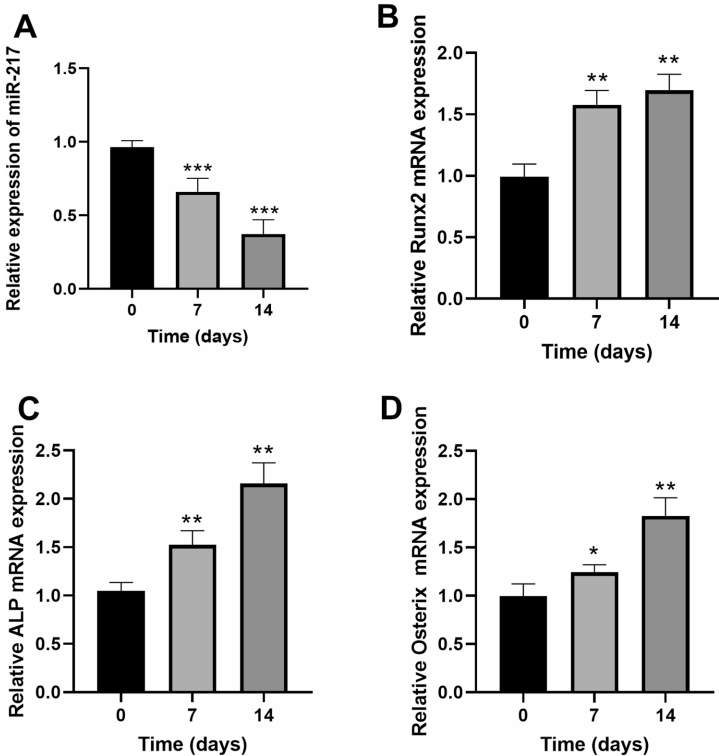
miR-217的细胞功能调控
过表达miR-217使MC3T3-E1细胞增殖率降低28.5%(
p<0.01),凋亡率增加2.1倍;而抑制miR-217则显著促进增殖并抑制凋亡(*
p<0.001)。成骨分化实验进一步证实,miR-217模拟物组Runx2表达量仅为对照组的43%(**
p<0.01),抑制剂组则升高至1.8倍。
OPG的靶向验证
生物信息学预测结合双荧光素酶实验证实,miR-217通过"5'-UCACAGCA-3'"序列特异性结合OPG mRNA的3'UTR(**
p<0.01)。WB显示miR-217过表达使OPG蛋白水平降低61%(*
p<0.05),这种调控可被si-OPG逆转。

动物模型验证
OVX大鼠血清miR-217水平较假手术组升高3.2倍(*
p<0.001),而antagomiR干预使其骨密度(BMD)回升21%(
p<0.01)。机制上,miR-217抑制通过上调OPG使RANKL/RANK比值降低47%(
p<0.01),同时p-p38/p38和p-NF-κB/NF-κB磷酸化水平显著下降(
p<0.01)。
研究结论与意义
该研究首次阐明miR-217在PMO中通过"miR-217→OPG↓→RANKL/RANK↑→NF-κB/MAPK激活"的分子轴促进骨丢失。创新性发现包括:① 确立miR-217作为成骨分化负调控因子的新功能;② 揭示OVX大鼠中miR-217通过靶向OPG破坏骨代谢平衡;③ 提出抑制miR-217可同时改善成骨分化与抑制破骨活性的双重作用。这些发现不仅为PMO的分子诊断提供潜在标志物,更开辟了基于miRNA的精准治疗新思路。
值得注意的是,研究也存在模型单一(仅MC3T3-E1细胞)、未验证Wnt/β-catenin等其他通路等局限。未来需要开展临床样本验证和药物递送系统研究,推动miR-217抑制剂向临床转化。正如作者所言,这项研究为破解"绝经后骨代谢失衡"这一世纪难题提供了新的理论支点。
 生物通微信公众号
生物通微信公众号
知名企业招聘