
-

生物通官微
陪你抓住生命科技
跳动的脉搏
术前BMI与肺癌肺叶切除术后总体死亡率的关系:一项基于限制性立方样条模型的预后分析
《World Journal of Surgical Oncology》:Relationship between preoperative body mass index and overall mortality in patients who have undergone lobectomy for lung cancer
【字体: 大 中 小 】 时间:2025年06月19日 来源:World Journal of Surgical Oncology 2.4
编辑推荐:
本研究针对肺癌肺叶切除患者的预后优化问题,通过回顾性队列分析(N=2365)探讨术前BMI与总体死亡率的关系。采用限制性立方样条(RCS)模型发现BMI在23.2-29.4区间时死亡率最低(HR 0.889),为临床营养干预提供了精准靶点。
在全球癌症负担中,肺癌死亡率持续高居首位,而中国更是肺癌新发病例和死亡病例的"双料冠军"。尽管肺叶切除术是早期肺癌的标准治疗方式,但患者预后改善长期停滞不前――这背后隐藏着一个关键矛盾:大多数已知预后因素(如年龄、分期)难以干预,而可调控的指标却缺乏精准指导。其中,术前营养状态作为潜在的可调节因素,其代表性指标BMI(身体质量指数)的临床意义充满争议:传统观点认为"正常BMI最安全",但"肥胖悖论"现象提示适度超重可能反而改善生存。
中国科学技术大学附属第一医院胸外科团队在《World Journal of Surgical Oncology》发表的研究,首次通过大样本队列(2009-2019年2365例肺叶切除术患者)结合限制性立方样条(RCS)建模,揭示了BMI与肺癌术后死亡率的J型曲线关系。研究创新性地发现:当BMI维持在23.2-29.4(亚洲标准超重范围)时,患者死亡风险最低(HR 0.889),突破了对"正常BMI范围"的传统认知。
关键技术方法
研究团队采用多中心回顾性队列设计,从3869例肺癌根治术患者中筛选出符合标准的2365例肺叶切除病例。通过医院数据库获取BMI、FEV1
%(肺功能指标)等临床数据,运用Kaplan-Meier生存分析和多变量Cox回归模型评估预后因素。核心创新是采用4节点RCS模型拟合BMI与死亡率的非线性关系,并针对性别、年龄、分期(早期/晚期)、术后辅助化疗(PAC)等关键变量进行分层分析。
主要研究结果
1. 背景特征
队列中71%患者为正常BMI(18.5-24.9),但超重组(25.0-29.9)5年死亡率最低(19.7% vs 正常组24.6%)。值得注意的是,肥胖组(BMI≥30)死亡率仅15.5%,显著低于体重不足组(30.6%)。
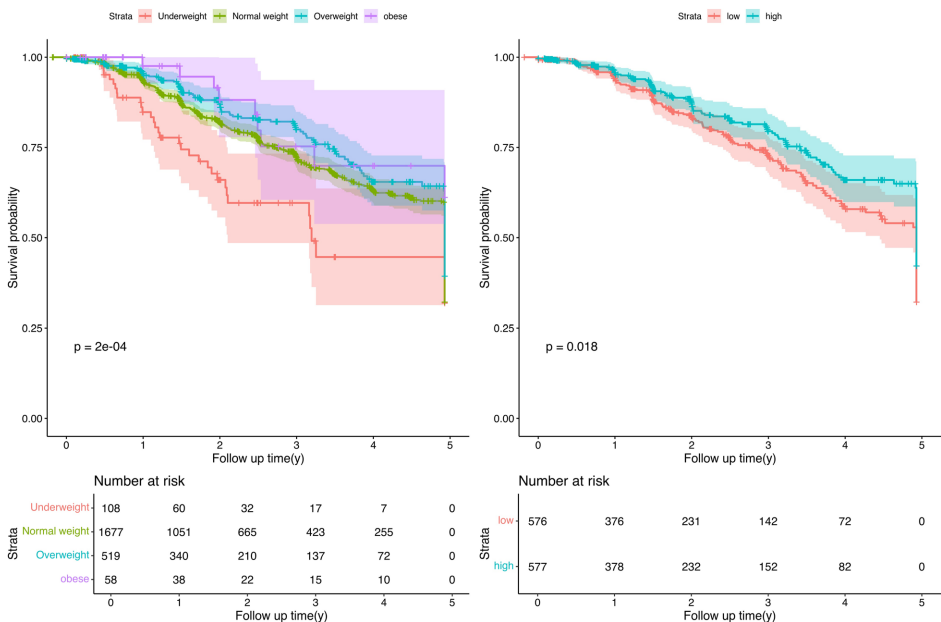
2. BMI与生存率关系
经倾向评分匹配消除年龄混杂后,超重/肥胖组生存优势仍然显著(p=0.018)。多变量分析确认BMI是独立预后因子(VIF<5),与年龄、分期、FEV1
%共同构成预后模型。
3. RCS模型揭示J型曲线
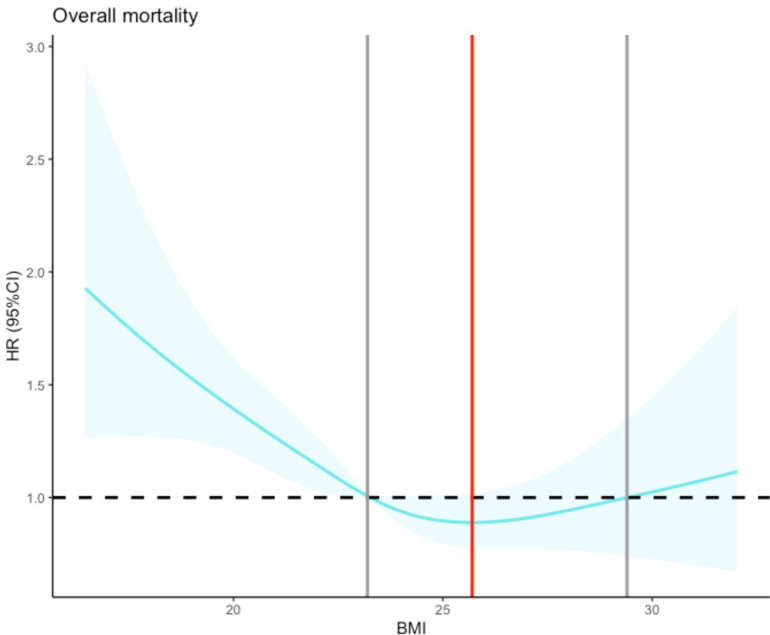
4. 亚组分析
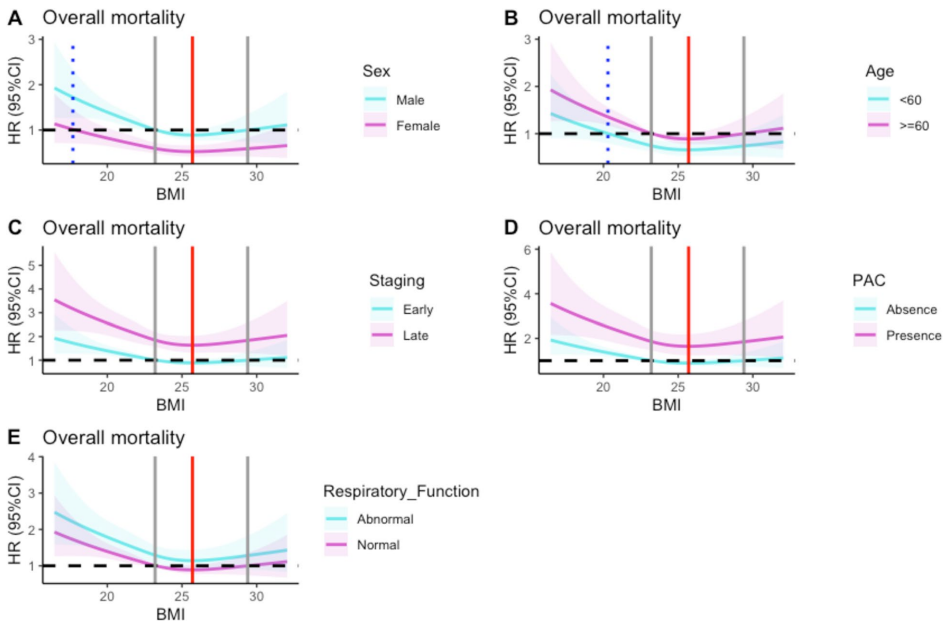
结论与意义
该研究首次量化了肺癌肺叶切除术后BMI的"黄金区间"(23.2-29.4),为临床营养干预提供循证依据:
这项研究将营养状态从模糊的"达标"概念推进到精准调控阶段,为改善肺癌预后开辟了可操作的新路径。
 生物通微信公众号
生物通微信公众号