
-

生物通官微
陪你抓住生命科技
跳动的脉搏
肠道菌群饮食指数与睡眠障碍对糖尿病及前期患者生存预后的联合影响研究
【字体: 大 中 小 】 时间:2025年06月19日 来源:Nutrition Journal 4.4
编辑推荐:
本研究针对糖尿病及前期患者死亡率风险问题,通过分析美国国家健康与营养调查(NHANES)数据,首次探讨了肠道菌群饮食指数(DI-GM)与睡眠障碍的联合预后效应。研究发现高DI-GM(≥6)联合无睡眠障碍可显著降低全因死亡率(HR 0.53)和心血管疾病死亡率(HR 0.36),为糖尿病管理提供了"饮食-睡眠"双重干预新策略。该成果发表于《Nutrition Journal》,对制定个性化干预方案具有重要临床意义。
糖尿病已成为全球重大公共卫生挑战,美国约38%成年人处于糖尿病前期状态。这类人群不仅面临血糖代谢异常,还普遍存在肠道菌群失调和睡眠障碍问题。既往研究多聚焦单一因素干预,但肠道菌群通过微生物群-肠-脑轴(Microbiota-Gut-Brain Axis)与睡眠形成复杂互作网络,二者如何协同影响糖尿病预后尚不明确。更关键的是,新近提出的肠道菌群饮食指数(DI-GM)能否通过调节菌群改善预后,以及与睡眠障碍是否存在联合效应,都是亟待解答的科学问题。
青岛大学附属医院内分泌科Wang Yangang团队基于NHANES 2007-2018数据,创新性地将DI-GM与睡眠障碍纳入联合分析。这项覆盖10,718名糖尿病及前期患者(加权人口67,232,394)的研究发现,DI-GM≥6且无睡眠障碍的患者全因死亡风险降低47%,心血管死亡风险降低64%。相关成果为糖尿病综合管理提供了重要循证依据。
研究采用多中心横断面设计,数据源自NHANES 2007-2018周期,关联2019年国家死亡指数记录。通过24小时饮食回忆计算DI-GM评分(包含14种有益/有害菌群的食物成分),睡眠障碍通过标准化问卷评估。采用加权Cox比例风险模型分析联合效应,并针对年龄、性别、BMI等变量进行多因素校正。队列中位随访6.4年,记录1,448例死亡事件。
【基线特征】
研究纳入人群平均年龄57.0岁,女性占51.8%。DI-GM≥6分组呈现"三高"特征:高龄(58.9岁)、女性比例高(53.9%)、非西班牙裔白人占比高(56.1%)。该组睡眠障碍发生率最低(31.6% vs 37.0% in DI-GM 0-3组),且正常睡眠时长(7-9h)比例最高(63.3%)。

【单独效应分析】
每增加1分DI-GM,全因死亡风险降低6%(HR 0.94),心血管死亡风险降低9%(HR 0.91)。其中有益菌群食物成分(如全谷物、发酵乳制品等)贡献显著,风险降幅达16-19%。睡眠障碍使全因死亡风险增加28%(HR 1.28),心血管死亡风险增加44%(HR 1.44)。
【联合效应】
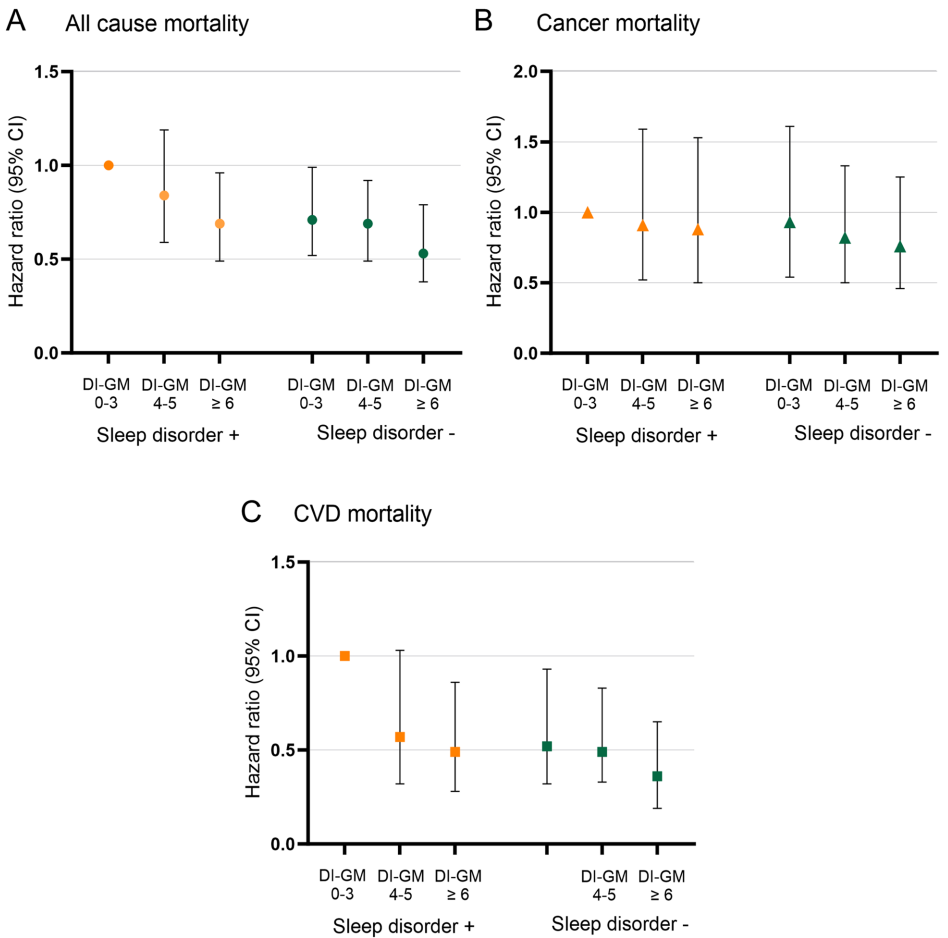
DI-GM≥6联合无睡眠障碍组展现出最佳预后:
• 全因死亡率:HR 0.53(95%CI 0.38-0.79)
• 心血管死亡率:HR 0.36(95%CI 0.19-0.65)
这种保护效应在糖尿病前期人群中更为显著,心血管死亡风险降低达68%(HR 0.32)。
【机制探讨】
研究揭示了可能的生物学通路:DI-GM中的膳食纤维经菌群发酵产生短链脂肪酸(SCFAs),通过激活G蛋白偶联受体(GPR43/GPR109A)改善胰岛素敏感性;而睡眠障碍导致致病菌(如肠杆菌科)增殖,通过迷走神经影响γ-氨基丁酸(GABA)受体表达,加剧糖代谢紊乱。二者协同作用于微生物群-肠-脑轴,形成恶性循环。
该研究首次证实DI-GM与睡眠障碍对糖尿病预后的协同影响,为临床制定"饮食-睡眠"双重干预策略提供了循证依据。特别值得注意的是,这种联合效应在糖尿病前期阶段更为显著,提示早期干预的重要性。未来研究可进一步探索特定菌株(如乳酸杆菌JB1)的干预价值,以及通过膳食调节睡眠节律的可行性。这些发现对完善糖尿病防治指南具有重要实践意义,也为个性化医疗提供了新思路。
 生物通微信公众号
生物通微信公众号
知名企业招聘