
-

ЩњЮяЭЈЙйЮЂ
ХуФузЅзЁЩњУќПЦММ
ЬјЖЏЕФТіВЋ
ЛљгкФЩУзПЙЬхЕФгЋЙтДуУ№ЬхгХЛЏВпТдЃКЬсЩ§ЕААзжЪМьВтСщУєЖШЕФДДаТЦНЬЈ
ЁОзжЬхЃК Дѓ жа аЁ ЁП ЪБМфЃК2025Фъ06дТ20Ше РДдДЃКCommunications Biology 5.2
БрМЭЦМіЃК
ЁЁЁЁБОбаОПеыЖдДЋЭГЕААзжЪМьВтЗНЗЈЖЏЬЌЗЖЮЇгаЯоЕФЮЪЬтЃЌЭЈЙ§РэадЩшМЦгыЗжзгЖЏСІбЇФЃФтЯрНсКЯЃЌПЊЗЂГіаТаЭФЩУзПЙЬхгЋЙтДуУ№ЬхЃЈQuenchbodyЃЉжЇМмЁЃбаОПШЫдБдкЛЅВЙОіЖЈЧјЃЈCDRЃЉв§ШыЙиМќЩЋАБЫсВаЛљЃЌЭЈЙ§ЬхЭтЖЈЯђНјЛЏЩИбЁЛёЕУеыЖдбзжЂвђзгIL-6ЕФИпадФмМьВтЬНеыЃЌЪЕЯж1.5-2.4БЖгЋЙтдіЧПКЭ1-2 nMМьВтЯоЁЃИУГЩЙћЮЊЩњЮяДЋИаЦїПЊЗЂЬсЙЉСЫЭЈгУЦНЬЈЃЌдкМВВЁеяЖЯКЭЛЗОГМрВтСьгђОпгаживЊгІгУМлжЕЁЃ
дкЩњЮявНбЇМьВтСьгђЃЌЕААзжЪБъжОЮяЕФОЋзМЪЖБ№гЬШчДѓКЃРЬеыЁЃДЋЭГжЪЦзММЪѕЫфЮЊН№БъзМЃЌШДЪмЯогкЩшБИХгДѓЁЂСїГЬИДдгЃЛЖјELISAЕШУтвпЗжЮіЗЈЫфМђБуПьЫйЃЌЕЋашвЊЗБЫіЕФЯДЕгВНжшКЭПЙЬхХфЖдЁЃИќСюШЫРЇШХЕФЪЧЃЌЯжгагЋЙтДуУ№ЬхЃЈQuenchbodyЃЉММЪѕЖдЕААзжЪПЙдЕФМьВтЖЏЬЌЗЖЮЇНі1.1-1.4БЖЃЌдЖВЛФмТњзуСйДВашЧѓЁЃетОЭЯёФУзХЗХДѓОЕбАевЮЂЩњЮяЃЌЙЄОпБОЩэЕФОжЯоШУживЊаХКХфЮУЛдкдыЩљжаЁЃ
еыЖдетвЛММЪѕЦПОБЃЌгЩАФДѓРћбЧбаОПЭХЖгСьЯЮЕФЙњМЪКЯзїаЁзщдкЁЖCommunications BiologyЁЗЗЂБэЭЛЦЦадГЩЙћЁЃбаОПШЫдБЖРБйѕшОЖЃЌНЋФПЙтЭЖЯђТцЭедДФЩУзПЙЬхЁЊЁЊетжжЗжзгСПНі15 kDaЕФЮЂаЭПЙЬхЃЌОпгаЮШЖЈадИпЁЂвзИФдьЕШЖРЬигХЪЦЁЃЭЈЙ§ЯЕЭГадИФдьЦфЛЅВЙОіЖЈЧјЃЈCDRЃЉЕФЩЋАБЫсЭјТчЃЌЭХЖгЙЙНЈГіаТвЛДњгЋЙтДуУ№ЬхжЇМмЃЌГЩЙІНЋМьВтСщУєЖШЬсЩ§жСаТИпЖШЁЃ
баОПВЩгУШ§ДѓЙиМќММЪѕЃКЗжзгЖЏСІбЇФЃФтЃЈ72 ІЬsзмЪБГЄЃЉНтЮігЋЙтЭХ-ЩЋАБЫсЯрЛЅзїгУЛњжЦЃЛЯИАћгЮРыБэДяЯЕЭГЪЕЯж24аЁЪБФкЭъГЩФЩУзПЙЬхЕФБэДяЁЂБъМЧгыДПЛЏЃЛЮЂЕЮАќЙќЕФSNAPеЙЪОММЪѕНјааЖЈЯђНјЛЏЩИбЁЃЌЭЈЙ§ЮхТжбЁдёЛёЕУИпадФмЭЛБфЬхЁЃетаЉЗНЗЈЕФДДаТзщКЯЮЊЕААзжЪМьВтММЪѕПЊБйСЫаТТЗОЖЁЃ
<ЙиМќЗЂЯж>
ЁОIn silico evaluation of de novo quenchbody modelsЁП
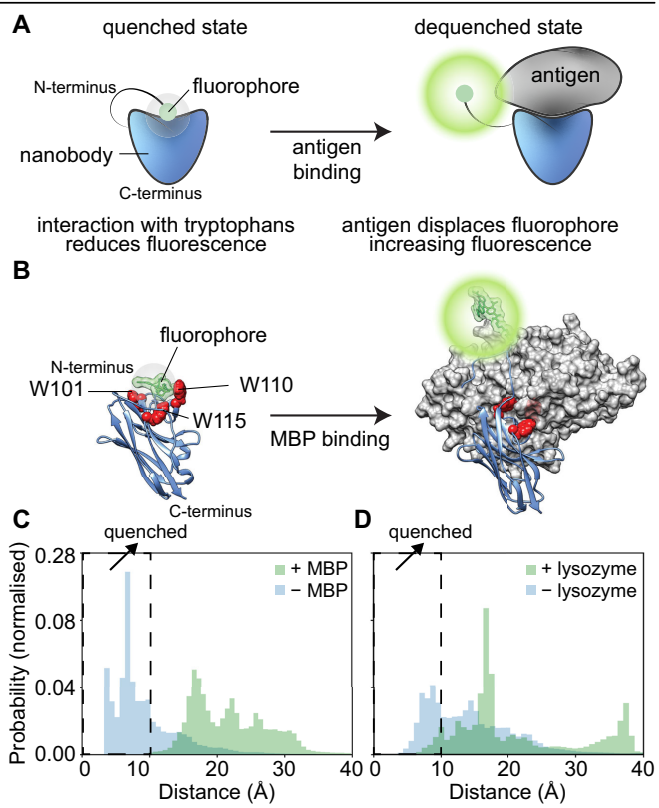
ЗжзгЖЏСІбЇФЃФтНвЪОЃКТѓбПЬЧНсКЯЕААзЃЈMBPЃЉФЩУзПЙЬхжаЃЌW110КЭW115дкЮДНсКЯзДЬЌЪБ70.7%ЪБМфгыгЋЙтЭХОрРыЁм10 ?ЃЌЖјПЙдНсКЯКѓжшНЕжС0.1%ЁЃШмОњУИФЩУзПЙЬхдђЯдЪОW103ЪЧжївЊДуУ№ЮЛЕуЃЌЦфЭЛБфЬхЃЈW103YЃЉгЋЙтЯьгІНЕЕЭ50%ЁЃетаЉЗЂЯжШчЭЌЗжзгГпЃЌОЋШЗеЩСПГіЙиМќЩЋАБЫсЕФПеМфЗжВМЙцТЩЁЃ
ЁОIn vitro production and biochemical characterisation of quenchbodiesЁП
ЪЕбщбщжЄЯдЪОЃЌгХЛЏКѓЕФQb-MBPКЭQb-LysЗжБ№ЪЕЯж1.5БЖКЭ1.3БЖгЋЙтдіЧПЃЌМьВтЯоДя4 nMКЭ1 nMЁЃEC50жЕгыЬьШЛФЩУзПЙЬхЧзКЭСІЯрЕБЃЈ14 nM vs 24 nMЃЛ7 nM vs 60 nMЃЉЃЌжЄЪЕгЋЙтБъМЧВЛгАЯьПЙдНсКЯФмСІЁЃ

ЁОCDR-tryptophans underpin the quenchbody sensing mechanismЁП
ЭЛБфЪЕбщжЄЪЕCDR1-Y110WЕЅЕуЭЛБфЪЙШмОњУИМьВтаХКХЬсЩ§жС1.7БЖЃЛЖјMBPФЩУзПЙЬхЕФY59W/Y114WЫЋЭЛБфЬхИќДя1.9БЖЁЃетаЉЪ§ОнШчЭЌЗжзгУмТыЃЌЦЦвыГіЩЋАБЫсЭјТчЕФзюгХХХСазщКЯЁЃ

ЁОIn vitro evolution of CDR-tryptophan quenchbodies for IL-6 detectionЁП
ЖЈЯђНјЛЏЛёЕУЕФIL-6МьВтЬНеыБэЯжОЊбоЃКБфЬх#15ЕФEC50=20 nMЃЌПЩМьВт1 nMХЈЖШЃЛБфЬх#35ИќДДЯТ2.4БЖгЋЙтдіЧПМЧТМЁЃетаЉЭЛЦЦадНјеЙЪЙМьВтСщУєЖШНгНќСйДВашЧѓуажЕЁЃ

<ПЦбЇвтвхгыеЙЭћ>
етЯюбаОПЕпИВСЫДЋЭГscFv/FabДуУ№ЬхЕФЩшМЦЗЖЪНЃЌЪзДЮВћУїФЩУзПЙЬхCDRЩЋАБЫсжБНгВЮгыПЙдНчУцДуУ№ЕФаТЛњжЦЁЃЫљНЈСЂЕФ"ЭЙУцЖрЩЋАБЫс"жЇМмШчЭЌЗжзгРжИпЃЌЮЊПьЫйПЊЗЂИїРрЕААзжЪМьВтЬНеыЬсЙЉЭЈгУЦНЬЈЁЃЫфШЛФПЧАЖдIL-6ЕФМьВтЯоЃЈ1-2 nMЃЉОрЩњРэХЈЖШЃЈ5.2 pg/mLЃЉШдгаВюОрЃЌЕЋЭЈЙ§КѓајЧзКЭСІГЩЪьЛђЫЋДуУ№ЬхВпТдЃЌгаЭћЪЕЯжХЇЖОжЂЕШМВВЁЕФМДЪБеяЖЯЁЃИќжЕЕУЦкД§ЕФЪЧЃЌИУММЪѕТЗЯпЭъШЋАкЭбЖЏЮяУтвпЯожЦЃЌЪЕЯжШЋКЯГЩЩњВњЃЌЮЊгІЖдЭЛЗЂДЋШОВЁЬсЙЉММЪѕДЂБИЁЃ
етЯюГЩЙћгЬШчЮЊЕААзжЪМьВтСьгђАВзАЩЯЗжзгЗХДѓЦїЃЌЦфвтвхВЛНідкгкММЪѕВЮЪ§ЕФЬсЩ§ЃЌИќПЊДДСЫ"МЦЫуЩшМЦ+ЖЈЯђНјЛЏ"ЕФаЭЌбаЗЂаТФЃЪНЁЃЫцзХГЌДуУ№ЬхЃЈUltra QuenchbodyЃЉЕШаТИХФюЕФв§ШыЃЌЮДРДЛђНЋМћжЄ50БЖгЋЙтдіЧПЕФФЩУзЬНеыЮЪЪРЃЌзюжеЪЕЯж"ЛьдШМДЖС"ЕФжеМЋМьВтУЮЯыЁЃ
 ЩњЮяЭЈЮЂаХЙЋжкКХ
ЩњЮяЭЈЮЂаХЙЋжкКХ
жЊУћЦѓвЕеаЦИ
НёШеЖЏЬЌ | ШЫВХЪаГЁ | аТММЪѕзЈРИ | жаЙњПЦбЇШЫ | дЦеЙЬЈ | BioHot | дЦНВЬУжБВЅ | ЛсеЙжааФ | ЬиМлзЈРИ | ММЪѕПьбЖ | УтЗбЪдгУ
АцШЈЫљга ЩњЮяЭЈ
Copyright© eBiotrade.com, All Rights Reserved
СЊЯЕаХЯфЃК
дСICPБИ09063491КХ