
-

生物通官微
陪你抓住生命科技
跳动的脉搏
人骨髓类器官研究:突破性进展与持续挑战
【字体: 大 中 小 】 时间:2025年06月21日 来源:TRENDS IN Biotechnology 14.3
编辑推荐:
为解决人类骨髓微环境体外建模难题,研究人员聚焦诱导多能干细胞(iPSC)来源的骨髓类器官(BMO)开发。通过中胚层诱导建立具有间充质-血管-造血三重特征的类胎儿组织,揭示了早期造血过程的调控机制。尽管在模拟成人骨髓功能方面仍存局限,该研究为血液发育、疾病建模及细胞治疗提供了创新平台。
骨髓研究的"迷你革命":从干细胞到类器官的突破
在生命科学领域,人类骨髓一直是个令人着迷又充满挑战的研究对象。这个隐藏在骨骼深处的柔软组织,每天产生约5000亿个血细胞,维持着我们的生命运转。然而,科学家们长期面临一个困境:如何在实验室里准确模拟这个复杂的微环境?传统二维培养系统无法再现骨髓的三维结构和细胞互作,而动物模型又存在物种差异。这种技术瓶颈严重阻碍了对血液疾病机制的理解和新型疗法的开发。
瑞典隆德大学的研究团队在《TRENDS IN Biotechnology》发表观点文章,系统评述了人骨髓类器官(Bone Marrow Organoids, BMO)领域的最新进展。通过整合多学科方法,研究人员利用诱导多能干细胞(iPSC)成功构建了包含间充质、血管和造血组分的三维模型,为破解骨髓发育密码提供了全新工具。这项研究标志着组织工程和再生医学的重要里程碑。
关键技术方法
研究采用iPSC中胚层诱导技术,结合血管内皮生长因子(VEGF)、骨形态发生蛋白4(BMP4)和β成纤维细胞生长因子(βFGF)的时序刺激,在2周内形成胚胎样体。通过胶原蛋白与基质胶(Geltrex)的3D培养体系,建立了具有自组织能力的组织块。单细胞转录组分析和功能验证揭示了类器官的细胞组成与功能特征。
研究结果
中胚层诱导作为生物工程原理
三项独立研究[12,13,15]均采用iPSC中胚层诱导策略,通过模拟胚胎发育过程获得造血内皮细胞。该方法在2周内形成直径800-1300μm的组织块,包含间充质、血管和造血三种核心组分。值得注意的是,不同实验室使用多种iPSC系均能获得成分相似的结构,证明了方法的可重复性。
形成具有有限干细胞功能的类胎儿组织
血管系统:所有BMO均形成密集的窦状血管网络,表达CD31、PDGRβ和CD34等标志物。Frenz-Wiessner等[13]还鉴定出前小动脉组分(CDH5+/PECAM+),证实了血管连接宿主循环系统的能力。
间充质组分:BMO包含LeptinR+/PDGFRα+的基质细胞,分泌CXCL12等造血支持因子。但与成人骨髓不同,这些细胞更接近胎儿间充质干细胞(MSC),缺乏成骨细胞和脂肪细胞。植入实验显示其无法通过软骨内骨化形成成熟骨组织。
造血组分:单细胞分析显示BMO主要包含巨核细胞-红系-巨噬细胞祖细胞(EMP),符合原始造血特征。Frenz-Wiessner模型[13]虽检测到类似成人造血干细胞(HSC)的群体,但缺乏HOXA基因特征,移植后仅实现短期造血重建。
当前BMO系统的前景与局限
模拟人类造血发生的平台
这些BMO为研究内皮-造血转化(Endothelial-to-Hematopoietic Transition, EHT)提供了独特模型。特别是Frenz-Wiessner系统[13]可追踪粒细胞分化过程,为理解谱系决定机制开辟新途径。
模拟成人骨髓的持续挑战
由于BMO重现的是胎儿而非成人造血特征,其在血液恶性肿瘤建模中的应用受限。Khan等[12]尝试将BMO与患者CD34+细胞共培养,虽可维持部分白血病细胞存活,但预测性仍需验证。单基因病VPS45模型[13]虽成功模拟儿童期骨髓纤维化,但难以复现成人白血病的复杂突变谱。
潜在技术路径

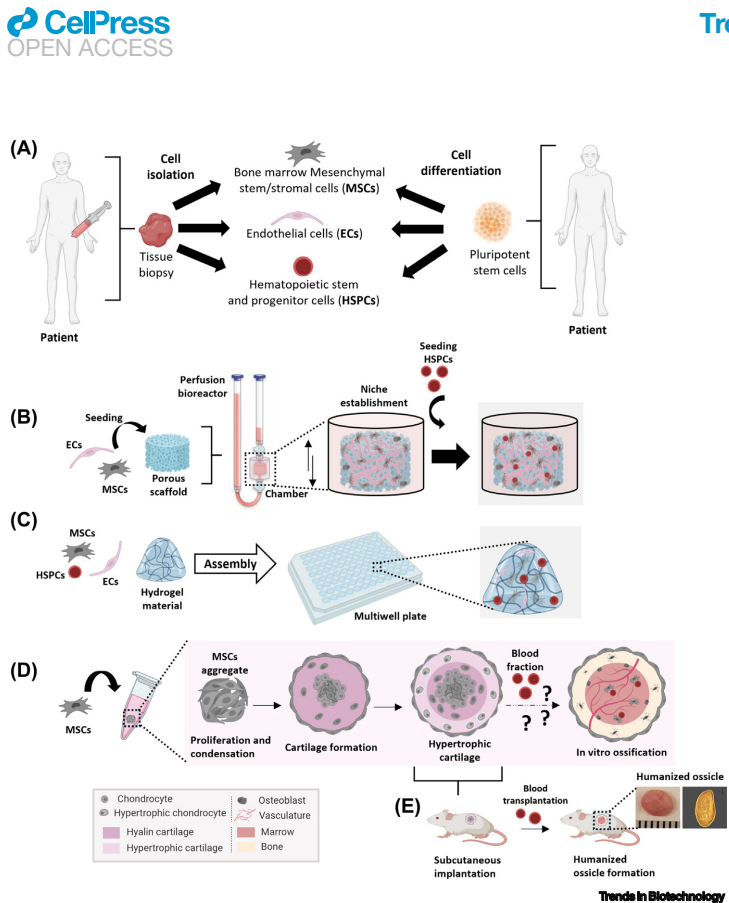
文章探讨了四种替代策略:(1)生物反应器构建的仿生骨髓类似物;(2)水凝胶微阵列培养系统;(3)体外软骨内骨化途径模拟;(4)人源化骨小体技术。其中,皮下植入工程化软骨形成"骨小体"的方法[34]目前最能模拟成人骨髓微环境,但存在人鼠细胞嵌合的技术瓶颈。
结论与展望
Paul E. Bourgine团队指出,现有BMO在模拟早期造血方面取得突破,但距离重建成人骨髓仍有差距。核心挑战在于血液发生学(hematopoiesis)的复杂性――从原始造血到确定造血的多阶段转换尚未在体外完全重现。未来研究需聚焦三个方向:(1)优化培养条件获得功能性HSC;(2)开发无血清定义化培养基;(3)整合时空调控信号模拟骨髓区域化特征。这项研究不仅为血液疾病机制研究提供新工具,更启示了通过发育工程(developmental engineering)构建复杂器官的可能。
随着技术的进步,BMO有望成为"个性化医疗芯片",实现从疾病建模到药物筛选的一体化平台。正如作者所言,这场"骨髓迷你革命"才刚刚开始,其最终目标不仅是复制自然,更是超越自然――在培养皿中创造比原生更可控、更透明的生命系统。
 生物通微信公众号
生物通微信公众号
知名企业招聘