
-

ЙъОпНЁ№ЩОў
ЕгДгЧҘЧЎЙъГьҝЖјј
Мш¶ҜөДВцІ«
Л«НјХэФт»ҜјҜіЙС§П°ҝтјЬSMODELЈәҝХјд¶аЧйС§КэҫЭЦРҝХјдУтҪвОцөДРВ·¶КҪ
ЎҫЧЦМеЈә ҙу ЦР РЎ Ўҝ КұјдЈә2025Дк06ФВ22ИХ АҙФҙЈәCommunications Biology 5.2
ұајӯНЖјцЈә
ЎЎЎЎұҫСРҫҝХл¶ФҝХјд¶аЧйС§КэҫЭПЎКиРФәН·ЦІјТмЦКРФДСМвЈ¬Мбіц»щУЪЛ«НјХэФт»ҜГӘөгёЕДо·ЦҪвөДјҜіЙС§П°ҝтјЬSMODELЎЈНЁ№эФӘЛШј¶јУИЁјҜіЙІЯВФХыәП¶а»щҫЫАаҪб№ыЈ¬ҪбәПҝХјдО»ЦГФјКшУлёЯҪЧНШЖЛРЕПўЈ¬іЙ№ҰКөПЦИЛАаБЬ°НҪбЎўИйПЩ°©ЧйЦҜөИёҙФУОў»·ҫіЦРҝХјдУтөДҫ«ЧјК¶ұрЈ¬ОӘҪвОцПё°ыТмЦКРФМṩРВ№ӨҫЯЎЈ
ҝХјдЙъОпС§өДРВН»ЖЖЈәSMODELЛг·ЁИзәОЦШЛЬ¶аЧйС§ХыәП·ЦОц
ЛжЧЕҝХјдЧӘВјЧйЈЁspatial transcriptomicsЈ©ЎўҝХјдұн№ЫЧйЈЁspatial epigenomicsЈ©өИјјКхөДҝмЛЩ·ўХ№Ј¬ҝЖС§јТГЗөГТФФЪұЈБфПё°ыҝХјдО»ЦГРЕПўөДН¬Кұ»сИЎ¶аО¬·ЦЧУМШХчЎЈИ»¶шЈ¬КэҫЭПЎКиРФЎўјјКхФлЙщТФј°ДЈМ¬јд·ЦІјІоТмЈ¬СПЦШЧи°ӯБЛ¶ФЧйЦҜОў»·ҫіЦРПё°ыТмЦКРФөДПөНіҪвОцЎЈҙ«НіөҘПё°ы¶аЧйС§ХыәП·Ҫ·ЁЈЁИзscVIЎўMultiVIЈ©НщНщәцКУҝХјдРЕПўЈ¬¶шПЦУРҝХјд·ЦОц·Ҫ·ЁЈЁИзSpatialGlueЎўPRAGAЈ©УЦДСТФЖҪәвјЖЛгР§ВКУлЙъОпС§ҪвКНРФЎЈ
ОӘҪвҫцХвТ»МфХҪЈ¬ЙоЫЪҙуС§өДСРҫҝНЕ¶УФЪЎ¶Communications BiologyЎ··ўұнМвОӘ"Unveiling spatial domains from spatial multi-omics data using dual-graph regularized ensemble learning"өДСРҫҝВЫОДЈ¬ҝӘ·ўіцSMODELЈЁSpatial Multi-Omics Domain Ensemble LearningЈ©Лг·ЁҝтјЬЎЈёГСРҫҝНЁ№эҙҙРВРФөШИЪәПГӘөгёЕДо·ЦҪвЈЁanchor concept factorizationЈ©УлЛ«НјХэФт»ҜФјКшЈ¬КЧҙОКөПЦҝХјд¶аЧйС§КэҫЭөДОИҪЎјҜіЙУлҝЙКУ»ҜҪвОцЎЈ
№ШјьјјКх·Ҫ·Ё
СРҫҝНЕ¶УІЙУГИэҪЧ¶ОјјКхВ·ПЯЈә1Ј©»щУЪk-meansөДГӘөгСЎФсУл·ЗёәҫШХу·ЦҪв№№ҪЁҝзЧйС§өНО¬ұнХчЈ»2Ј©ТэИлФӘЛШј¶јУИЁІЯВФЈЁelement-wise weightingЈ©ХыәПSeuratЎўMOFA+өИ7ЦЦ»щҫЫАаҪб№ыЈ»3Ј©НЁ№эҝХјдО»ЦГНјЈЁEuclidean distance-based graphЈ©УлёЯҪЧ»ҘРЕПўНјЈЁPMI matrixЈ©өДЛ«ЦШФјКшЈ¬ұЈБфЧйЦҜҪб№№өДјёәОБчРОМШХчЎЈКөСйСйЦӨәӯёЗИЛАаБЬ°НҪбЈЁVisiumЖҪМЁЈ©ЎўРЎКуИйПЩ°©ЈЁMMTV-PyMTДЈРНЈ©ј°ДЈДвИэЧйС§КэҫЭЈ¬ІЙУГNMIЎўARIөИ8ПоЖА№АЦёұкЎЈ
СРҫҝҪб№ы
»щЧјІвКФСйЦӨРФДЬУЕКЖ
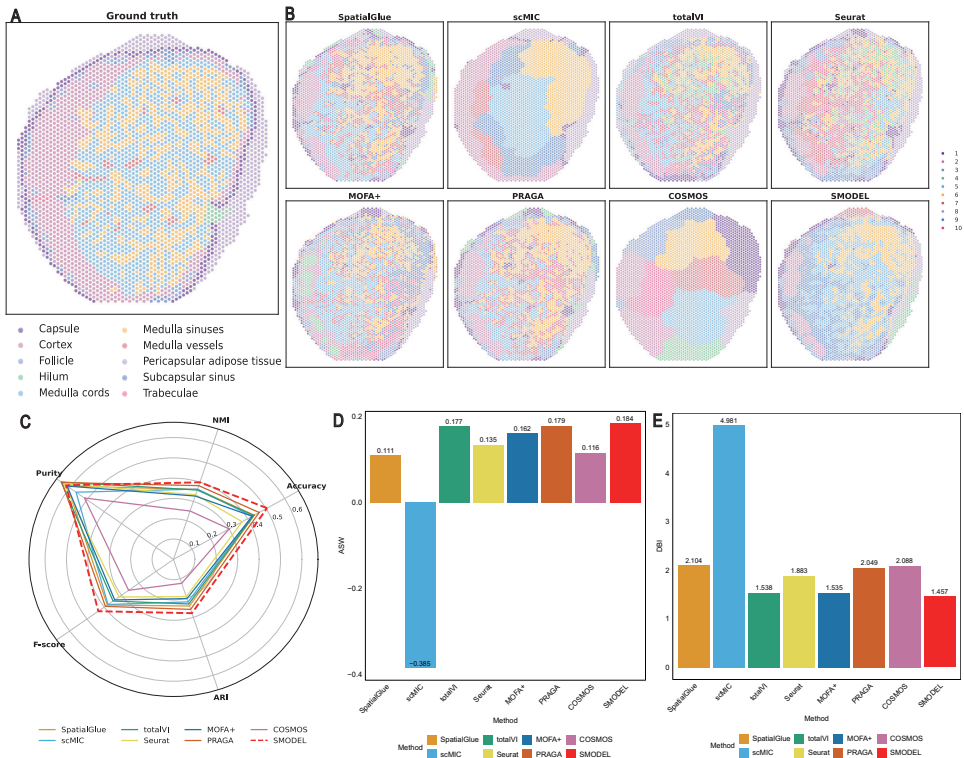
ФЪИЛАаБЬ°НҪбСщұҫA1өД10АаҪб№№ЧўКНЦРЈ¬SMODELЧјИ·К¶ұрұ»ДӨЈЁcapsuleЈ©ЎўЖӨЦКЈЁcortexЈ©әНЛиЛчЈЁmedulla cordsЈ©өИ№ШјьЗшУтЈЁНј2BЈ©ЎЈ¶ЁБҝЖА№АПФКҫЖдASWЦөҙп0.184ЈЁНј2DЈ©Ј¬DBIЦёКэ1.457ЈЁНј2EЈ©Ј¬ҫщПФЦшУЕУЪSpatialGlueөИ»щПЯ·Ҫ·ЁЎЈ
ИйПЩ°©Оў»·ҫіҪвОц
УҰУГЦБ1978ёцspotsөДИйПЩ°©КэҫЭКұЈ¬SMODELіЙ№ҰІ¶»сM2РНҫЮКЙПё°ыМШХчЈЁArg1+Ј©ФЪЦЧБцұЯҪзөДГвТЯТЦЦЖРФ·ЦІјЈЁНј3AЈ©ЎЈЙъҙж·ЦОцПФКҫЖдјш¶ЁөДSvoplЈЁp<0.05Ј©УлSerpini1ЈЁp<0.05Ј©·ЦұрЧчОӘАЦ№Ы/ұҜ№ЫФӨәуұкЦҫОпЈЁНј3D-EЈ©Ј¬ІўНЁ№эJAK-STAT3НЁВ·ІыКНLeprөчҝШөДM2ј«»Ҝ»ъЦЖЈЁНј3FЈ©ЎЈ
ұн№Ы-ЧӘВјЧйРӯН¬·ЦОц
ФЪРЎКуДФҝХјдATAC-RNA-seqКэҫЭЦРЈ¬SMODELЗеОъЗш·ЦЖӨІгЈЁCTXЈ©·ЦІгҪб№№УлОЖЧҙМеЈЁStrЈ©Ј¬ФцЗҝPde10aЈЁОЖЧҙМеЈ©ЎўMbpЈЁлЭлХМеЈ©өИЗшУтМШТмРФ»щТтұнҙпРЕәЕЈЁНј4CЈ©ЎЈ
ИэЧйС§ХыәПДЬБҰ
ДЈДвКөСйЦӨГчSMODELҝЙЧФККУҰ·ЦЕдRNAЈЁ50.5%Ј©ЎўATACЈЁ30.7%Ј©ЎўADTЈЁ9.5%Ј©өДДЈМ¬ИЁЦШЈЁНј5CЈ©Ј¬ФЪ90%ПЎКи¶ИПВИФұЈіЦОИ¶ЁРФЈЁІ№ідНј5Ј©ЎЈ
ҪбВЫУлХ№Ны
ёГСРҫҝҝӘҙҙРФөШҪ«јҜіЙС§П°ТэИлҝХјд¶аЧйС§·ЦОцЈ¬ЖдҙҙРВРФМеПЦФЪЈә1Ј©НЁ№эГӘөгёЕДо·ЦҪвҪвҫцДЈМ¬ТмЦКРФЈ»2Ј©АыУГЛ«НјХэФт»ҜұЈБфҝХјдНШЖЛҪб№№Ј»3Ј©ФӘЛШј¶јУИЁІЯВФМбЙэ»щҫЫАаҝЙҝҝРФЎЈФЪБЬ°НҪбЛиЦКҪб№№К¶ұрЎўИйПЩ°©ГвТЯОў»·ҫіҪвОцөИіЎҫ°ЦРХ№ПЦіці¬ФҪПЦУР·Ҫ·ЁөДРФДЬЈ¬ОӘЦЧБцГвТЯЦОБЖ°Рөг·ўПЦЈЁИзLepr-STAT3ЦбЈ©МṩРВЛјВ·ЎЈОҙАҙҝЙНЁ№эХыәПH&EНјПсКэҫЭУлБ¬РшЗРЖ¬·ЦОцЈ¬ҪшТ»ІҪНШХ№ЖдФЪБЩҙІЧӘ»ҜЦРөДУҰУГјЫЦөЎЈ
 ЙъОпНЁОўРЕ№«ЦЪәЕ
ЙъОпНЁОўРЕ№«ЦЪәЕ
ЦӘГыЖуТөХРЖё
ҪсИХ¶ҜМ¬ | ИЛІЕКРіЎ | РВјјКхЧЁАё | ЦР№ъҝЖС§ИЛ | ФЖХ№МЁ | BioHot | ФЖҪІМГЦұІҘ | »бХ№ЦРРД | МШјЫЧЁАё | јјКхҝмС¶ | Гв·СКФУГ
°жИЁЛщУР ЙъОпНЁ
Copyright© eBiotrade.com, All Rights Reserved
БӘПөРЕПдЈә
ФБICPұё09063491әЕ