
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:铜死亡:肺癌中的一种新型治疗机制
【字体: 大 中 小 】 时间:2025年06月26日 来源:Cancer Cell International 5.3
编辑推荐:
这篇综述系统阐述了铜死亡(Cuproptosis)这一新型铜依赖性细胞死亡机制在肺癌治疗中的潜力。文章详细解析了铜稳态(Copper homeostasis)失衡与肺癌发生发展的关联,重点探讨了铜转运蛋白(CTR1/ATP7A/B)、铜伴侣蛋白(ATOX1/CCS/COX17)及关键调控基因(FDX1/LIPT1)的作用机制,并总结了铜离子载体(Elesclomol/Disulfiram)和铜螯合剂(ATTM/TETA)等靶向诱导铜死亡的临床转化前景,为肺癌治疗提供了新策略。
肺癌作为全球癌症相关死亡的首要原因,其治疗面临转移、复发和耐药等挑战。近年研究发现,铜离子浓度与肺癌进展呈正相关,而铜死亡――一种依赖线粒体呼吸和铜离子积累的新型细胞死亡方式,为肺癌治疗提供了全新视角。
细胞内铜浓度通过精密系统维持平衡:
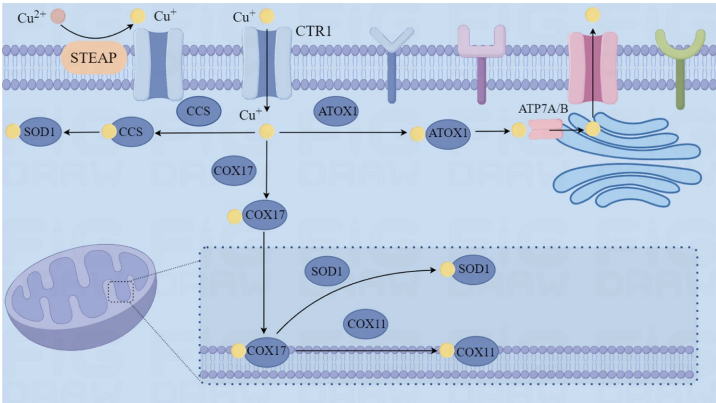
铜死亡区别于凋亡、坏死性凋亡等其他程序性死亡方式,其核心特征包括:
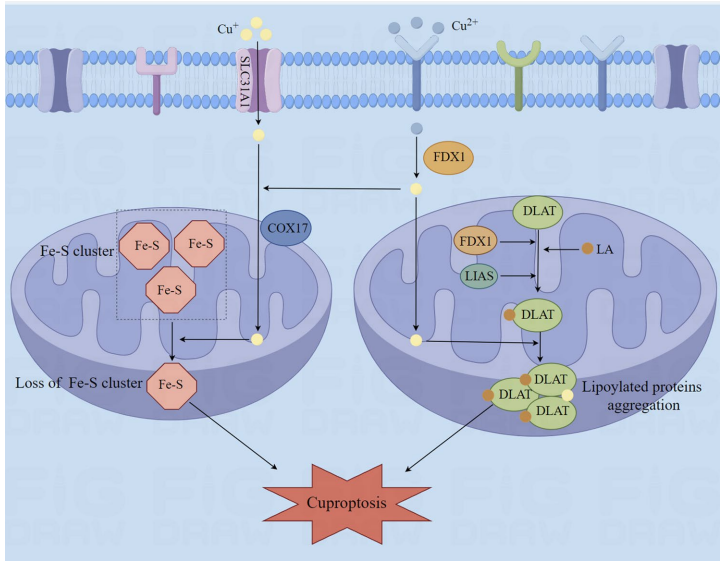
肺癌组织中存在显著铜代谢异常:
尽管铜死亡为肺癌治疗带来突破,但仍需解决:
该领域研究将推动肺癌精准治疗的发展,为改善患者预后提供新思路。
 生物通微信公众号
生物通微信公众号
知名企业招聘