
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:ASXL1、SRSF2和EZH2突变在骨髓增生异常肿瘤和急性髓系白血病染色质失调中的作用
【字体: 大 中 小 】 时间:2025年06月26日 来源:Leukemia 12.8
编辑推荐:
这篇综述系统阐述了ASXL1、SRSF2和EZH2基因突变通过破坏组蛋白修饰(H2AK119ub/H3K27me3)和RNA剪接机制,驱动骨髓增生异常肿瘤(MDS)和急性髓系白血病(AML)发生的分子机制。作者强调这些突变作为不良预后标志物,与表观遗传调控异常(如PRC2/PR-DUB复合物功能失调)和剪接体缺陷(如EZH2 mRNA毒外显子插入)密切相关,并探讨了 Venetoclax联合去甲基化药物等新兴治疗策略的潜力。
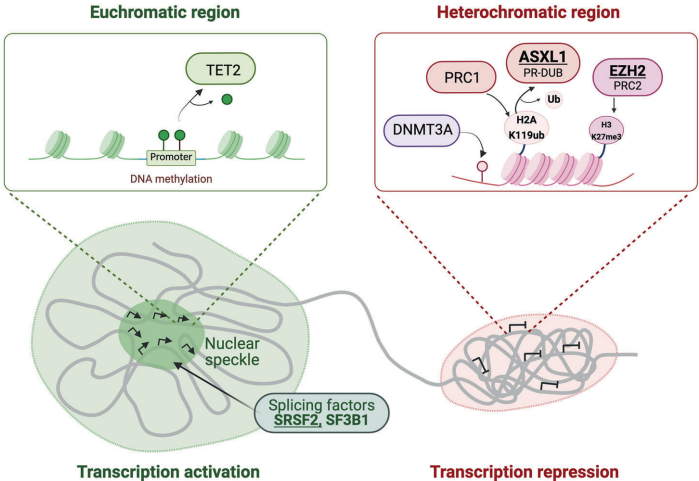
染色质失调是MDS/AML的核心特征,由TET2、DNMT3A、ASXL1和EZH2等表观遗传调控因子突变驱动。这些基因突变频率在MDS中分别达23%、18.4%、18.2%和5.5%,通过破坏DNA甲基化(DNMT3A)与去甲基化(TET2)平衡,以及组蛋白修饰(H3K27me3/H2AK119ub)稳态,导致造血干细胞分化障碍。其中ASXL1作为PR-DUB复合物组分,通过去泛素化H2AK119ub拮抗PRC1介导的基因沉默,而EZH2则是PRC2催化亚基,负责H3K27三甲基化。
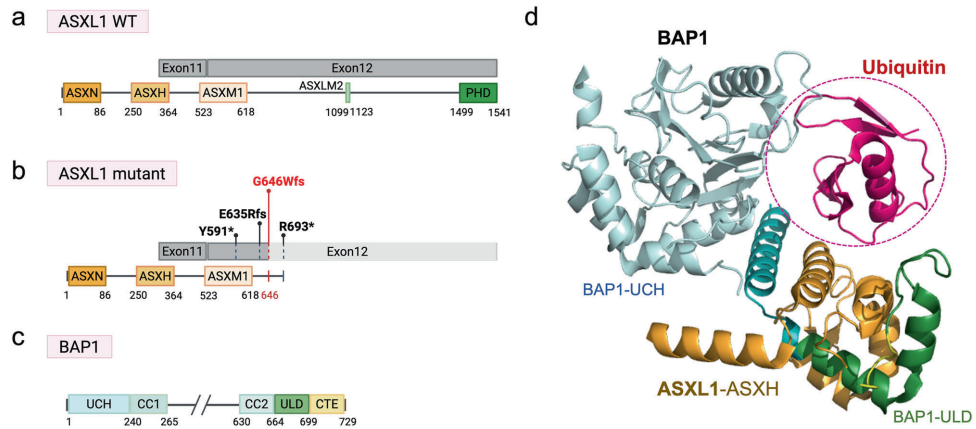
ASXL1突变(如G646Wfs)导致C端截短,虽丧失PHD结构域但意外增强PR-DUB活性。突变体通过抑制多聚泛素化降解,稳定与BAP1的相互作用,进而过度去除H2AK119ub,激活HOXA基因簇(如HOXA9),阻断造血干细胞终末分化。
突变体还表现出独特功能:①减少与PRC2互作,降低H3K27me3水平;②异常结合BRD4,通过P-TEFb促进RNA聚合酶II磷酸化,激活PRDM16等促癌基因;③破坏与NONO蛋白互作,抑制核旁斑(paraspeckle)形成,导致RNA剪接异常。
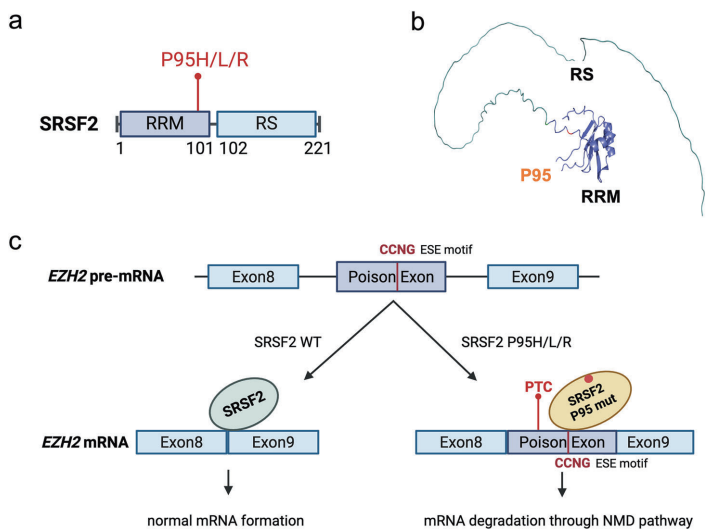
SRSF2 P95H/L/R突变改变RRM结构域RNA结合特异性(从GGNG转向CCNG),诱导EZH2 mRNA毒外显子插入,触发无义介导的mRNA降解(NMD),使EZH2蛋白水平下降50%。类似地,SF3B1 K700E突变导致BRD9毒外显子异常剪接,破坏ncBAF染色质重塑复合体定位。
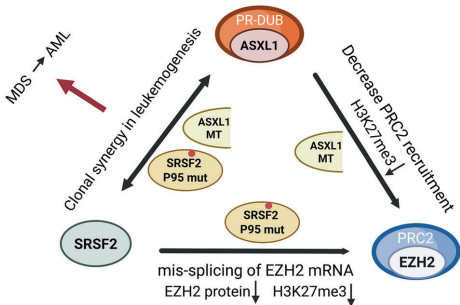
在淋巴瘤中,EZH2 Y646等SET结构域突变(GOF)增强H3K27me3催化活性;而在MDS/AML中,R690/D664突变(LOF)则削弱PRC2功能。这种表观遗传失调与ASXL1突变协同,通过HOXA基因去抑制共同促进白血病转化。
ASXL1/SRSF2共突变患者总生存期显著缩短(图5),ELN-2022指南将其列为高危因素。当前策略包括:①Venetoclax联合去甲基化剂克服SRSF2突变不良预后;②CDK9抑制剂靶向ASXL1突变;③PRMT5抑制剂(如GSK3326595)通过干扰剪接因子甲基化展现潜在疗效。未来需开发直接靶向突变体蛋白(如稳定ASXL1-BAP1互作的小分子)或修复表观遗传失衡的精准疗法。
 生物通微信公众号
生物通微信公众号
知名企业招聘