
-

ЙъОпНЁ№ЩОў
ЕгДгЧҘЧЎЙъГьҝЖјј
Мш¶ҜөДВцІ«
ЧЫКцЈәіҰөАОўЙъОпЧйөДГвТЯөчҪЪМШРФЈә¶ФАа·зКӘРФ№ШҪЪСЧөДХп¶ПәНЦОБЖЗұБҰ
ЎҫЧЦМеЈә ҙу ЦР РЎ Ўҝ КұјдЈә2025Дк07ФВ02ИХ АҙФҙЈәClinical and Experimental Medicine 3.2
ұајӯНЖјцЈә
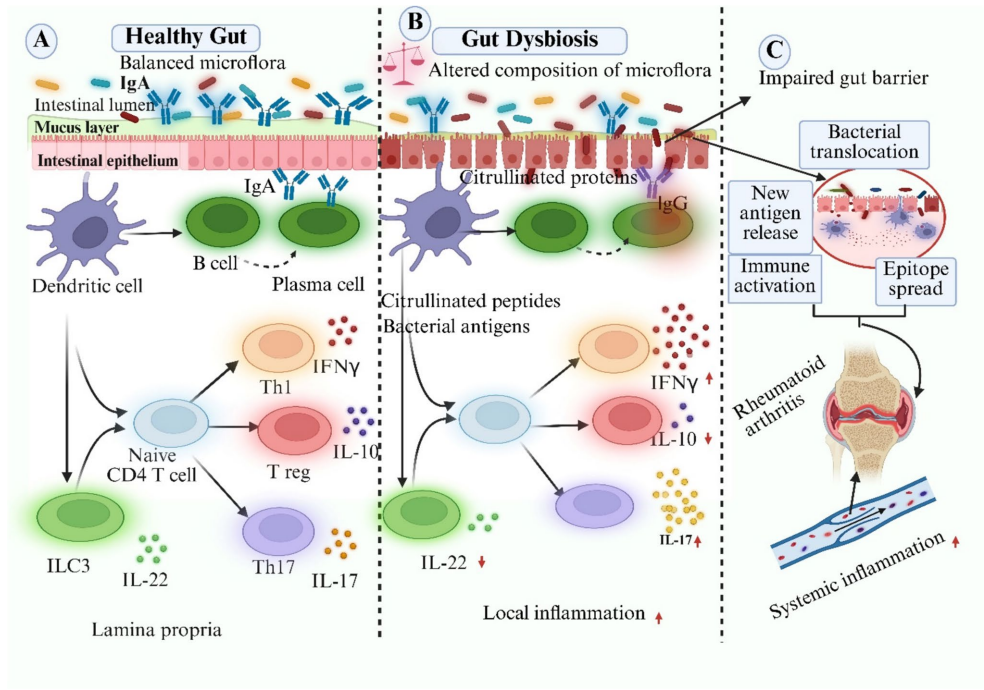
ЎЎЎЎХвЖӘЧЫКцПөНіІыКцБЛіҰөАОўЙъОпЧйЈЁgut microbiomeЈ©НЁ№эГвТЯөчҪЪ»ъЦЖУ°ПмАа·зКӘРФ№ШҪЪСЧЈЁRAЈ©·ўЙъ·ўХ№өДЧоРВСРҫҝҪшХ№Ј¬ЦШөгМҪМЦБЛОўЙъОпК§өчЈЁdysbiosisЈ©Ўў¶МБҙЦ¬·ҫЛбЈЁSCFAsЈ©ҙъР»ТміЈУлTh17/TregПё°ыК§әвөД№ШБӘЈ¬ІўМбіцБЛ»щУЪТжЙъҫъЈЁprobioticsЈ©Ўў·аҫъТЖЦІЈЁFMTЈ©әНҙ«НіЦРТ©ЈЁTCMЈ©өД°РПтёЙФӨІЯВФЈ¬ОӘRAөДҫ«ЧјХпБЖМṩБЛРВЛјВ·ЎЈ
Аа·зКӘРФ№ШҪЪСЧЈЁRAЈ©КЗТ»ЦЦТФ№ШҪЪ»¬ДӨФцЙъЎўИн№ЗЖЖ»өәНПөНіРФСЧЦўОӘМШХчөДВэРФЧФЙнГвТЯІЎЈ¬И«Зт»јІЎВКФј0.5%-1.0%Ј¬Е®РФ·ўІЎВКПФЦшёЯУЪДРРФЎЈҫЎ№ЬЙъОпЦЖјБЈЁbDMARDsЈ©әНTNF-ҰБТЦЦЖјБөДУҰУГёДЙЖБЛ60-70%»јХЯөДФӨәуЈ¬ИФУР30-40%»јХЯТтБЖР§І»Чг»тёұЧчУГНЈТ©ЎЈҪьДкСРҫҝ·ўПЦЈ¬іҰөАҫъИәК§өчНЁ№э·ЦЧУДЈДвЎўЖБХПЖЖ»өәНҙъР»ОпОЙВТөИ»ъЦЖЗэ¶ҜRA·ўІЎЈ¬іЙОӘН»ЖЖЦОБЖЖҝҫұөДРВ°РөгЎЈ
ҪЎҝөіҰөАҫъИәНЁ№э·ЦГЪ¶МБҙЦ¬·ҫЛбЈЁSCFAsЈ©ИзТТЛбЈЁacetateЈ©ЎўұыЛбЈЁpropionateЈ©әН¶ЎЛбЈЁbutyrateЈ©Ј¬ҙЩҪшөчҪЪРФTПё°ыЈЁTregЈ©·Ц»ҜІўТЦЦЖTh17Пё°ы№э¶И»о»ҜЈ¬О¬іЦГвТЯОИМ¬ЎЈ¶шRA»јХЯЖХұйҙжФЪЖХАЧОЦҫъЈЁPrevotella copriЈ©·б¶ИЙэёЯЎўЛ«ЖзёЛҫъЈЁBifidobacteriumЈ©әН·аёЛҫъЈЁFaecalibacteriumЈ©јхЙЩөДМШХчРФК§әвЎЈ¶ҜОпКөСйПФКҫЈ¬ТЖЦІRA»јХЯ·аұгөДРЎКуіҰөАTh17Пё°ыА©ФцЈ¬¶Ф60SәЛМЗМеө°°ЧL23AЈЁRPL23AЈ©өДIL-17·ҙУҰФцЗҝЈ¬№ШҪЪСЧЦўЧҙјУЦШЎЈ
ОўЙъОпұкЦҫОпЈә
ҙъР»ОпұкЦҫОпЈә
ТжЙъҫъЈә
·аҫъТЖЦІЈә
ҙ«НіЦРТ©Јә
іҰөАҫъИә-ГвТЯЦбОӘRAМṩБЛҙУФзЖЪХп¶ПөҪёцМе»ҜЦОБЖөДИ«РВКУҪЗЎЈө«РиҪшТ»ІҪГчИ·ҫъЦкМШТмРФЧчУГЈЁИзP. copriУлP. histicolaөДПа·ҙР§УҰЈ©Ј¬УЕ»ҜFMT·Ҫ°ёЈ¬ІўМҪЛчОўЙъОпҙъР»ОпЈЁИз5-HIAAЈ©НЁ№э·јПгМюКЬМеЈЁAhRЈ©өчҝШBregПё°ыөД·ЦЧУ»ъЦЖЎЈХыәП¶аЧйС§КэҫЭәНБЩҙІКФСйҪ«НЖ¶ҜОўЙъОп°РПтБЖ·ЁЧЯПтБЩҙІЧӘ»ҜЎЈ
 ЙъОпНЁОўРЕ№«ЦЪәЕ
ЙъОпНЁОўРЕ№«ЦЪәЕ
ЦӘГыЖуТөХРЖё
ҪсИХ¶ҜМ¬ | ИЛІЕКРіЎ | РВјјКхЧЁАё | ЦР№ъҝЖС§ИЛ | ФЖХ№МЁ | BioHot | ФЖҪІМГЦұІҘ | »бХ№ЦРРД | МШјЫЧЁАё | јјКхҝмС¶ | Гв·СКФУГ
°жИЁЛщУР ЙъОпНЁ
Copyright© eBiotrade.com, All Rights Reserved
БӘПөРЕПдЈә
ФБICPұё09063491әЕ