
-

ЩњЮяЭЈЙйЮЂ
ХуФузЅзЁЩњУќПЦММ
ЬјЖЏЕФТіВЋ
ЛљгкЛњЦїбЇЯАЕФЗЪХжгыЫЅРЯЯрЙиЬиеїЦздЄВтЮИЯйАЉдЄКѓМАУтвпжЮСЦЛёвц
ЁОзжЬхЃК Дѓ жа аЁ ЁП ЪБМфЃК2025Фъ07дТ02Ше РДдДЃКDiscover Oncology 2.8
БрМЭЦМіЃК
ЁЁЁЁБОбаОПеыЖдЮИЯйАЉ(STAD)дЄКѓдЄВтКЭУтвпжЮСЦЯьгІЦРЙРЕФСйДВФбЬтЃЌЩЧЭЗДѓбЇвНбЇдКИНЪєЕквЛвНдКЭХЖгЭЈЙ§ећКЯTCGAКЭGEOЖрзщбЇЪ§ОнЃЌдЫгУ10жжЛњЦїбЇЯАЫуЗЈЙЙНЈСЫЗЪХжгыЫЅРЯЯрЙиЬиеїЦз(ORS)ЁЃбаОПЗЂЯжLASSOЫуЗЈПЊЗЂЕФ4Лљвђ(DPSYL4/NR3C1/HTRA3/BGN)ФЃаЭдЄВтаЇФмзюгХ(C-index=0.81)ЃЌЕЭORSзщЛМепБэЯжГіИќЧПЕФУтвпЯИАћНўШѓЁЂИќИпЕФPD1/CTLA4УтвпБэаЭЦРЗжКЭжзСіЭЛБфИККЩ(TMB)ЃЌЧвЖдЛЏСЦвЉЮяУєИаадИќИпЁЃИУбаОПЮЊSTADИіЬхЛЏжЮСЦЬсЙЉСЫаТаЭЗжзгБъжОЮяЁЃ
баОПБГОА
ЮИЯйАЉ(STAD)зїЮЊШЋЧђЕкШ§ДѓАЉжЂЫРвђЃЌЦфИпвьжЪадКЭжЮСЦЕжПЙадЕМжТЛМеп5ФъЩњДцТЪВЛзу30%ЁЃОЁЙмУтвпМьВщЕувжжЦМС(ICI)ЮЊЭэЦкЛМепДјРДЯЃЭћЃЌЕЋЯжгаЩњЮяБъжОЮяШчPD-L1БэДяКЭЮЂЮРаЧВЛЮШЖЈад(MSI)ЕФдЄВтМлжЕгаЯоЁЃгыДЫЭЌЪБЃЌСїааВЁбЇбаОПНвЪОЗЪХж(BMIЁн30)КЭЫЅРЯ(ФъСфЁн65Ыъ)гыSTADВЛСМдЄКѓЯджјЯрЙиЃЌЕЋЦфЗжзгЛњжЦЩаЮДВћУїЁЃ
ММЪѕЗНЗЈ
баОПЭХЖгећКЯTCGA(n=325)КЭ4ИіGEOЪ§ОнМЏ(GSE15459/GSE26253/GSE62254/GSE84437)ЃЌЭЈЙ§limmaАќЩИбЁВювьБэДяЛљвђ(DEGs)ЃЌНсКЯШЫРрЫЅРЯЛљвђзщзЪдДПтКЭMSigDBЪ§ОнПтЛёШЁЗЪХж/ЫЅРЯЯрЙиЛљвђЁЃВЩгУ10жжЛњЦїбЇЯАЫуЗЈЙЙНЈдЄВтФЃаЭЃЌЭЈЙ§СєвЛЗЈНЛВцбщжЄЦРЙРадФмЁЃУтвпНўШѓЗжЮіЪЙгУTIMER/xCellЕШ7жжЫуЗЈЃЌвЉЮяУєИаадЭЈЙ§oncoPredictАќМЦЫуIC50жЕЁЃ
баОПНсЙћ
3.1 ЩњЮяБъжОЮяЩИбЁ
Дг10,757ИіDEGsжаМјЖЈГі76ИіЗЪХж/ЫЅРЯЯрЙиЛљвђЃЌЦфжа9Иі(DPSYL4/NR3C1/HTRA3ЕШ)ОЕЅБфСПCoxЛиЙщЯдЪОдЄКѓМлжЕЁЃ

3.2 ORSФЃаЭЙЙНЈ
LASSOЫуЗЈЙЙНЈЕФ4ЛљвђФЃаЭБэЯжзюгХЃЌЗчЯеЦРЗжЙЋЪНЮЊЃК0.1025ЁСDPYSL4+(-0.1203)ЁСNR3C1+(-0.0985)ЁСHTRA3+0.1865ЁСBGNЁЃИУФЃаЭдкбщжЄМЏжа1/3/5ФъAUCДя0.871/0.803/0.768ЁЃ
3.4 УтвпЮЂЛЗОГЬиеї
ЕЭORSзщЯдЪОCD8+ TЯИАћНўШѓдіМг(Іб=-0.42,p<0.01)ЃЌAPCЙВДЬМЄКЭTЯИАћЛюЛЏЦРЗжЩ§ИпЃЌЧвHLA-DRB1ЕШПЙдГЪЕнЛљвђБэДяЩЯЕїЁЃ

3.5 жЮСЦЯьгІдЄВт
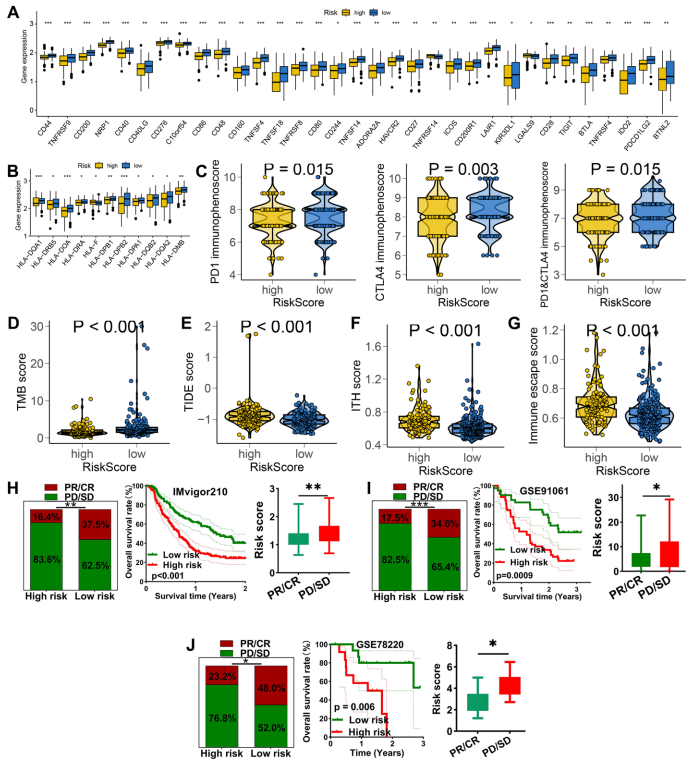
ЕЭORSзщдкIMvigor210ЖгСажаУтвпжЮСЦЯьгІТЪЬсИп2.1БЖ(p<0.01)ЃЌTIDEЦРЗжНЕЕЭ38%ЃЌЭЌЪБЖд5-FU/ЫГВЌЕШЛЏСЦвЉЮяIC50жЕЯджјНЕЕЭЁЃ
3.6 ЙІФмИЛМЏ
ИпORSзщИЛМЏPI3K-AKT-mTORЭЈТЗ(ES=2.31)КЭЩЯЦЄМфжЪзЊЛЏ(EMT)ЬиеїЛљвђЃЌЬсЪОЧБдкжЮСЦАаЕуЁЃ
НсТлгывтвх
ИУбаОПЪзДЮНЈСЂећКЯЗЪХжгыЫЅРЯЬиеїЕФSTADдЄКѓФЃаЭЃЌНвЪОBGNЕШЛљвђЭЈЙ§ЕїПиУтвпЮЂЛЗОГгАЯьжЮСЦЯьгІЁЃСйДВзЊЛЏЗНУцЃЌORSПЩжИЕМICIгУвЉбЁдёЁЊЁЊЕЭORSЛМепПЩФмДгPD-1вжжЦМСжаЛёвцЃЌЖјИпORSЛМепИќЪЪКЯАаЯђPI3KЭЈТЗСЊКЯЛЏСЦЁЃбаОПЮЊSTADОЋзМвНСЦЬсЙЉСЫаТЕФОіВпЙЄОпЃЌЯрЙиГЩЙћЗЂБэгкЁЖDiscover OncologyЁЗЁЃ
 ЩњЮяЭЈЮЂаХЙЋжкКХ
ЩњЮяЭЈЮЂаХЙЋжкКХ
жЊУћЦѓвЕеаЦИ
НёШеЖЏЬЌ | ШЫВХЪаГЁ | аТММЪѕзЈРИ | жаЙњПЦбЇШЫ | дЦеЙЬЈ | BioHot | дЦНВЬУжБВЅ | ЛсеЙжааФ | ЬиМлзЈРИ | ММЪѕПьбЖ | УтЗбЪдгУ
АцШЈЫљга ЩњЮяЭЈ
Copyright© eBiotrade.com, All Rights Reserved
СЊЯЕаХЯфЃК
дСICPБИ09063491КХ