
-

生物通官微
陪你抓住生命科技
跳动的脉搏
中国南方两大前瞻性队列研究揭示EB病毒VCA-IgA抗体与多种癌症风险的显著关联
【字体: 大 中 小 】 时间:2025年07月02日 来源:Nature Communications 14.7
编辑推荐:
本研究针对EB病毒(Epstein-Barr virus, EBV)致癌谱不明确的问题,通过中国南方73,939人的前瞻性队列分析,首次系统评估了VCA-IgA抗体与多种癌症风险的关联。结果显示VCA-IgA血清阳性者总癌症风险增加4.88倍(95%CI:2.84-8.37),其中鼻咽癌风险升高26.05倍,并首次发现与肺癌(HR=1.76)、肝癌(HR=1.70)的显著关联。研究为EBV致癌机制提供了新证据,估算中国南方7.8%的癌症负担可归因于EBV感染,对癌症防控策略具有重要指导意义。
EB病毒(EBV)作为首个被发现的人类致癌病毒,全球约95%人口携带这种"潜伏杀手"。尽管早在1997年就被国际癌症研究机构(IARC)列为I类致癌物,但其致癌谱始终存在巨大争议――传统观点认为EBV仅与鼻咽癌(NPC)、部分淋巴瘤等少数癌症相关,但临床观察和分子研究不断提示其可能参与更广泛的致癌过程。这种认知局限直接影响了癌症防控策略的制定,特别是在中国南方等EBV高流行区,亟需大规模流行病学证据揭示EBV与癌症风险的真正关联。
为破解这一科学难题,中山大学肿瘤防治中心联合梧州市红十字会医院等机构的研究团队开展了一项开创性研究。研究人员利用中国国家癌症筛查项目的资源优势,构建了包含73,939名30-69岁成年人的两大前瞻性队列(中山队列和梧州队列),通过8-10年随访追踪,系统分析了EBV VCA-IgA抗体与癌症风险的关联。这项发表在《Nature Communications》的研究不仅证实了EBV与传统相关癌症的强关联,更首次揭示了其与肺癌、肝癌等常见恶性肿瘤的显著联系,为全面认识EBV致癌作用提供了里程碑式证据。
研究采用多中心前瞻性队列设计,关键技术方法包括:1) 建立中山(n=29,026)和梧州(n=44,913)两大区域代表性队列,通过标准化问卷采集基线数据;2) 采用ELISA(中山)和免疫酶法(梧州)检测血清VCA-IgA抗体水平;3) 通过癌症登记系统年度随访确认964例(中山)和1026例(梧州)新发癌症病例;4) 应用Cox比例风险模型评估风险比(HR),计算人群归因风险百分比(PARP);5) 对部分肺癌(n=129)和肝癌(n=348)组织进行EBER原位杂交验证病毒存在。
队列特征与基线分析
中山队列中6.6%参与者VCA-IgA血清阳性,梧州队列为5.6%。多变量分析显示,年龄增长、男性、低教育程度和吸烟与血清阳性率显著正相关,而较高BMI呈负相关。这种风险模式提示EBV活性可能受宿主免疫状态和行为因素调控。
癌症标准化发病率
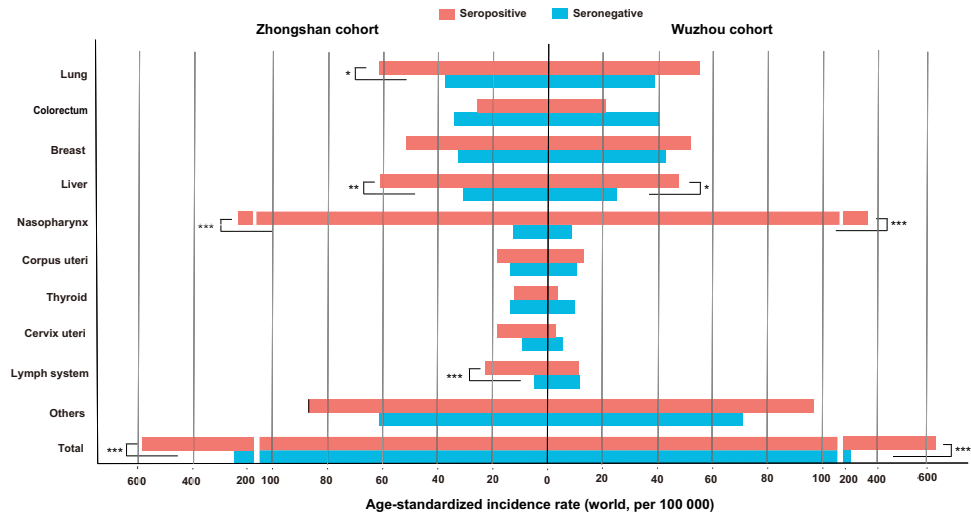
VCA-IgA阳性组总癌症年龄标准化发病率(ASR)显著高于阴性组:中山队列(592.73 vs 253.77/10万人年,P=1.32×10-9),梧州队列(650.10 vs 262.45,P=2.81×10-11)。除预期的鼻咽癌差异外,中山队列阳性组肺癌(62.75 vs 37.16)、肝癌(60.65 vs 31.30)和淋巴瘤(22.67 vs 5.39)的ASR均显著升高。
癌症风险关联分析
汇总分析显示VCA-IgA阳性者风险显著增加:总癌症(HR=4.88,95%CI:2.84-8.37)、肺癌(1.76,1.23-2.54)、肝癌(1.70,1.10-2.63)、鼻咽癌(26.05,11.77-57.65)和淋巴瘤(3.20,1.46-6.99)。敏感性分析排除随访初期病例后结果保持稳定,证实关联的时序合理性。值得注意的是,VCA-IgA与HBV感染对肝癌风险存在协同效应(交互作用P=0.001),二者共阳性者风险较单阳性显著升高。
剂量反应与时间动态
中山队列中,VCA-IgA抗体水平与总癌症风险呈显著剂量反应关系(P=6.95×10-5)。时间动态分析显示抗体水平升高可预测长达10年后的癌症风险,提示EBV异常活化可能是癌症发生的早期事件。
癌症负担评估
VCA-IgA血清阳性导致58.5%(95%CI:53.3-63.7%)的阳性者癌症发生,人群归因风险百分比(PARP)达7.8%,意味着中国南方约7.8%癌症病例可归因于EBV感染。即使排除鼻咽癌,PARP仍达2.6%,显著高于全球既往估计(1.9%)。
肿瘤组织EBER检测
在129例肺癌和348例肝癌组织中发现低比例(1.1-1.6%)EBER阳性信号,主要位于鳞癌和肝内胆管癌细胞中。这种"稀疏散在"模式支持EBV可能通过"hit-and-run"机制或间接免疫调控参与致癌。
这项研究从根本上拓展了对EBV致癌作用的认识:首先,证实EBV异常活化(VCA-IgA升高)不仅与经典相关癌症有关,还与肺癌、肝癌等常见恶性肿瘤风险显著相关;其次,发现EBV与HBV在肝癌发生中具有协同作用,为多因素致癌机制提供新见解;最重要的是,研究首次量化了中国南方EBV相关癌症负担(PARP 7.8%),这一数据远超预期,对公共卫生策略制定具有重大意义。
讨论部分深入分析了潜在机制:EBV可能通过三种途径参与致癌――直接感染肿瘤细胞(如鼻咽癌)、诱导基因组不稳定性(如EBNA1致11q23断裂)、或通过慢性炎症和免疫逃逸创造促癌微环境。对肺癌、肝癌等EBER低检出癌症,研究者提出"分子痕迹"假说,即EBV可能在肿瘤发生早期起推动作用后消失。这些发现为后续分子机制研究指明了方向,也为开发基于EBV抗体的广谱癌症风险评估工具奠定基础。
研究的创新性在于:1) 首次在前瞻性设计中系统评估EBV与多种癌症关联;2) 采用双队列设计增强结果可靠性;3) 创新性计算PARP量化疾病负担。局限性包括地区特异性(中国南方)、抗体检测方法差异等。未来需要更多族裔队列验证,并探索其他EBV抗体(如EA、EBNA1)的预测价值。这项研究为重新审视EBV在癌症预防中的地位提供了坚实证据,将推动EBV检测纳入癌症风险分层体系,最终实现精准防控。

 生物通微信公众号
生物通微信公众号
知名企业招聘