
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Sintilimab联合安罗替尼与吉西他滨/顺铂治疗晚期胆道癌的随机II期SAGC试验:低剂量抗血管生成方案优化肿瘤微环境并提升疗效
【字体: 大 中 小 】 时间:2025年07月02日 来源:Nature Communications 14.7
编辑推荐:
本研究针对晚期胆道癌(BTC)一线治疗生存获益有限的临床难题,由浙江省肿瘤医院团队开展多中心随机II期SAGC试验,探索PD-1抑制剂(sintilimab)联合抗血管生成药(anlotinib)与化疗(GC方案)的协同疗效。结果显示SAGC组中位无进展生存期(PFS)显著延长至8.5个月(HR 0.48),客观缓解率(ORR)提升至51.4%,且8mg安罗替尼剂量组展现出更优生存趋势。动物实验揭示低剂量(3mg/kg)方案通过血管正常化增强T细胞毒性,为临床剂量优化提供机制依据。该研究发表于《Nature Communications》,为BTC免疫联合治疗提供新策略。
胆道癌(Biliary Tract Cancer, BTC)作为仅次于肝细胞癌的第二大肝胆恶性肿瘤,其五年生存率不足10%,多数患者确诊时已失去手术机会。尽管吉西他滨联合顺铂(GC方案)是标准一线治疗,但中位总生存期(OS)仅11.7个月,且靶向治疗仅适用于少数存在FGFR2融合或IDH1突变的患者。免疫检查点抑制剂(Immune Checkpoint Inhibitors, ICIs)虽在二线治疗中展现潜力,但TOPAZ-1和KEYNOTE-966等III期研究显示,一线免疫联合化疗的生存获益增幅不足2个月。如何突破疗效瓶颈?浙江省肿瘤医院Jieer Ying团队在《Nature Communications》发表的重要研究给出了创新性答案。
研究团队设计了一项多中心随机II期临床试验(SAGC试验),首次将PD-1抑制剂sintilimab、多靶点抗血管生成药anlotinib与GC方案联用,并创新性通过临床-基础转化研究揭示剂量优化机制。关键技术包括:1) 80例晚期BTC患者的1:1随机对照设计;2) 基于mRECIST和RECIST 1.1的双重疗效评估;3) AKT/YAP诱导的原位胆管癌小鼠模型构建;4) 流式细胞术分析肿瘤免疫微环境;5) 血管灌注与缺氧区域定量检测。
患者特征与治疗暴露
研究纳入80例不可切除/转移性BTC患者(SAGC与GC组各40例),62.5%为肝内胆管癌(ICC)。SAGC组中位治疗周期为7个(范围1-22),化疗剂量强度与GC组相当。值得注意的是,22例患者接受安罗替尼8mg剂量调整后,3/4级血小板减少发生率从38.9%降至13.6%。
疗效结果
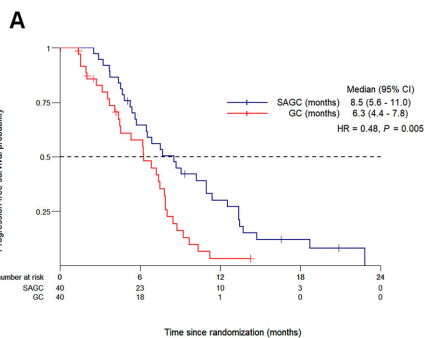
安全性特征
SAGC组3/4级治疗相关不良事件(TRAEs)发生率为75%,主要为血液学毒性(中性粒细胞减少45%)。剂量调整后8mg组4级AE发生率降低10.5个百分点。免疫相关AE均为1/2级,包括甲状腺功能异常(10%)和皮疹(10%)。
机制探索

这项研究为晚期BTC治疗带来三重突破:首先,SAGC方案成为首个在随机对照试验中证实PFS显著改善的免疫-抗血管-化疗三联方案;其次,8mg安罗替尼的剂量优化策略在提升疗效同时降低毒性,为临床实践提供重要参考;最后,通过创新性动物实验阐明低剂量抗血管药物通过"血管正常化"重塑免疫微环境的机制。研究结果不仅适用于BTC,也为其他实体瘤联合治疗策略的剂量设计提供了范式转换思路。正如讨论部分强调,该研究开启了"减毒增效"的精准联合治疗新时代,未来需进一步探索生物标志物指导下的个体化给药方案。
 生物通微信公众号
生物通微信公众号
知名企业招聘