
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于单核转录组的人类大脑神经元衰老标志物鉴定及其在神经退行性疾病中的机制研究
《npj Aging》:Identification of markers for neurescence through transcriptomic profiling of postmortem human brains
【字体: 大 中 小 】 时间:2025年07月03日 来源:npj Aging 5.4
编辑推荐:
本研究通过整合SenMayo、CSP和SIP三种衰老相关基因面板,利用特征基因方法分析人类前额叶皮层单核RNA测序数据,首次发现CDKN2D-ETS2基因对可高精度(99%)区分衰老神经元(neurescence)。研究揭示了324个差异表达基因与阿尔茨海默病(AD)、帕金森病等神经退行性疾病的线粒体功能障碍和细胞骨架失调通路显著相关,为开发神经元衰老靶向干预策略提供了新依据。
神经元衰老(neurescence)作为大脑衰老和神经退行性疾病的重要特征,长期以来因缺乏可靠标志物而难以精准识别。尽管SenMayo基因列表等工具可表征衰老相关分泌表型(SASP),但神经元特有的衰老机制仍存在巨大知识空白。这种认知局限严重阻碍了针对tau蛋白神经原纤维缠结和β淀粉样斑块等病理特征的靶向治疗开发。
为破解这一难题,由Miranda E. Orr和Habil Zare领衔的研究团队在《npj Aging》发表突破性成果。研究者创新性地整合SenMayo、经典衰老通路(CSP)和衰老启动通路(SIP)三个基因面板,对来自宗教秩序研究(ROS)队列的4套人脑前额叶皮层单核RNA测序数据集(总计80.5万个细胞核)进行特征基因(eigengene)分析。通过决策树算法和差异表达分析,首次建立神经元衰老的多维度鉴定体系。
关键技术包括:1)基于Mathys 2019等4个公共数据集构建特征基因模型;2)采用加权PCA平衡细胞类型偏差;3)结合MAST和SigEMD双算法鉴定差异基因;4)通过KEGG通路分析揭示生物学机制。
结果
Identification of specific markers for neurons
研究发现MAP2K1单基因标记准确率达99%,而CDKN2D-ETS2组合可将特异性提升至100%。

Differentially expressed genes
双算法交叉验证获得324个差异基因,其中16个核心基因(如COX6C、TUBB4A)同时富集于5大神经退行性疾病通路。
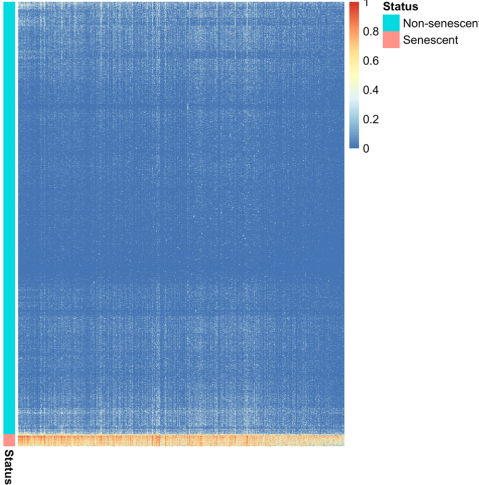
Pathway analysis
线粒体电子传递链(COX7C、UQCRB等)和微管蛋白(TUBA4A、TUBB2A)基因异常表达,提示能量代谢障碍和细胞骨架重塑是神经元衰老的关键特征。

讨论
该研究突破性地证实:1)神经元衰老具有独特的分子标签,不同于传统SASP模式;2)CDKN2D-ETS2组合可作为高特异性病理标志物;3)线粒体-细胞骨架轴可能是神经退行性疾病的共同干预靶点。尽管p19INK4D抗体特异性等限制仍需突破,但这项研究为开发延缓认知衰退的senolytics(衰老细胞清除剂)提供了全新分子靶标,对理解阿尔茨海默病等疾病的发病机制具有重要启示。
 生物通微信公众号
生物通微信公众号