
-

生物通官微
陪你抓住生命科技
跳动的脉搏
SREBP-2通过甲羟戊酸-Akt通路促进非小细胞肺癌进展的机制研究及临床意义
【字体: 大 中 小 】 时间:2025年07月03日 来源:Scientific Reports 3.8
编辑推荐:
本研究针对非小细胞肺癌(NSCLC)中胆固醇代谢异常的关键调控因子――固醇调节元件结合蛋白2(SREBP-2)展开深入探究。研究人员通过459例临床样本分析发现SREBP-2高表达与不良预后显著相关,并首次揭示其通过激活甲羟戊酸-Akt通路促进肿瘤增殖、迁移和侵袭的分子机制。动物实验证实SREBP抑制剂可显著抑制肿瘤生长,为NSCLC提供了新的预后标志物和潜在治疗靶点。
肺癌是全球癌症死亡的首要原因,其中非小细胞肺癌(NSCLC)占比高达85%。尽管诊疗技术不断进步,患者5年生存率仍不足20%,亟需探索新的治疗靶点。近年来,代谢重编程被认为是癌症的重要特征之一,胆固醇代谢异常在多种肿瘤中被发现,但其在NSCLC中的调控机制尚不明确。固醇调节元件结合蛋白2(SREBP-2)作为胆固醇合成的核心转录因子,在前列腺癌等肿瘤中已被证实具有促癌作用,但在NSCLC中的临床意义和功能机制仍是空白。
为解决这一科学问题,复旦大学附属肿瘤医院与山东第一医科大学附属省立医院的研究团队联合开展了一项系统性研究。通过分析459例NSCLC临床样本,结合体外实验和小鼠模型,首次揭示了SREBP-2在NSCLC中的表达特征、临床价值及分子机制。研究发现SREBP-2不仅可作为独立的预后指标,更通过甲羟戊酸-Akt信号通路促进肿瘤恶性进展,为NSCLC治疗提供了新的干预策略。该成果发表于《Scientific Reports》杂志。
研究主要采用免疫组织化学(IHC)分析临床样本、基因沉默/过表达技术、Transwell迁移侵袭实验、Western blot信号通路检测以及小鼠异种移植模型等关键技术方法。其中临床样本来自山东省级医院2015-2023年的完整队列,包含训练集(275例)和验证集(184例)。
SREBP-2在NSCLC中高表达并预示不良预后
通过IHC检测发现,SREBP-2在NSCLC组织中的表达显著高于癌旁正常组织。在263对匹配样本中,37.3%的肿瘤呈现SREBP-2高表达,而正常组织仅1.5%。临床相关性分析显示,SREBP-2高表达与高龄(>60岁)、晚期TNM分期(IIB-IV期)、较大肿瘤(>3cm)、T2-T4分期和淋巴结转移显著相关。生存分析证实,SREBP-2高表达患者中位生存期明显缩短,Cox多因素分析表明其是独立的预后不良因素。
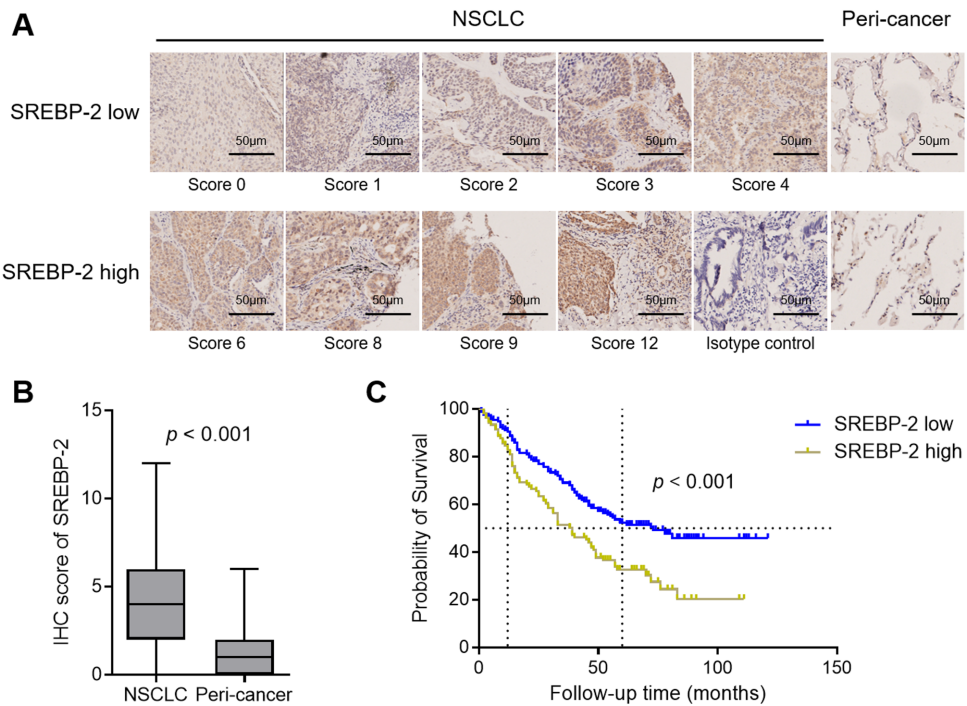
SREBP-2促进NSCLC细胞增殖、迁移和侵袭
基因功能实验显示,敲低SREBP-2可显著抑制H1299和PC-9细胞的增殖能力,CCK-8检测显示72小时增殖率下降40%-50%。Transwell实验证实,SREBP-2沉默使细胞迁移和侵袭能力降低2-3倍。相反,过表达SREBP-2能上调胆固醇合成关键酶HMGCS1、HMGCR和LDLR的表达,并促进肿瘤细胞恶性表型。特异性抑制剂fatostatin可剂量依赖性地逆转这些效应。
SREBP-2通过甲羟戊酸-Akt通路发挥作用
机制研究发现,SREBP-2敲除降低Akt(Ser473)磷酸化水平但不影响Erk1/2信号。甲羟戊酸通路抑制剂辛伐他汀可阻断SREBP-2诱导的Akt激活及促癌效应,证实该通路的关键作用。动物实验进一步验证,过表达SREBP-2使小鼠移植瘤体积增大2倍,而30mg/kg fatostatin治疗可使肿瘤生长抑制率达60%。
这项研究首次系统阐明了SREBP-2在NSCLC中的临床意义和分子机制,不仅将其确立为新的预后标志物,更揭示了靶向胆固醇代谢通路治疗NSCLC的可行性。特别值得注意的是,研究采用的SREBP抑制剂fatostatin已进入临床前评估阶段,为转化医学研究提供了直接依据。尽管高剂量fatostatin存在一定毒性,但该发现仍为开发更特异的SREBP-2抑制剂奠定了重要基础,对改善NSCLC患者预后具有重要临床价值。
 生物通微信公众号
生物通微信公众号
知名企业招聘