
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Mbnl1通过NF-κB通路调控小胶质细胞/巨噬细胞极化改善脑缺血再灌注损伤的机制研究
【字体: 大 中 小 】 时间:2025年07月04日 来源:Molecular Neurobiology 4.6
编辑推荐:
本研究针对缺血性卒中后神经炎症与认知功能障碍的临床难题,揭示了肌肉盲样蛋白1(Mbnl1)通过抑制NF-κB信号通路调控小胶质细胞M2型极化、减轻细胞凋亡和炎症反应的新机制。河北医科大学第二医院团队通过tMCAO小鼠模型和BV-2细胞OGD模型,证实Mbnl1过表达可缩小脑梗死体积、改善认知功能,为卒中治疗提供了新靶点。
缺血性卒中(Ischemic stroke, IS)作为中国致残首因,其并发症卒中后认知障碍(PSCI)严重影响患者生存质量。尽管神经保护药物研发不断推进,临床转化效果却不尽如人意。近年研究发现,过度激活的小胶质细胞释放的促炎因子如肿瘤坏死因子-α(TNF-α)和白介素-6(IL-6)会加剧神经元损伤,而M2型极化小胶质细胞则能分泌抗炎因子促进修复。肌肉盲样蛋白1(Mbnl1)作为RNA结合蛋白,虽已知与脑结构发育相关,但其在卒中后小胶质细胞极化和神经保护中的作用仍是未解之谜。
河北医科大学第二医院神经内科张向健团队在《Molecular Neurobiology》发表的研究,通过临床样本分析结合tMCAO小鼠模型和BV-2细胞氧糖剥夺(OGD)模型,综合运用激光散斑成像、免疫荧光共定位、流式细胞术等技术,系统阐明了Mbnl1通过NF-κB通路调控小胶质细胞极化改善神经功能的分子机制。研究纳入30例卒中患者和15例健康对照,检测血清Mbnl1水平与神经功能评分相关性;构建Mbnl1过表达AAV病毒注射的tMCAO小鼠模型,通过TTC染色、Y迷宫等评估神经保护效应;采用Western blot、ELISA等技术分析炎症因子和凋亡相关蛋白表达。
Mbnl1在卒中患者和动物模型中低表达
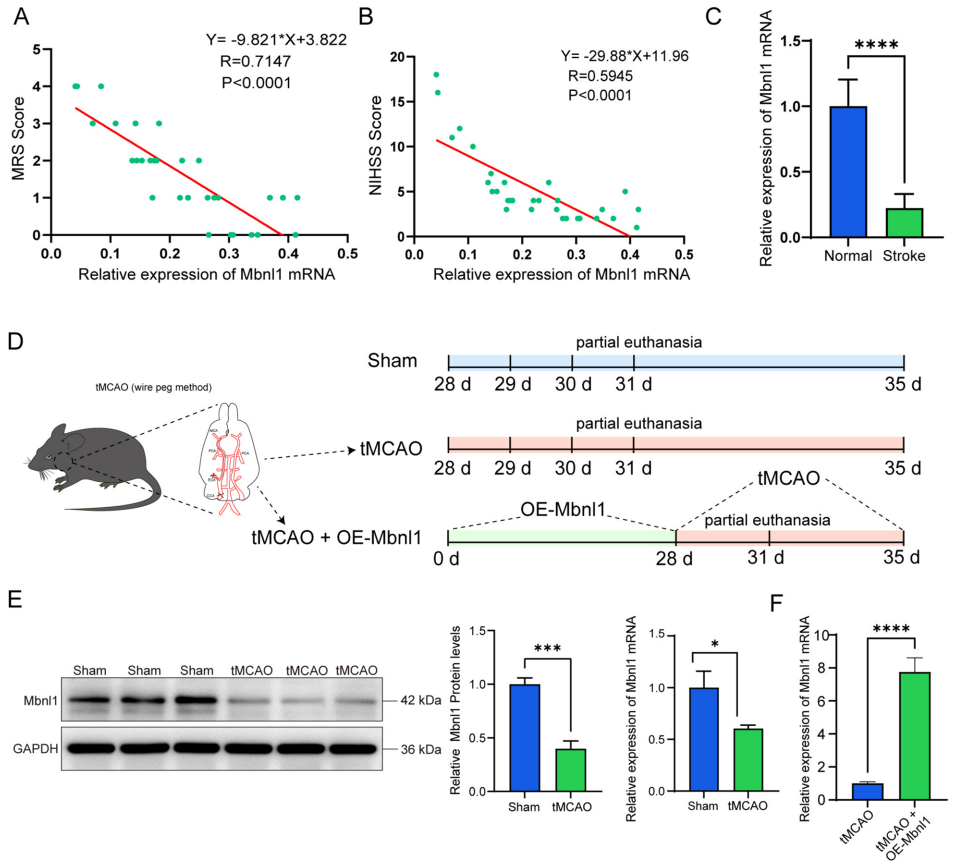
临床数据显示卒中患者血清Mbnl1 mRNA水平显著低于健康对照,且与改良Rankin量表(mRS)和美国国立卫生研究院卒中量表(NIHSS)评分呈负相关。tMCAO模型小鼠脑组织中Mbnl1蛋白和mRNA表达均显著下调,提示Mbnl1可能参与卒中病理过程。
Mbnl1改善神经功能与脑组织损伤
过表达Mbnl1使tMCAO小鼠脑梗死体积缩小42.7%,激光散斑成像显示脑血流灌注显著改善。行为学测试表明,Mbnl1过表达组在旋转棒实验中停留时间延长1.8倍,Y迷宫自发交替率提高67%,神经功能评分较模型组显著改善。
促进小胶质细胞M2型极化
免疫荧光显示Mbnl1过表达使CD206+/Iba-1+ M2型小胶质细胞比例增加2.3倍,而CD16+/Iba-1+ M1型比例降低58%。Western blot证实M2型标志物CD206和CD163蛋白表达上调,M1型标志物CD16和CD86下调。在OGD模型中,Mbnl1过表达同样显著促进BV-2细胞M2极化。
抑制细胞凋亡与炎症反应
TUNEL染色显示Mbnl1过表达使脑组织凋亡细胞减少61%,流式检测显示BV-2细胞凋亡率下降44%。分子机制上,Mbnl1上调抗凋亡蛋白Bcl-2表达,同时降低促凋亡蛋白Bax和Cleaved-caspase-3水平。ELISA检测发现Mbnl1过表达使促炎因子TNF-α和IL-6降低50%-70%,抗炎因子IL-4和IL-10升高1.5-2倍。
调控NF-κB信号通路
关键实验显示Mbnl1过表达使磷酸化p65(p-p65)/p65和磷酸化IKBα(p-IKBα)/IKBα比值分别降低62%和55%。当用LPS激活NF-κB通路时,Mbnl1对M2极化的促进作用被显著逆转,证实该通路在Mbnl1调控机制中的核心地位。
这项研究首次阐明Mbnl1通过抑制NF-κB通路促进小胶质细胞M2极化、减轻神经炎症和凋亡的分子机制,为缺血性卒中治疗提供了新思路。临床转化方面,血清Mbnl1水平可作为预后评估指标,而靶向Mbnl1的基因治疗或药物开发可能成为突破现有治疗瓶颈的新策略。未来研究需进一步验证Mbnl1在不同卒中亚型中的作用,并探索其与其他神经保护途径的协同效应。
 生物通微信公众号
生物通微信公众号
知名企业招聘