
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:应用单细胞和空间组学技术解析癌症药物反应和耐药性的细胞特征
【字体: 大 中 小 】 时间:2025年07月04日 来源:Journal of Hematology & Oncology 29.9
编辑推荐:
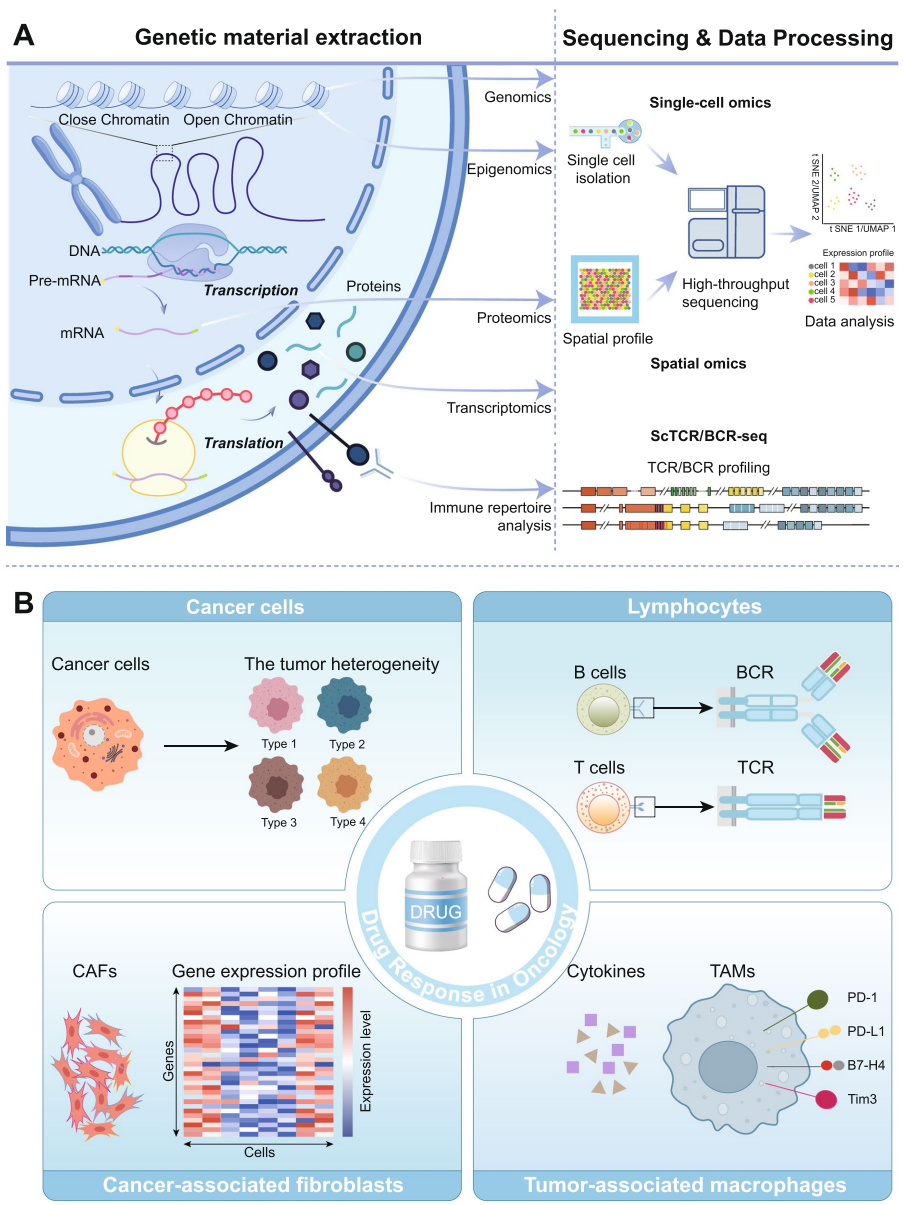
这篇综述系统阐述了单细胞组学(scRNA-seq、scATAC-seq)和空间组学(ST、SP)技术在揭示肿瘤异质性(ITH)、肿瘤微环境(TME)重编程及耐药机制中的突破性应用,重点总结了25种癌症中预测药物反应/耐药的细胞标志物(如CXCL13+ T细胞、LRRC15+ CAFs)及关键通路(JAK/STAT、PI3K-AKT),为精准医疗提供新策略。
癌症耐药性是临床治疗的主要挑战,导致高复发率和死亡率。肿瘤异质性和TME动态互作是影响疗效的核心因素。传统测序技术难以捕捉细胞间异质性,而单细胞与空间组学技术通过高分辨率解析个体细胞的基因表达、表观调控和蛋白分布,为揭示耐药机制提供了全新视角。
单细胞转录组学(scRNA-seq)能识别肿瘤细胞亚群和免疫细胞状态,例如在TNBC中发现ZNF689缺失通过LINE-1逆转录转座增加基因组不稳定性,导致免疫治疗耐药。而CXCL13+ CD8+ T细胞则预示PD-1抑制剂疗效。
单细胞表观组学(scATAC-seq)通过染色质可及性分析揭示调控元件,如卵巢癌中JAK/STAT通路激活与CAFs分泌的IL-6相关。
单细胞免疫组库分析(scTCR-seq/scBCR-seq)追踪克隆演化,例如黑色素瘤中TEM细胞扩增与免疫治疗响应正相关。
空间转录组(ST)定位基因表达的空间模式,如乳腺癌中PD-1响应者的效应T细胞更靠近肿瘤细胞,通过CD274/CD80互作增强杀伤。
空间蛋白质组(CODEX)发现肝癌中波形蛋白high巨噬细胞与Treg共定位形成免疫抑制微环境。
空间代谢组揭示胃癌边界区免疫细胞的谷氨酰胺代谢上调与免疫逃逸相关。
多组学整合(如CITE-seq)可关联转录组与蛋白表达,但面临技术成本高、数据标准化等挑战。未来需通过机器学习挖掘动态标志物,并推动临床转化,如靶向CXCR4+耗竭T细胞联合ICIs的疗法。
该领域发展需平衡数据共享与隐私保护,并通过前瞻性临床试验验证标志物的临床价值,最终实现个体化治疗。
 生物通微信公众号
生物通微信公众号
知名企业招聘