
-

生物通官微
陪你抓住生命科技
跳动的脉搏
单细胞RNA测序揭示近视中前向跨突触变性及突触重塑加剧的分子机制
【字体: 大 中 小 】 时间:2025年07月04日 来源:Experimental & Molecular Medicine 9.5
编辑推荐:
本研究通过单细胞RNA测序技术揭示了近视发展中视网膜神经节细胞凋亡诱导的视觉通路前向跨突触变性(TSD)现象。研究人员发现Fos基因介导的视网膜神经元凋亡会触发视觉皮层突触结构和功能异常,通过多模态技术证实了近视中"眼-脑"协同功能障碍的病理机制,为近视防治提供了新的分子靶点。
近视已成为全球性的公共卫生问题,预计到205年全球近半数人口将受其困扰。随着近视度数增加,黄斑病变、开角型青光眼等并发症风险显著上升。尽管已知视网膜损伤会导致视觉皮层退化(称为前向跨突触变性),但近视中这一过程的分子机制仍不清楚。山东中医药大学附属眼科医院等机构的研究团队在《Experimental & Molecular Medicine》发表重要成果,首次系统揭示了近视中视网膜神经节细胞凋亡如何通过视觉通路影响大脑皮层功能。
研究人员采用多学科交叉方法,通过构建豚鼠近视模型,结合单细胞转录组测序、功能磁共振成像、电生理等技术开展研究。关键实验包括:1) 使用-6.0D镜片诱导豚鼠近视模型;2) 对视网膜和视觉皮层进行单细胞RNA测序和核RNA测序;3) 采用7.0T小动物MRI进行脑功能成像;4) 通过膜片钳记录视觉皮层神经元突触电流;5) 利用透射电镜观察突触超微结构。
【RGC凋亡发生在近视中】
单细胞测序分析显示近视豚鼠视网膜中Fos表达显著上调,与凋亡信号通路激活相关。免疫荧光和TUNEL检测证实视网膜神经节细胞凋亡增加,伴随Bcl-2下降和Bax升高。钙离子流检测显示视网膜Ca2+外流增加,而Fos基因敲除可逆转这些变化。视网膜厚度测量显示近视组全视网膜和神经节细胞层变薄。
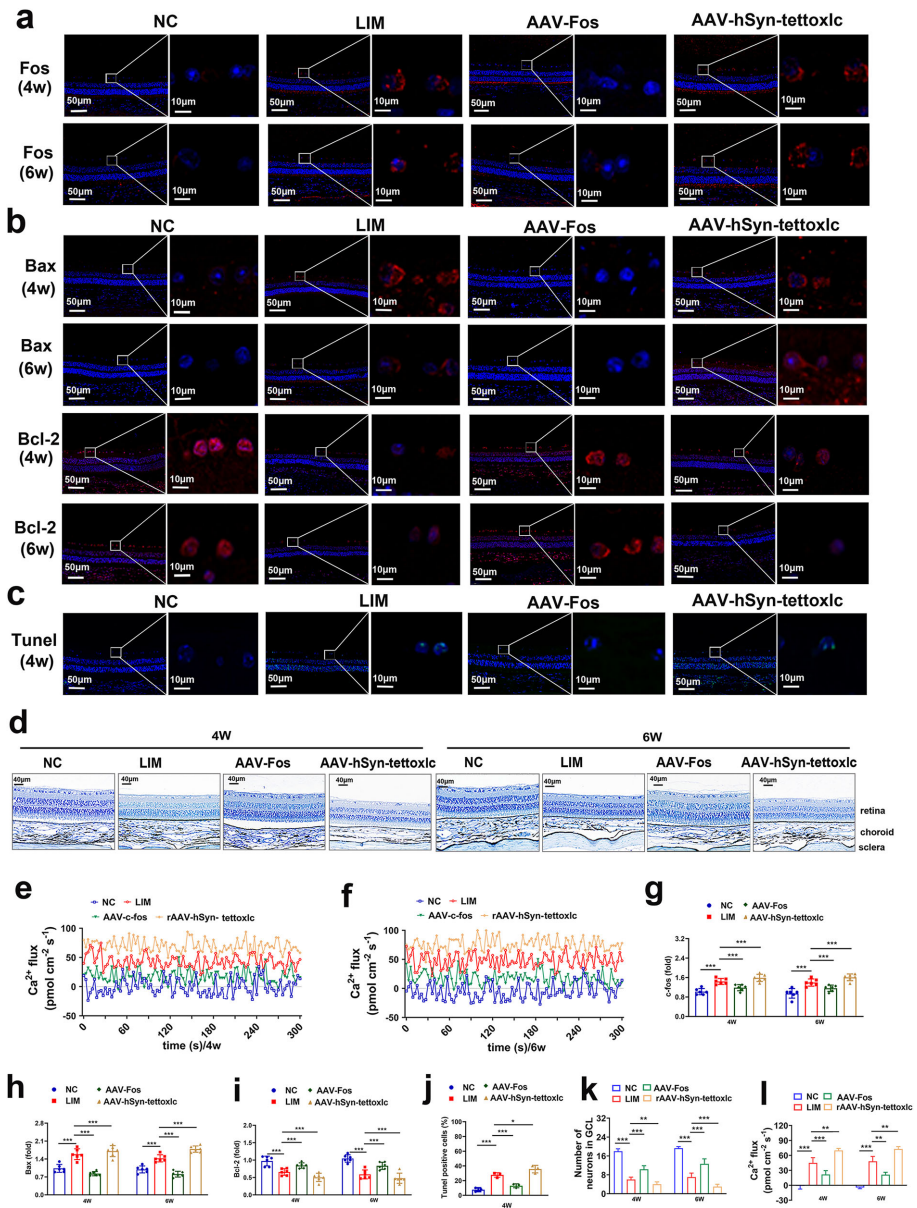
【RGC凋亡导致视觉通路失活】
功能MRI显示近视组视神经各向异性分数(FA)值增加,而视束轴向扩散率(AD)降低。视觉皮层与下丘脑等脑区的功能连接(FC)异常,局部一致性(ReHo)值在初级视觉皮层单眼区降低。闪光视觉诱发电位(FVEP)检测显示P1、P2波幅降低。高尔基染色显示视交叉和外侧膝状体(LGN)神经元结构损伤,树突密度下降。
【视觉皮层神经元兴奋性降低】
单细胞测序发现视觉皮层兴奋性神经元数量和比例减少。钙离子流检测显示视觉皮层Ca2+外流增加。低频振幅(ALFF)分析表明初级视觉皮层神经元兴奋性降低。突触后密度蛋白95(PSD95)表达下降,透射电镜观察到突触密度、长度和突触小泡数量减少。

【突触重塑加剧】
膜片钳记录显示自发性兴奋性突触后电流(sEPSC)幅值和频率降低,而抑制性电流(sIPSC)增加。长时程增强(LTP)诱导实验显示近视组场兴奋性突触后电位(fEPSP)增幅减小。突触相关基因ERBB4、NLGN1等表达显著下调。高尔基染色显示视觉皮层神经元树突棘数量减少。
这项研究首次证实近视中存在前向跨突触变性现象,揭示了Fos介导的视网膜神经节细胞凋亡通过视觉通路影响皮层功能的分子机制。研究发现近视不仅导致视网膜结构损伤,还会引起视觉皮层突触可塑性改变,表现为长时程抑制增强和神经元兴奋性降低。通过AAV载体敲除Fos基因可有效抑制视网膜凋亡和下游通路损伤,这为开发针对近视神经退行性变化的干预策略提供了新思路。该研究创新性地将眼科疾病与神经退行性病变研究相结合,为理解近视的"眼-脑"协同病理机制奠定了重要基础。
研究也存在一定局限,如未对Fos干预后的单细胞转录组变化进行分析。未来研究可进一步探索不同视觉剥夺模型对视觉系统各层面的长期影响,以及TSD与长时程抑制的具体关联机制。这些发现不仅对近视防治具有重要临床意义,也为理解神经退行性疾病的跨突触传播机制提供了新视角。
 生物通微信公众号
生物通微信公众号
知名企业招聘