
-

生物通官微
陪你抓住生命科技
跳动的脉搏
细胞互作中IFNγ的差异表达:区分局部与弥漫型色素沉着绒毛结节性滑膜炎及类风湿关节炎的生物学标志与治疗新视角
【字体: 大 中 小 】 时间:2025年07月05日 来源:Arthritis Research & Therapy 4.4
编辑推荐:
本研究针对色素沉着绒毛结节性滑膜炎(PVNS)与类风湿关节炎(RA)的病理差异,通过对比滑膜细胞对炎症刺激和免疫细胞互作的响应机制,揭示局部型PVNS中IFNγ的高分泌与IL-10的负相关性特征。团队发现局部型PVNS滑膜细胞诱导IFNγ的能力显著高于弥漫型及RA,且迁移能力与细胞因子分泌谱存在亚型特异性差异,为PVNS的靶向治疗提供分子依据。成果发表于《Arthritis Research & Therapy》,推动个体化诊疗策略发展。
关节疾病中,色素沉着绒毛结节性滑膜炎(PVNS)是一种罕见的侵袭性滑膜增生病变,分为局部型(单结节)和弥漫型(全滑膜受累),常导致关节肿胀、疼痛和骨破坏。尽管其病理特征与类风湿关节炎(RA)相似――如滑膜细胞异常增殖和免疫细胞浸润――但PVNS的分子机制尚不明确。当前手术切除后复发率高达40%,且缺乏靶向治疗方案。更棘手的是,局部型与弥漫型PVNS的生物学行为差异显著,却无明确分子标志物区分。法国里昂市民 Hospices Civils de Lyon 的研究团队由此提出核心问题:PVNS滑膜细胞是否具有独特的炎症响应模式?其与免疫细胞的互作如何驱动疾病特异性进展?
研究通过三大实验体系对比PVNS与RA滑膜细胞:
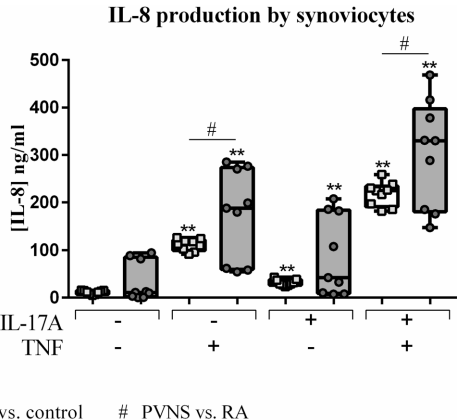
在IL-17/TNF刺激下,PVNS与RA滑膜细胞均显著上调IL-6和IL-8分泌,且双因子联合呈现协同效应(p≤0.01)。但RA细胞分泌IL-8的量显著高于PVNS(174.8 vs 111.0 ng/ml),提示滑膜基质细胞的基础炎症状态存在疾病特异性。

在PBMC共培养体系中,局部型PVNS滑膜细胞展现出独特诱导能力:
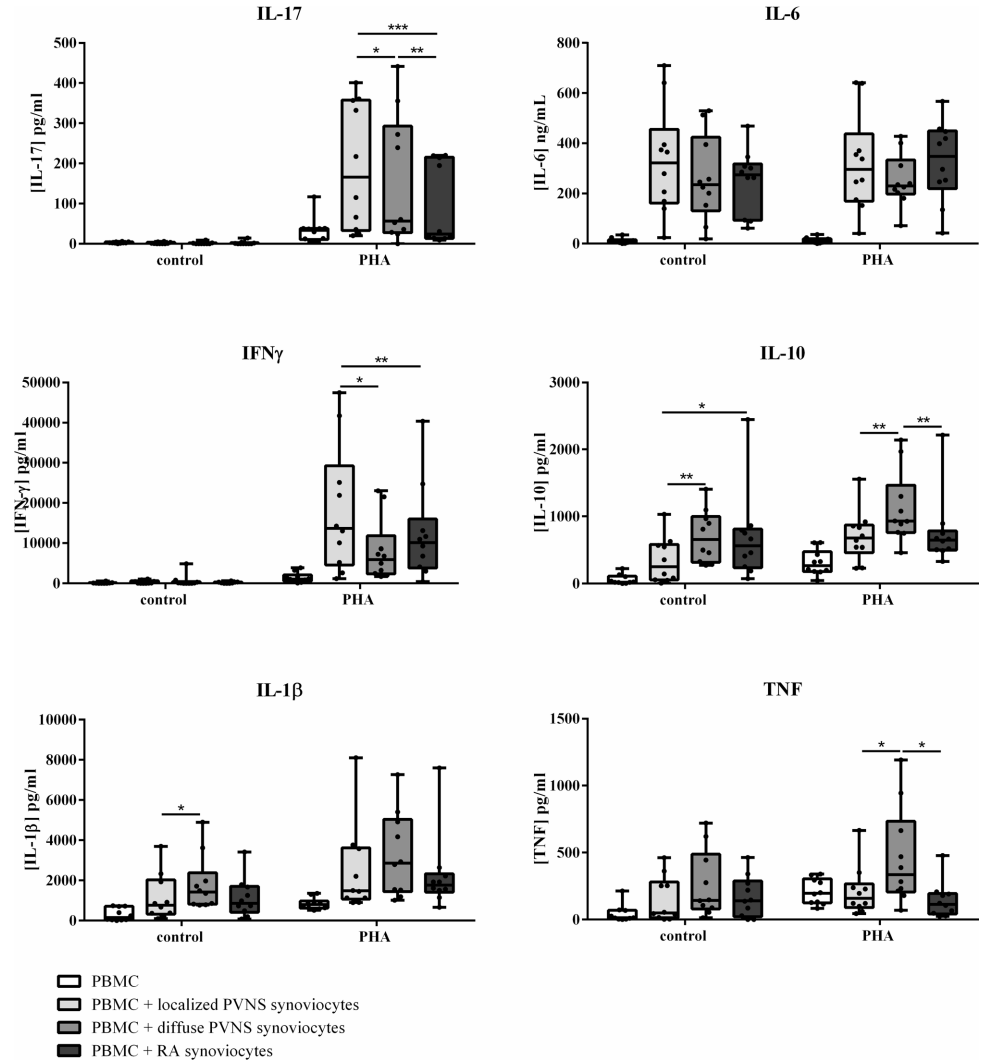
本研究首次揭示:局部型PVNS通过滑膜细胞驱动IFNγ优势应答,而弥漫型倾向IL-10介导的免疫抑制。这种失衡与疾病行为直接关联:IFNγ可抑制破骨细胞形成,解释局部型较低的骨破坏性;而弥漫型的高IL-6和高IL-10则与其侵袭性及复发风险相关。
临床转化价值:
该研究发表于《Arthritis Research & Therapy》,为罕见关节疾病的精准分型与治疗奠定分子基石,推动PVNS从"一刀切"手术迈向个体化靶向时代。
 生物通微信公众号
生物通微信公众号
知名企业招聘