
-

生物通官微
陪你抓住生命科技
跳动的脉搏
NCOA4在胶质母细胞瘤中的临床价值:诊断、预后及治疗靶点新发现
【字体: 大 中 小 】 时间:2025年07月08日 来源:BMC Cancer 3.4
编辑推荐:
本研究针对胶质母细胞瘤(GBM)预后差、治疗靶点匮乏的临床难题,通过多组学分析结合实验验证,首次系统揭示了铁蛋白自噬关键蛋白NCOA4在GBM中的三重价值:其低表达与肿瘤恶性程度呈负相关,可作为独立预后标志物(HR=0.421);通过调控铁死亡(Ferroptosis)和B细胞信号通路,影响免疫微环境浸润;为GBM的精准诊疗提供了新靶点。
胶质母细胞瘤(GBM)作为WHO IV级最致命的脑肿瘤,患者中位生存期不足两年。尽管现有分子标志物如IDH1/2突变、MGMT甲基化等已应用于临床,但受限于肿瘤异质性和动态演变,亟需发现更可靠的生物标志物。近年研究发现,核受体辅激活因子4(NCOA4)通过介导铁蛋白自噬(Ferritinophagy)调控铁死亡(Ferroptosis),在多种癌症中发挥抑癌作用。然而,NCOA4在GBM中的临床意义尚属空白。贵州医科大学附属医院联合团队在《BMC Cancer》发表的研究,首次揭示了NCOA4在GBM诊断、预后预测和免疫调控中的多维价值。
研究采用TCGA-GBMLGG、CGGA和TCGA-GBM三大数据库进行生物信息学分析,结合27例不同级别胶质瘤样本的免疫组化实验。通过生存分析、Cox回归模型评估预后价值,利用TIMER和GEPIA2平台解析免疫浸润特征,并采用GO/KEGG富集分析阐明生物学功能。
NCOA4在胶质瘤中的表达模式
数据分析显示,NCOA4表达随WHO分级升高而显著降低,GBM中达最低值(p<0.05)。免疫组化验证发现,II级胶质瘤NCOA4水平显著高于III级和IV级(GBM)(p<0.001)。组织学亚型分析表明,GBM的NCOA4表达低于少突胶质细胞瘤、星形细胞瘤等低恶性亚型(p<0.05)。
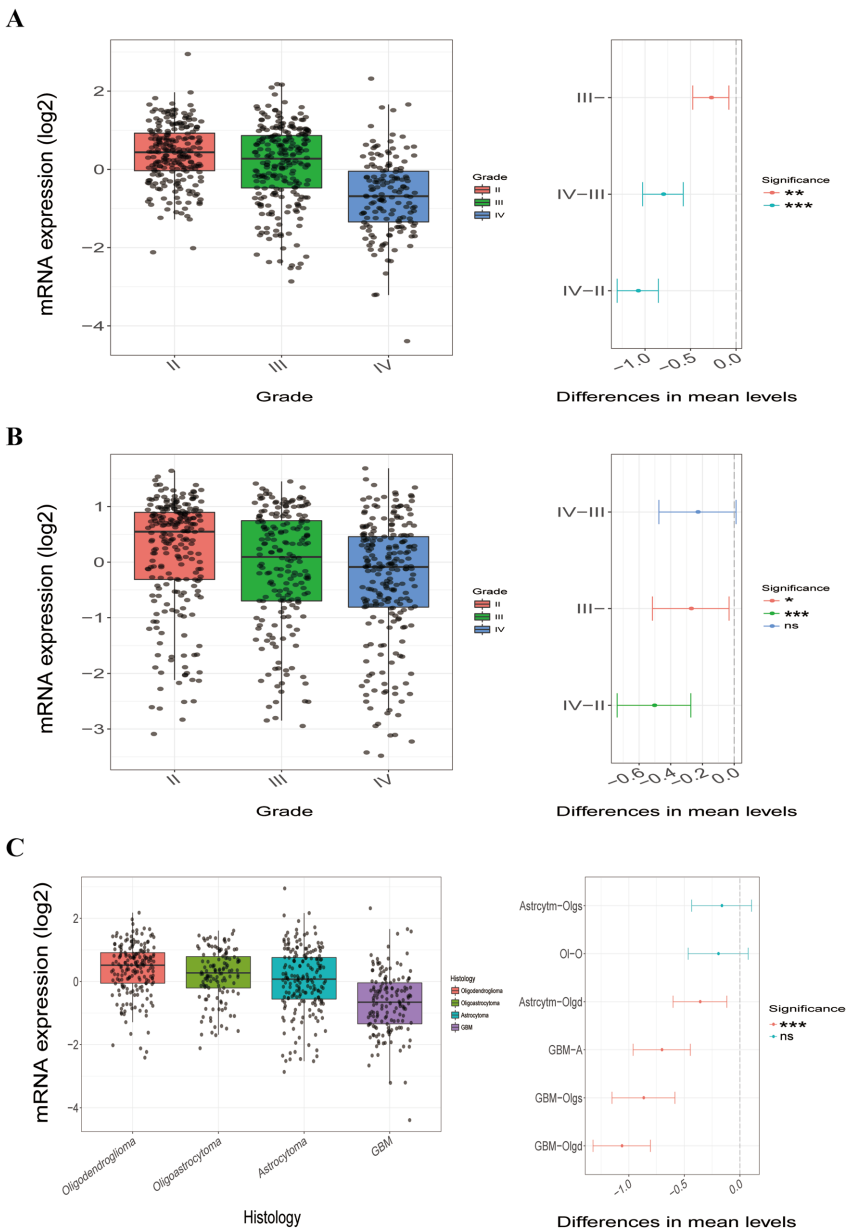
NCOA4与GBM临床病理特征
NCOA4在经典分子亚型和NON-G-CIMP型GBM中表达最低(p<0.05),这两种亚型已知预后最差。年轻患者(≤60岁)和亚洲人群NCOA4水平更高(p<0.05),与较好预后群体特征吻合。
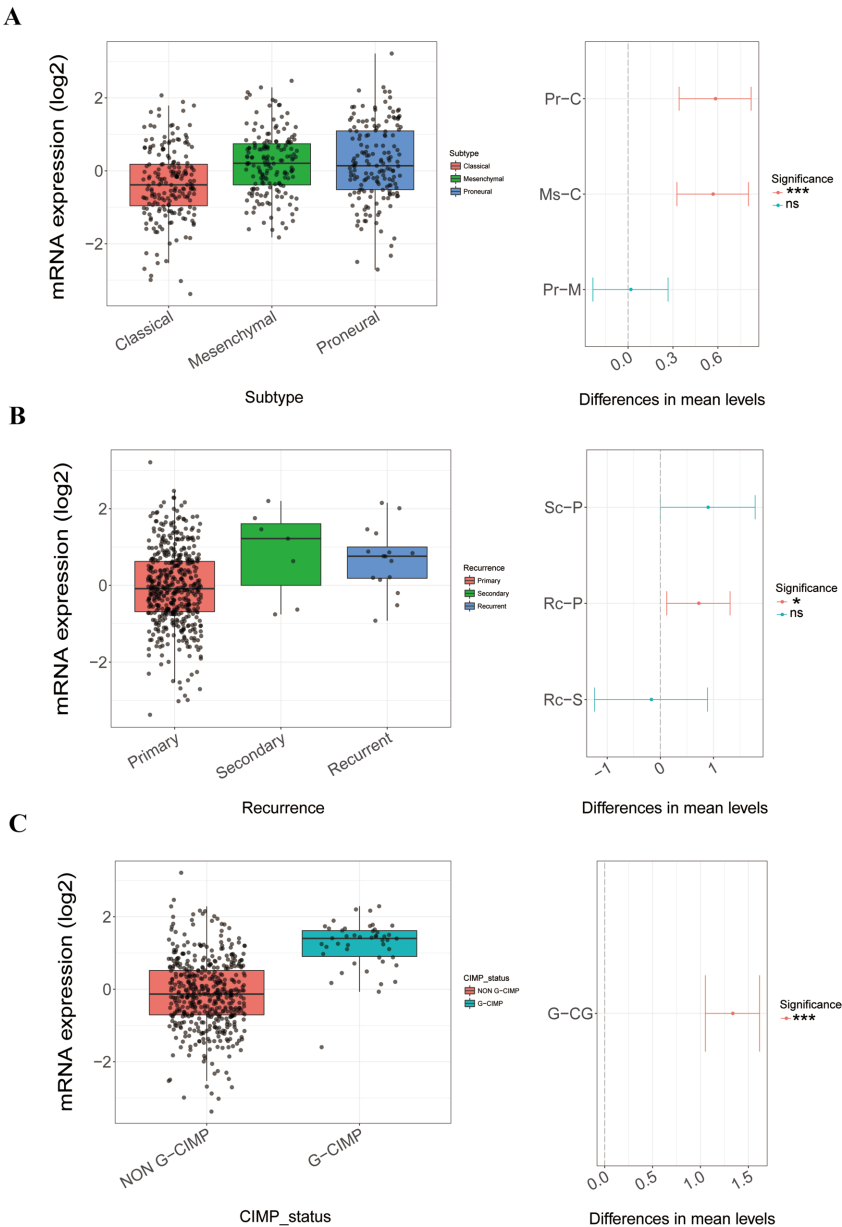
预后价值与免疫调控机制
低NCOA4表达组中位生存期显著缩短(HR=0.421,95%CI:0.326-0.544),且为独立预后因素(p<0.001)。其低表达与B细胞(CD19/CD38)、巨噬细胞(CD68/CD86)等免疫细胞浸润不足相关(p<0.05),而后者与患者不良预后直接相关。

生物学功能解析
GO/KEGG分析揭示NCOA4主要参与铁离子稳态、自噬体形成等过程,显著富集于铁死亡和B细胞受体信号通路(p<0.05)。

该研究首次系统阐明NCOA4在GBM中的三重临床价值:诊断方面,其表达梯度可作为恶性度判读指标;预后方面,是独立于现有标志物的预测因子;治疗方面,通过调控铁死亡和免疫微环境成为潜在靶点。特别值得注意的是,NCOA4与B细胞浸润的正相关性为理解GBM免疫抑制微环境提供了新视角。尽管存在未检测铁死亡标志物等局限,但研究为开发NCOA4激动剂(如人参皂苷Rg5、葛根素等天然化合物)提供了理论依据,未来或可通过联合诱导铁死亡和增强免疫浸润实现协同治疗。
 生物通微信公众号
生物通微信公众号
知名企业招聘