
-

生物通官微
陪你抓住生命科技
跳动的脉搏
肿瘤微环境中乳酸化修饰(Lactylation)的复杂调控网络:从代谢废物到癌症治疗新靶点
【字体: 大 中 小 】 时间:2025年07月08日 来源:The Innovation 33.2
编辑推荐:
本研究聚焦乳酸在癌症中的新型调控角色――乳酸化修饰(Lactylation),揭示其如何通过酶促/非酶促机制修饰组蛋白与非组蛋白(如p53、微管相关蛋白),调控基因表达、细胞骨架动态、有丝分裂及化疗耐药。北京大学团队系统解析了乳酸化转移酶(如p300/AARS1)的分子机制,阐明其对染色体不稳定性(CIN)和肿瘤代谢重编程的驱动作用,为靶向乳酸化克服抗癌药物耐药提供了新视角。
过去一个世纪,乳酸在癌症研究中的身份经历了戏剧性转变:从沃伯格效应(Warburg effect)中的代谢废物,到重塑肿瘤微环境的酸化因子,再到调控信号通路的关键分子。然而,张尚航等学者发现,乳酸竟能作为新型翻译后修饰(PTM)的底物――乳酸化修饰(Lactylation),为癌细胞的猖獗生长增添全新注脚。这种修饰如何改写细胞命运?其复杂调控网络又为癌症治疗带来哪些启示?
北京大学联合团队在《The Innovation》发表研究,系统揭示乳酸化修饰在癌症中的多重作用机制。研究不仅发现新型乳酸化转移酶(如AARS1/AARS2),更首次阐明乳酸化通过破坏微管动态稳定性(dynamic instability)、干扰染色体分离,直接导致癌细胞有丝分裂异常和化疗耐药。该成果为理解肿瘤代谢与表观遗传的交互作用提供了关键桥梁。
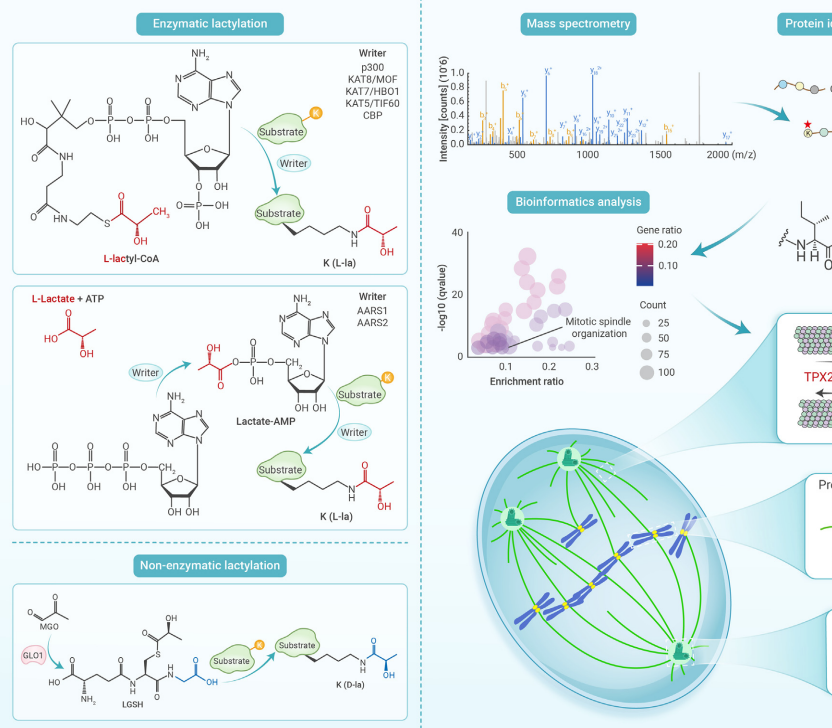
研究整合质谱技术鉴定组蛋白/非组蛋白乳酸化位点(覆盖4种癌症类型临床样本);利用AlphaFold预测乳酸化转移酶结构域;通过功能实验(如CRISPR筛选、微管动态成像)验证乳酸化对细胞骨架蛋白(如TPX2/NUMA1)的调控机制;结合临床队列分析乳酸化水平与化疗耐药相关性。
1. 乳酸化修饰的双重合成机制
乳酸化通过两种途径发生:

2. 新型乳酸化转移酶的发现
细胞质中氨酰-tRNA合成酶AARS1以ATP依赖方式乳酸化p53,破坏其相分离及DNA结合能力;线粒体AARS2则修饰PDHA1/CPT2,重编程代谢通路。
3. 乳酸化驱动细胞骨架功能紊乱
临床质谱数据显示,TPX2(微管成核因子)、NUMA1(中心体调控蛋白)等细胞骨架蛋白在胃肠癌/肝癌中高频乳酸化:
4. 染色体不稳定性(CIN)的乳酸化根源
乳酸化直接干扰染色体分离关键蛋白:
5. 乳酸化介导化疗耐药的新机制
微管靶向药物(如紫杉醇)耐药性与肿瘤乳酸水平呈正相关:
本研究首次构建乳酸化修饰在癌症中的全局调控图谱:从代谢底物到PTM执行者,乳酸通过修饰细胞骨架蛋白(TPX2/NUMA1/微管蛋白)和染色体分离因子(WAPL/CHAMP1),直接导致微管动态失衡、中心体扩增和染色体错误分离。这些发现为解释肿瘤细胞有丝分裂异常及化疗耐药提供了全新代谢-表观遗传视角。
未来研究需突破三大方向:
乳酸化研究虽处起步阶段,但其作为"乳酸信号"的核心载体,正在改写我们对癌症代谢适应性的认知――它不仅是肿瘤微环境的产物,更是癌细胞操纵生命活动的精密分子工具。
 生物通微信公众号
生物通微信公众号
知名企业招聘